阿斯利康达格列净片再夺“首”,市场却不被看好?
当地时间5月5日,美国食品和药物管理局(FDA)宣布已批准Farxiga(达格列净片,安达唐)用于降低射血分数降低的成人心力衰竭患者心血管死亡和因心力衰竭住院的风险。Farxiga是这一特殊药物类别中的第一个SGLT2抑制剂,被批准用于治疗心力衰竭且射血分数降低的成年人。
Farxiga在一项临床试验中被证明可以改善射血分数降低的成人心力衰竭患者的生存率和减少住院治疗的需要。这是一项有4744名受试者参与的随机、双盲、安慰剂对照试验,对Farxiga的安全性和有效性进行了评估。受试者的平均年龄为66岁,大多数为男性(77%)。为了确定药物的有效性,研究人员检查了患者心血管死亡、因心力衰竭住院和紧急心力衰竭就诊的发生率。受试者被随机分配接受每日一次的10mg Farxiga或安慰剂(非活性治疗)的治疗。大约18个月后,接受Farxiga治疗的患者相比接受安慰剂治疗的患者,发生心血管死亡、因心力衰竭住院和紧急心力衰竭就诊的更少。
FDA药物评价和研究中心心内科和肾脏科主任Norman Stockbridge表示:“心力衰竭是一种严重影响健康状况的疾病,八分之一的美国人因此死亡,将近650万的美国人受到影响,这项批准为射血分数降低的心力衰竭患者提供了一种新的治疗选择,可以提高生存率,减少住院治疗的需要。”
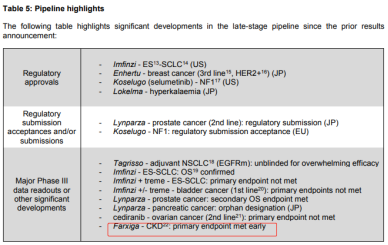
Farxiga在2014年获FDA批准结合饮食和锻炼,用于改善2型糖尿病患者的血糖控制,2017年3月在中国获批上市,成为了在中国上市的首个SGLT2抑制剂。去年,扩大其使用范围,FDA批准用于伴有中度肾损害的2型糖尿病(T2D)患者;后又批准用于治疗因T2D引起,已确诊的心血管疾病(CVD)或多发性心脏病引起的心力衰竭(hHF)。在临床试验方面,今年3月,Farxiga治疗慢性肾脏病(CKD)患者的III期DAPA-CKD试验取得了压倒性的疗效;阿斯利康与美国圣卢克中美洲心脏研究所合作启动一项随机全球III期试验,评估Farxiga治疗COVID-19住院患者的潜力,这些患者可能出现严重并发症,如器官衰竭。Farxiga在欧盟于去年上半年获批治疗1型糖尿病(T1D)成人患者,但在去年7月,FDA拒绝了Farxiga治疗T1D的补充新药申请(sNDA)。
SGLT2抑制剂市场竞争压力大,各大产品强势进入心衰治疗市场。Farxiga的另外2个竞争对手Invokana(卡格列净)和礼来的Jardiance(恩格列净)都被FDA批准了降低2型糖尿病患者主要心血管不良事件(MACE)和因心衰住院风险的适应症。
Farxiga在2019年的销售额为15.43亿美元,相比2018年增长了10.9%。阿斯利康2020年第一季度的财报显示,Farxiga的总收入为4.07亿美元。虽然在2020年的第一季度Farxiga的总收入在阿斯利康的药物销售排在前几名,也不断扩大其适应症范围,但是它未来的市场并不被看好。
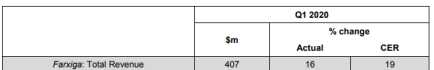
数据来源:阿斯利康
根据Evaluate Pharma 2017年的数据显示,预测Farxiga在2022年的全球销售额将达21.46亿美元,有望成为抗糖尿病药物的佼佼者,当时更是被预测为阿斯利康的TOP1产品。但是据医药市场调研机构Evaluate Pharma近日发布的一份长期预测报告显示,阿斯利康有三款药物在2026年有巨大销售潜力,其中并不包括Farxiga,他们是治疗慢性阻塞性肺病的Breztri Aerosphere、阿斯利康与第一三共针对肿瘤领域而合作研发的Enhertu和阿斯利康与安斯泰来、Fibrogen合作研发的Evrenzo。
参考来源:
1.FDA approves new treatment for a type of heart failure
2.Long term forecasts confirm Keytruda’s dominance
3.阿斯利康官网财报

责任编辑:杰尼龟
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。


• 撬动100亿$ AD药物度普利尤单抗“王者”地位,礼来能否后来者居上?
• 加快药物开发流程!分子结晶技术新突破
• 礼来收购VS基石合作!RET抑制剂市场火药味十足!
• 安排!赛诺菲Dupixent新指征,AMD理想靶点找到
• 诺和诺德NASH药物超车吉利德?打响霸主争夺战
• 阿斯利康达格列净片再夺“首”,市场却不被看好?
• 最“火爆”研发管线新鲜出炉!恒瑞、吉利德、诺华、斯微生物...
• FDA“自打脸”?氯喹和羟氯喹还能治疗COVID-19吗?
• 全球首款!FDA批准转移性三阴乳腺癌靶向ADC药物加速上市
• 诺华公布Mayzent最新临床数据!艾伯维伊布替尼第11项适应症获批!
合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





