撬动100亿$ AD药物度普利尤单抗“王者”地位,礼来能否后来者居上?
8月2日,Evaluate Vantage 的最新报告称,赛诺菲和再生元的 Dupixent 是目前特应性皮炎(atopic dermatitis,AD)领域的王者;但礼来希望通过其竞争者 lebrikizumab 打破现状,这将很快产生关键数据。
Dupixent下一个“修美乐”?
Dupixent(度普利尤单抗)是一种全人源性单克隆抗体,特异性抑制2种关键蛋白IL-4和IL-13的过度激活信号,从而调节下游一系列细胞因子和趋化因子的释放,达到调节炎症的作用;由赛诺菲和再生元共同开发。
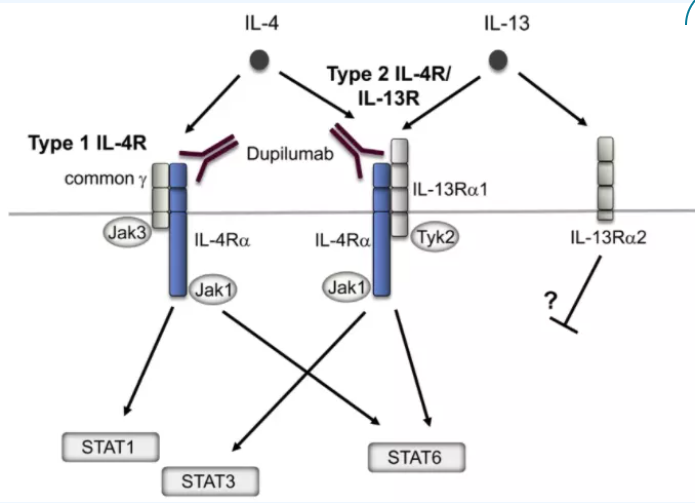
(来源:Dupilumab: Basic aspects and applications to allergic diseases, Allergology International)
2017年3月Dupixen获得美国FDA批准,用于外用处方药无法充分控制病情或不适合这些药物治疗的中度至重度特应性皮炎成人患者。这项批准,使Dupixent成为首个用于治疗成人中重度特应性皮炎的靶向生物药。Dupixent曾被NMPA/CDE纳入境外已上市的临床急需境外新药第二批名单;2020年6月18日以治疗成人中重度特异性皮炎进入中国市场。这款特应性皮炎疗法在中国从递交申请到正式获批,不到6个月的时间。
上市后,Dupixent销售额一路高歌,首年实现销售额 2.47亿美元;2018年实现销售额8.73亿美元;2019年全球销售收入即达到23亿美元。2020年销售额达35.34亿欧元,增加73.9%。已然成为重磅炸弹药。
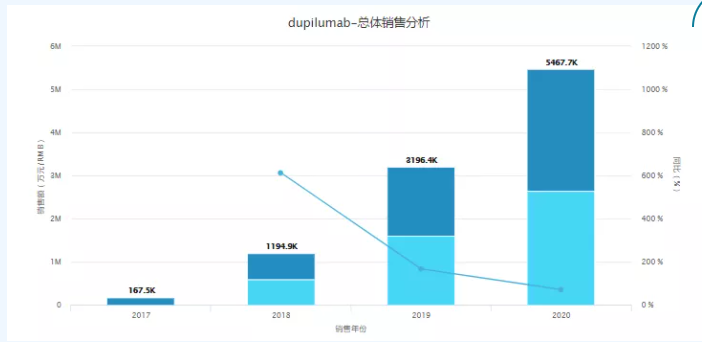
图片来源:药智数据全球畅销药品数据库
值得提及的是,Dupixent被誉为可能会是下一个 “修美乐”,尽管目前其全球销售与修美乐存在很大的差距,追上也有一定的困难,不过据药智数据不完全统计,Dupixent正在扩展适应症已发掘潜力市场,已有哮喘、变异性支气管肺曲霉菌病、慢性荨麻疹、嗜酸性粒细胞性食管炎、神经性皮炎、荨麻疹、大疱性类天疱疮、痒疹、慢性阻塞性肺疾病等10种适应症处于临床研究3期,顺利获批上市,具有巨大的市场潜力,而修美乐上市近20年也不过16个适应症。
Dupixent优异的市场表现成为目前AD药物治疗市场的引领者。无疑会吸引更多的竞争者进军此领域,想要打破Dupilumab一枝独秀的地位。众多竞争者中,礼来制药为其中一员;8月2日,Evaluate Vantage 的最新报告称,礼来希望通过其 lebrikizumab 打破Dupilumab领导地位,并将很快产生关键数据。
打破Dupilumab一枝独秀
礼来“重磅炸弹”在手?
据悉,2020年初,礼来(Lilly)以总价约11亿美元的价格收购Dermira,以扩大其免疫学管线。作为协议的一部分,礼来公司获得了可能成为Dupixent竞争对手的中度至重度特应性皮炎候选药物lebrikizumab。
lebrikizumab的2b期随机临床试验结果显示在成人中重度特应性皮炎(AD)患者的广泛临床表现中提供了快速、剂量依赖性的疗效,并显示出良好的安全性。而这个结果与Dupixent的功效类似,据Evaluate Vantage记者Madeleine报道,如果lebrikizumab能重现2b期随机临床试验结果,那礼来将拥有一个“重磅炸弹”在手,但是如果lebrikizumab表现不尽人意,那lebrikizumab将在特应性皮炎领域不知前景。

图片来源:JAMA Network
报告显示,礼来希望lebrikizumab能够在第三阶段赶上Dupixent,lebrikizumab有几个优势可能有助于其项目获得市场份额。第一,更方便的给药方式,每四周一次,Dupixent为每两周一次:第二,安全,早期的lebrikizumab试验发现结膜炎发生率低,这也是Dupixent的一个常见的不良反应。第三,lebrikizumab在止痒方面表现不错。Dupixent的两个关键性特应性皮炎试验Solo 1和Solo 2的主要终点是相同的IGA测量,为lebrikizumab提供了一个基准。

资料来源:Dupixent label&JAMA皮肤病学
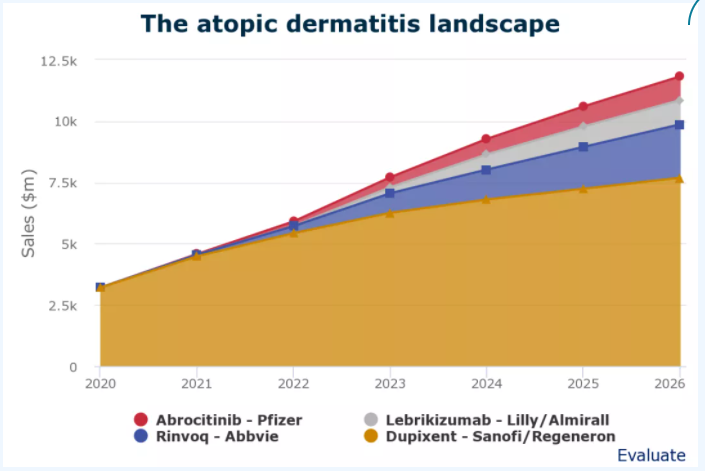
Evaluate Pharma将lebrikizumab列为特应性皮炎的第三大销售商,预计2026年销售额为9.9亿美元。在这之前的是辉瑞(Pfizer)的abrocitinib(阿布昔替尼)和艾伯维(Abbvie)的JAK抑制剂Rinvoq(upadacitinib)。
安全性不良,NDA审查延长
礼来lebrikizumab能否弯道超车
然而,今年3月评估每日一次口服abrocitinib治疗中度至重度特应性皮炎的3期JADE COMPARE研究(NCT03720470)的完整结果发表在国际医学期刊《新英格兰医学杂志》(NEJM)。该研究在接受背景外用疗法的中度至重度AD成人患者中开展,评估了2种剂量abrocitinib(100mg和200mg)与安慰剂的疗效和安全性。该研究中还包括了一个阳性药物对照组,该组患者接受了皮下注射Dupixent(dupilumab)治疗。结果显示,2种剂量abrocitinib均达到了共同主要终点。
abrocitinib(100mg,200mg)用于治疗年龄≥12岁中度至重度AD患者的新药申请(NDA)也正在接受美国FDA的审查。

图片来源:《新英格兰医学杂志》(NEJM)
4月7日,辉瑞发布公告称,美国FDA将口服抗炎药abrocitinib新药申请(NDA)的优先审查期延长了3个月,至第三季度初。在公告中,辉瑞并没有披露FDA推迟审查期的原因。
有分析师表示,此次推迟全为JAK抑制剂审查的推迟,表明FDA将对该类别的全部药物进行严格审查。而原因就是辉瑞的JAK制剂Xeljanz与传统的TNF抑制剂相比,与心脏相关的不良事件的风险增加。
受此次审查推迟影响的还有艾伯维Rinvoq的 2份sNDA (治疗中重度AD成人患者、治疗活动性银屑病关节炎成人患者)。
Rinvoq在2019年获得美国FDA批准,用于对甲氨蝶呤应答不足或不耐受(MTX-IR)的中度至重度活动性类风湿性关节炎(RA)成人患者的治疗。Rinvoq现已被欧盟委员会(EC)批准治疗3种风湿适应症:类风湿性关节炎、银屑病关节炎、强直性脊柱炎。Rinvoq被认为极有可能接任Humira成为新一任“药王”。然而,此次由于担心JAK类药物缺乏安全性,艾伯维推迟了对特应性皮炎的试验。
所以未来谁将称霸特应性皮炎市场,这还是个未知数,赛诺菲的Dupixent、辉瑞的abrocitinib、艾伯维的Rinvoq和礼来的lebrikizumab,你pick谁呢?
参考来源:
1.最畅销特应性皮炎生物药Dupixent中国获批
2.Lilly’s lebrikizumab looks to outdo Dupixent
3.赛诺菲2020年业绩 | Dupixent跃居榜首 Libtayo不断拓展新适应症
4.辉瑞abrocitinib和Xeljanz审查遭FDA推迟3个月
5.Efficacy and Safety of Lebrikizumab, a High-Affinity Interleukin 13 Inhibitor, in Adults With Moderate to Severe Atopic Dermatitis doi:10.1001/jamadermatol.2020.0079
6.Abrocitinib versus Placebo or Dupilumab for Atopic Dermatitis DOI: 10.1056/NEJMoa2019380
7.艾伯维公布Rinvoq的最新数据,Rinvoq能否顺利接棒Humira?

责任编辑:三七
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。

• 撬动100亿$ AD药物度普利尤单抗“王者”地位,礼来能否后来者居上?
• 加快药物开发流程!分子结晶技术新突破
• 礼来收购VS基石合作!RET抑制剂市场火药味十足!
• 安排!赛诺菲Dupixent新指征,AMD理想靶点找到
• 诺和诺德NASH药物超车吉利德?打响霸主争夺战
• 阿斯利康达格列净片再夺“首”,市场却不被看好?
• 最“火爆”研发管线新鲜出炉!恒瑞、吉利德、诺华、斯微生物...
• FDA“自打脸”?氯喹和羟氯喹还能治疗COVID-19吗?
• 全球首款!FDA批准转移性三阴乳腺癌靶向ADC药物加速上市
• 诺华公布Mayzent最新临床数据!艾伯维伊布替尼第11项适应症获批!
合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





