2018年1月CDE药品审评情况分析报告
看点:
1.本月药审中心受理总量为514个(不计复审)。
2.本月两项1类化药提交新药上市申请。
3.北京华素制药股份有限公司申报的中药1类新药——知母皂苷BII及胶囊,目前已进入IND序列排队待审。
根据药智数据库最新统计,2018年1月份CDE共承办新的药品注册申请以受理号计有514个(复审除外,下同)。
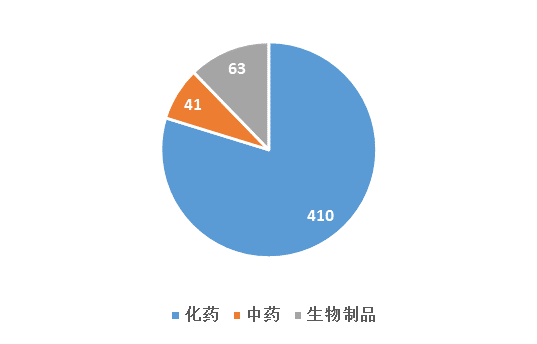
图一 2018年1月CDE药品受理情况
本月受理总量突破500,新年伊始,算是开了一个好头。相比12月增加18.7%,其中化药410个,中药41个,生物制品63个。以下让我们分析一下化药、中药、生物制品的注册受理及审评情况。
一 化药审评情况
1月份CDE共承办新的化药注册申请以受理号计有410个。
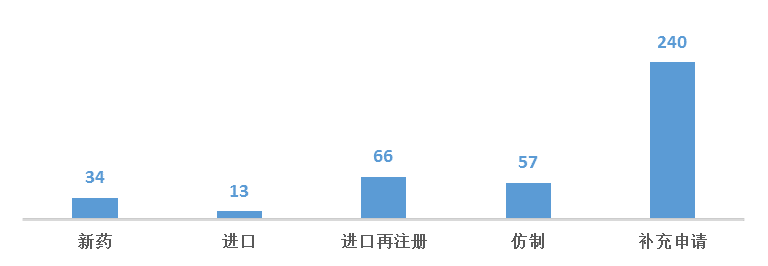
图二 2018年1月CDE化药各申请类型受理情况
从化药的申报来看,本月的承办数据了为近半年来最高值,主要由于补充申请数量大幅增加。
1.化药1类新药申报情况
本月CDE受理化药1类新药共计25个受理号,涉及10个品种11家企业,同时有两项为新药的上市申请。下图为1月新承办1类新药。
表一 2018年1月新承办的化药1类新药
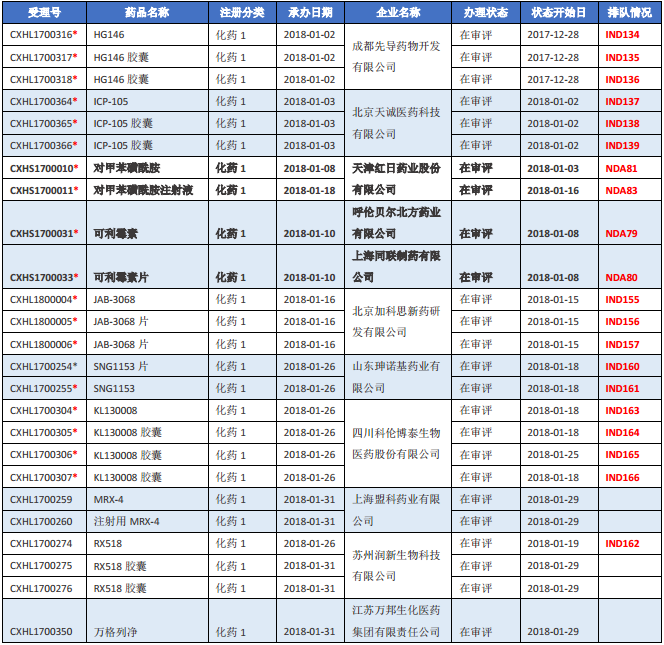
注:1.排队序号截止至2018年2月5日;2.“*”为特殊审批品种。
可利霉素作为国家重大专项产品,在2010年首次申报上市,随后2017年又申请了复审,但最终上市未果。2018年再度提交上市申请,目前已纳入特殊审批品种。
对甲苯磺酰胺注射液原申报临床申请人为北京健达康新药开发有限公司(受理号CXHB0800314),并于 2009 年 4 月获得了三期临床《药物临床试验批件》。 在完成临床试验后,北京健达康于2012年4月将此项目在中国的全部知识产权和所有权转入天津红日健达康医药科技有限公司。2014年5月,对甲苯磺酰胺原料药和对甲苯磺酰胺注射液的上市申请获得药审中心承办(受理号CXHS1400079,CXHS1400080),由天津红日药业股份有限公司红日健达康和天津红日药业股份有限公司联合申报,但在2015年的“722”临床数据自查中主动撤回。时隔两年,二度提交申报上市(来源于其上市公告)。
表二 对甲苯磺酰胺相关国内临床试验信息
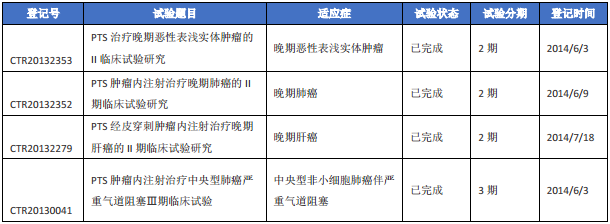
北京加科思新药研发有限公司的1类创新药——JAB-3068的临床试验于2018年1月16日获得CDE受理。据称,研究显示JAB-3068单独口服给药能够促进CD8+T细胞杀伤肿瘤的功能,也可以与PD1/PD-L1抗体联合应用,所以,JAB-3068将用于PD-1/PD-L1抗体无应答的肿瘤治疗。加科思创立于2015年,管理层由留美海归博士团队和业内资深的新药研发及管理团队组成,董事长王印祥博士是贝达药业创始人之一。此外,加科思宣布JAB-3068此前已在美国申请了临床试验,并且已获得FDA的批准。
KL130008胶囊是四川科伦药业股份有限公司控股子公司四川科伦博泰生物医药股份有限公司自主研发且具有知识产权的创新小分子JAK抑制剂,拟用于类风湿关节炎的治疗。临床前研究数据表明:KL130008作用机制明确,高效选择性抑制JAK激酶活性,实现显著缓解类风湿关节炎病情的同时,兼具良好的安全性和耐受性。申报规格分别为1 mg;2 mg;5mg(以分子实体计)(来源于其上市公告)。
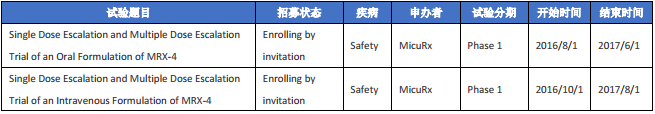
MRX-1 是新一代噁唑烷酮类抗菌药,与利奈唑胺等第一代同类抗菌药相比,MRX-1 在确保疗效的基础上大幅提高了对造血系统的安全性。此次上海盟科申报的MRX-4 是 MRX-1 的前药,可通过静脉注射或口服的形式达到全身给药的疗效。目前已在美国开展了一期临床试验。
表三 MRX-4相关美国临床试验信息
万格列净为全新结构的 SGLT-2 抑制剂,主要用于Ⅱ型糖尿病适应症治疗。该新药由 Sirona Biochem Corp.自主研发,万邦医药在2014年获 Sirona Biochem Corp.于中国境内(不包括港澳台地区,下同)的研发、生产、商业化权利等授权,对该新药进行系统的药学和非临床研究,符合临床试验申请要求(来源于其上市公告)。
2.化药1类进口药申报情况
本月2项进口化药1类药获得承办。
表四 2018年1月新承办的化药1类进口药

注:1.排队序号截止至2018年2月5日;2.“*”为特殊审批品种。
二 中药审评情况
1月份CDE承办新的中药注册申请受理号共计41个,其中新药9个,补充申请32个。
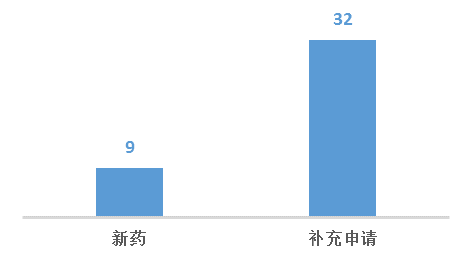
图三 2018年1月CDE中药受理情况
本月有一项中药1类新药获得承办,北京华素制药股份有限公司申报的知母皂苷BII及胶囊。知母皂苷 BII系列药物是军事医学科学院放射与辐射医学研究所自主开发、国际首创的新型中药有效成分脑血液循环改善剂。未来有望成为疗效肯定、安全性好、具有我国自主知识产权的新型抗痴呆药物。 2015年,北京华素制药股份有限公司以人民币 6,000 万元的价格向中国人民解放军军事医学科学院放射与辐射医学研究所购买国家 1 类新药知母皂苷 BII 原料药、胶囊,国家 1类新药知母皂苷 BII 注射用原料药、注射液及相关保健品智参颗粒的相关专利的独占许可使用权。
三 生物制品审评情况
1月份CDE承办新的生物制品注册申请受理号共计63个,新药32个,补充申请23个,进口5个。
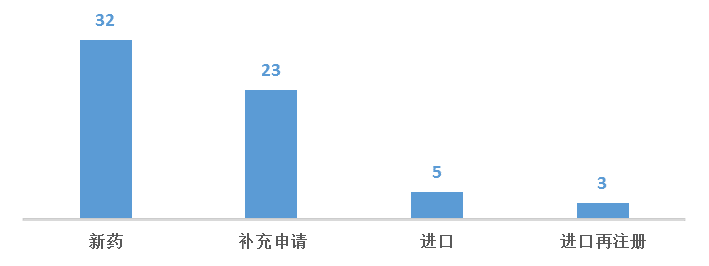
图四 2018年1月CDE生物制品受理情况
本月有9个1类治疗用生物制品获得承办,目前均已经进入相应序列排队待审。
表五 2018年1月新承办的治疗用生物制品1类新药
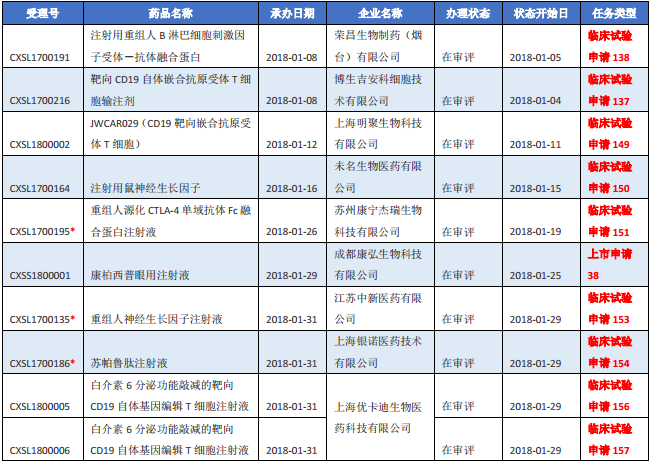
注:1.排队序号截止至2018年2月5日;2.“*”为特殊审批品种。
注:本文以上文章刊载内容知识产权归药智网所有,如需转载,请注明出处和本文链接。
点击下载报告:





合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938


