2018年2月CDE药品审评情况分析报告
看点:
1.本月药审中心受理总量为570个(不计复审)。
2.本月17项1类化药提交新药临床试验申请。
根据药智数据库最新统计,2018年2月份CDE共承办新的药品注册申请以受理号计有570个(复审除外,下同)。
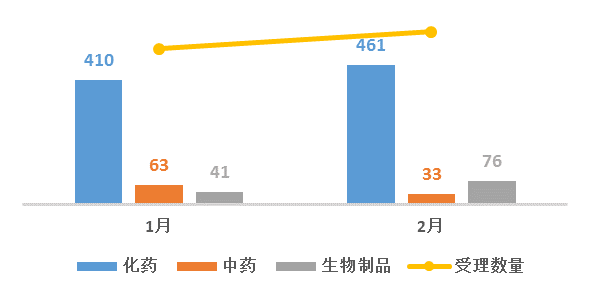
图1 2018年1-2月CDE药品受理情况
本月受理总量创近两年来的新高,其中还包含了春节假期。相比1月增加10.9%,相比去年同总量翻了一番,其中化药461个,中药33个,生物制品76个。以下让我们分析一下化药、中药、生物制品的注册受理及审评情况。
一 化药审评情况
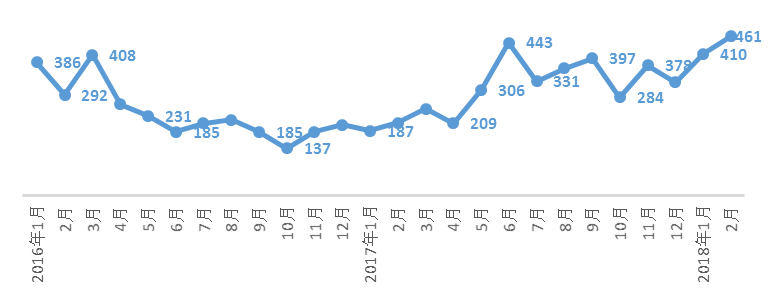
图2 2016年-2018年每月CDE化药受理情况
从图1可以看出,从2016年4月起CDE受理的化药数据开始呈下降趋势,最小值出现在2016年10月,仅为137,这种申报低迷的情况一直维持到2017年下半年才开始出现缓解。
2018年2月份CDE共承办新的化药注册申请以受理号计有461个。
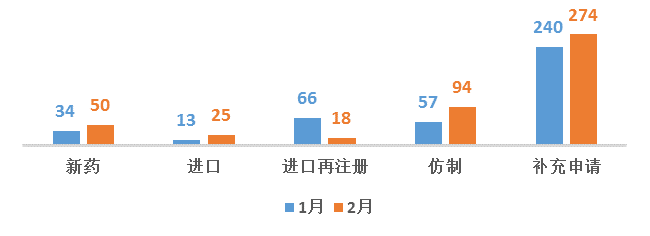
图3 2018年1-2月CDE化药各申请类型受理情况
从化药的申报来看,本月的承办数据继续增加,除进口再注册减少之外,其余申请均有不同程度的增加。
1.化药1类新药申报情况
本月CDE受理化药1类新药共计47个受理号,涉及17个品种17家企业。下图为2月新承办1类新药。
表一 2018年2月新承办的化药1类新药
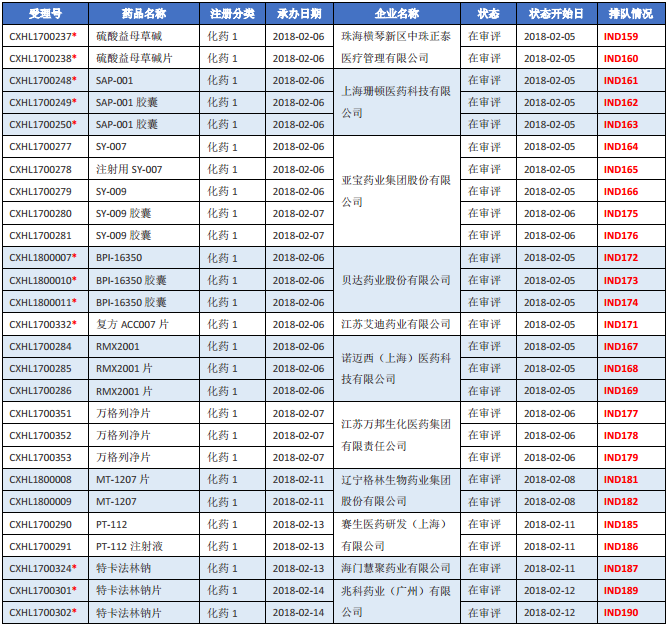
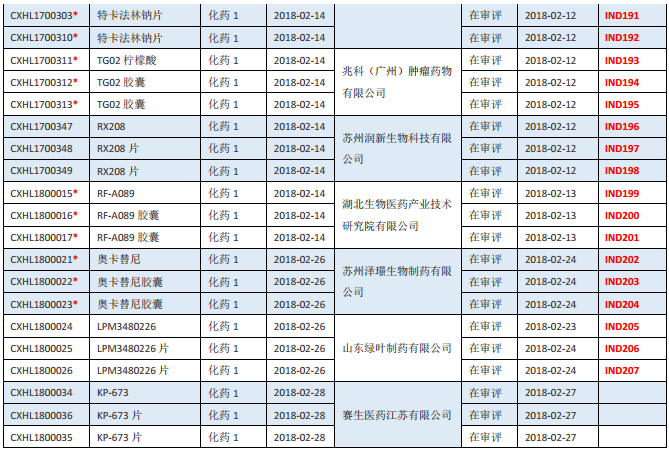
注:1.排队序号截止至2018年3月5日;2.“*”为特殊审批品种。
硫酸益母草碱又名 SCM-198 单体化合物,由珠海横琴新区中珠正泰医疗管理有限公司(以下简称“中珠正泰”)与复旦大学联合申报。该药品是复旦大学科研团队利用我国传统中药资源,经过独立研究与开发,在传统妇科用药益母草中筛选出异于传统适应证的活性单体,适应症为治疗高血脂。中珠正泰与复旦大学双方共同享有技术成果的署名权;对于本药品可能取得的临床批件所产生的商业权益,全部归中珠正泰享有。
上海珊顿医药科技有限公司和诺迈西(上海)医药科技有限公司都是2016年才注册的新公司,分别为外国法人独资和中外合资,均为首次在我国提交药品注册申请。
贝达药业股份有限公司自主研发的抗肿瘤新药——BPI-16350 胶囊及其原料药,目前已进入IND序列排队待审。其针对的靶点为细胞周期蛋白依赖性激酶 4/6(CDK4/6),拟单药或与激素疗法联合,主要用于治疗激素受体阳性和人类表皮生长因子受体2阴性(HR 阳性/HER2 阴性)的绝经后晚期或转移乳腺癌患者,还可用于Rb+的其他癌症的一、二线或联合治疗。目前,美国食品药品监督管理局批准了三个 CDK 4/6抑制剂药物,包括辉瑞公司的Palbociclib(帕博西尼, 商品名:Ibrance) 、诺华公司的Ribociclib(瑞博西尼,商品名:Kisqali)以及礼来公司的Abemaciclib(商品名:Verzenio)。(来源其上市公告)
SY-007 是亚宝药业集团股份有限公司与加拿大Primary Peptides公司合作开发的用于治疗脑卒中的新型注射药物。SY-009是公司与美国礼来制药公司合作开发的用于治疗Ⅱ型糖尿病的新型口服药物。
RF-A089为新一代的间变性淋巴瘤激酶(简称“ALK” )抑制剂,属于化药1类新药,由人福医药集团股份公司和控股子公司湖北生物医药产业技术研究院有限公司联合申请,本次申请拟定适应症为ALK阳性的局部晚期或转移性非小细胞肺癌,有潜力扩展适应症至除非小细胞肺癌以外的ALK阳性其他肿瘤。
2017年3月,江苏艾迪药业有限公司抗艾滋病一类新药ACC007正式获得国家食品药品监督管理局颁发的《药物临床试验批件》。此次申报为ACC007的复方制剂。
赛生医药研发(上海)有限公司申报的PT-112及注射剂,其注射剂在2017年由赛生医药江苏有限公司申报过进口,适应症为晚期实体瘤和晚期肝细胞癌,本次按国产1类新药再次提交注册申请。
表二 PT-112相关药品注册信息
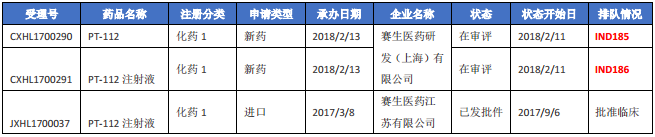
2.化药1类进口药申报情况
本月3项进口化药1类药获得承办。
表三 2018年2月新承办的化药1类进口药
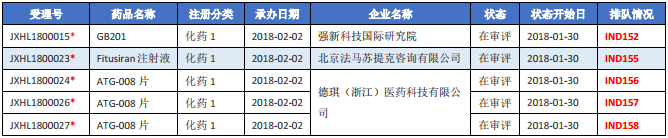
注:1.排队序号截止至2018年3月5日;2.“*”为特殊审批品种。
二 中药审评情况
2月份CDE承办新的中药注册申请受理号共计33个,其中新药6个,补充申请27个。
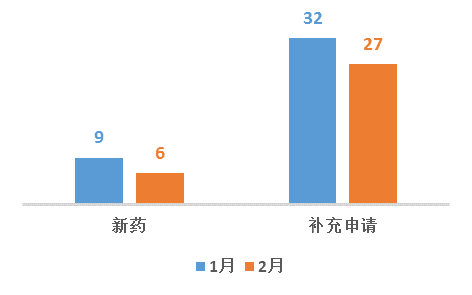
图4 2018年1-2月CDE中药受理情况
三 生物制品审评情况
2月份CDE承办新的生物制品注册申请受理号共计76个,新药39个,补充申请28个,进口8个,进口再注册1个。
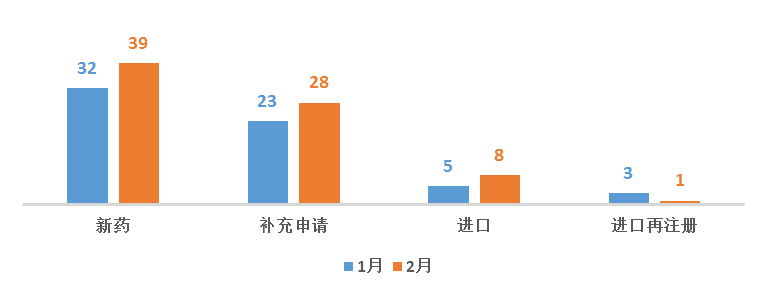
图5 2018年1-2月CDE生物制品受理情况
四 按一致性评价申报的品种情况
本月共计6个品种按一致性评价要求进行申报。
表四 2018年2月新承办一致性评价品种

注:本文以上文章刊载内容知识产权归药智网所有,如需转载,请注明出处和本文链接。
点击下载报告:





合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938


