2017年2月CDE药品审评情况分析报告

据药智数据库最新统计,2017年2月份CDE共承办新的药品注册申请以受理号计有285个(复审除外,下同)。
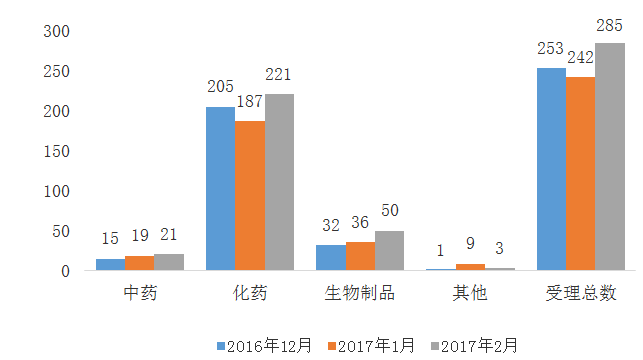
图一 2016年12月与2017年1月、2月CDE药品受理情况
2017年2月,受理总量285个较过去两个月有较明显的增长,除1月份受理数量受放假影响外,总局为2017年开了一个好头,果真是撸起袖子加油干。在2月27日举办的国新办发布会上,国家食药监总局局长毕井泉也晒出了2016年“成绩单”注册申请积压的件数已经由2015年高峰时的22000件降到现在8000件左右。本月从CDE收审情况来看,2月受理注册的品种其中化药221个,中药21个,生物制品50个,体外诊断试剂2个,药用辅料1个。以下让我们来分析一下化药、中药、生物制品的注册受理及审评情况。
一、化药
2月份CDE共承办新的化药注册申请以受理号计有221个。(不计复审)
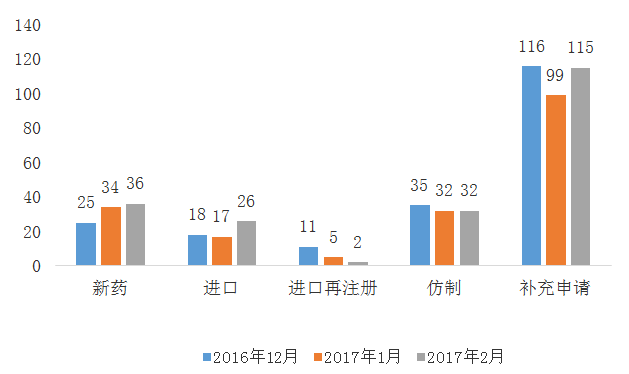
图二 2016年12月与2017年1月、2月CDE化药各申请类型受理情况
从近3个月来看,申报数量基本持平。本月申报新药共受理36个(涉及13个品种,13个厂家),包含一个旧3.1类新药,进口受理26个(涉及16个品种,16个厂家),进口再注册2个(涉及1个品种,1个厂家),仿制申请32个(涉及23个品种,23个厂家),补充申请115个。
1.化药1类新药申报情况
本月CDE受理化药1类共计35个受理号,涉及12个品种12家企业。下图为2月新承办的1类新药。
表一 2017年2月新承办的化药1类新药
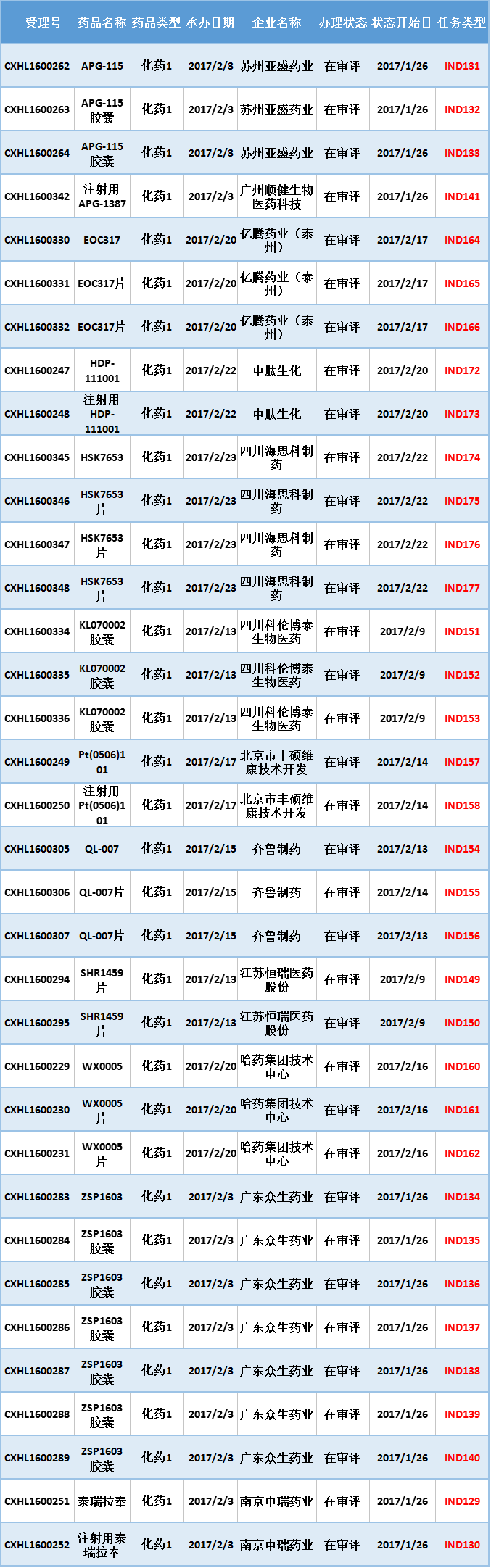
注:排队序号截止至2017年3月1日
2017年2月份广东众生药业申报第三款1类新药ZSP1603及其胶囊剂,依旧是与药明康德合作开发。去年2016年10月份广东众生药业与药明康德合作开发的ZSP1601片、ZSP1602胶囊进入审评中心,本次ZSP1603胶囊进入审评中心,半年不到,已申报3个化药1类新药。ZSP1601片用于治疗非酒精性脂肪肝炎、ZSP1602胶囊治疗小细胞肺癌等恶性肿瘤。而ZSP1603胶囊则具有2个适应症:特发性肺纤维化(IPF)和恶性肿瘤,每种适应症3种规格(12.5mg,50mg,100mg)。
表二 2016年10月至今广东众生药业申报的化药1类新药
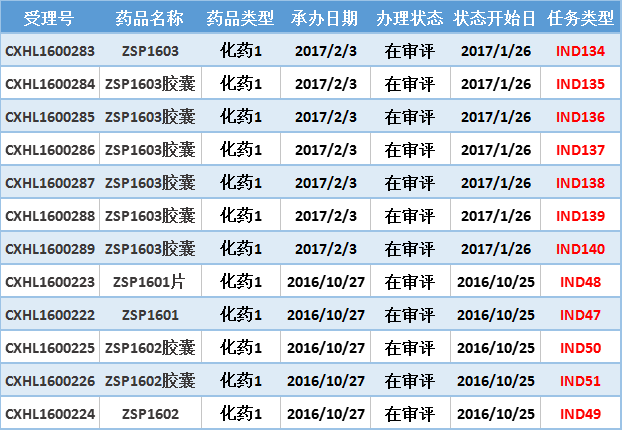
注:排队序号截止至2017年3月1日
本月苏州亚盛药业有限公司又一款1类化药APG-115及其胶囊剂进入审评中心,3个月内CDE共受理5个受理号。APG-115为口服高度选择性靶向MDM2-p53蛋白结合的小分子抑制剂,临床前研究数据表明,APG-115对肉瘤、原发肝癌、原发胃癌等肿瘤可形成高效抑制,动物试验给药可让肿瘤组织完全消失。另外APG-115对干性老年眼底黄斑病变具有显着的治疗作用。本品已于2016年10月在美国获批进入Ⅰ期临床,目前正处于招募状态。
表三 2016年12月至今苏州亚盛药业申报的化药1类新药
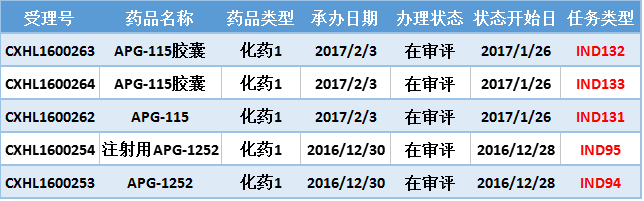
注:排队序号截止至2017年3月1日
2.化药1类进口药申报情况
本月CDE共受理进口化药1类共10个(涉及4个品种,4个厂家)。
表四 2017年2月新承办的化药1类进口药
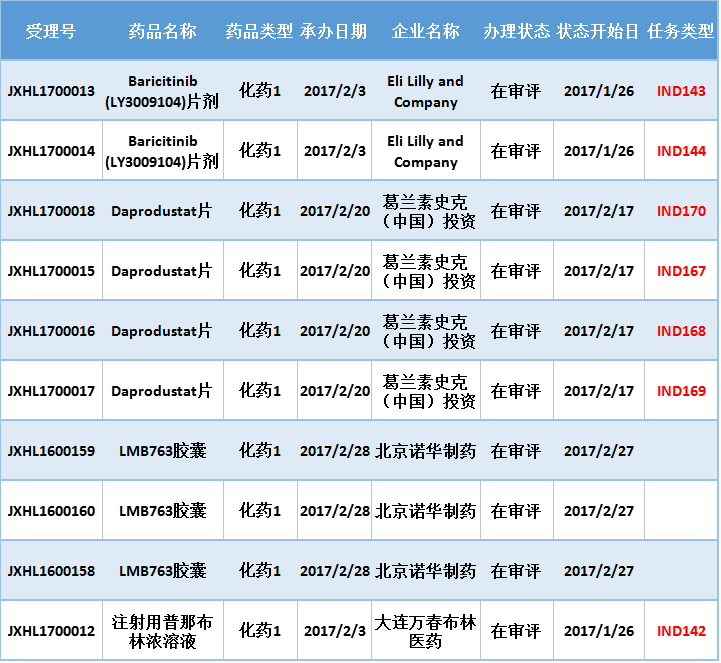
注:排队序号截止至2017年3月1日
3.化药仿制药申报情况
化药仿制32个,涉及23个品种,23个厂家。其中按旧6类申报的仿制药以受理号计有13个,涉及11个品种;按新的4类仿制药申报的受理号有15个,涉及12个品种。
按新的3类申报的仿制药以受理号计有4个,涉及4个品种。分别是:
表五2017年2月新承办的化药仿制药3类
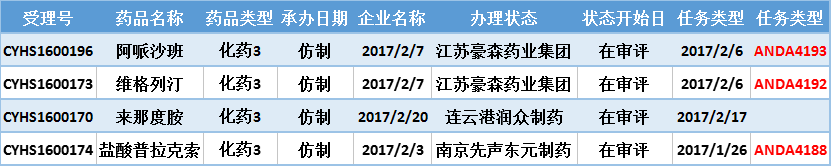
二、中药
2月份CDE承办新的中药注册申请受理号共计21个,其中新药3个(涉及3个品种,3个厂家),补充申请14个(涉及13个品种,10个厂家),进口再注册4个(涉及2个品种,2个厂家)。
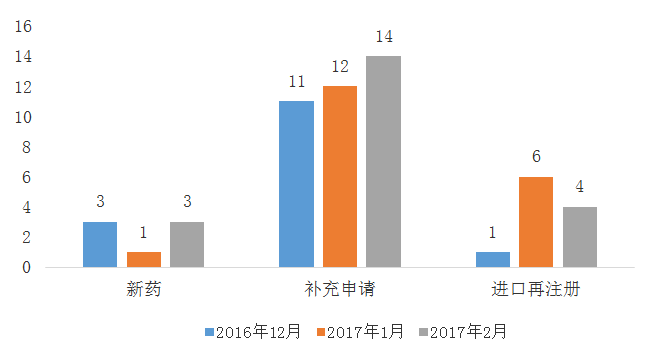
图三 2016年12月与2017年1月、2月CDE中药各申请类型受理情况
表六 2017年2月新承办的中药新药
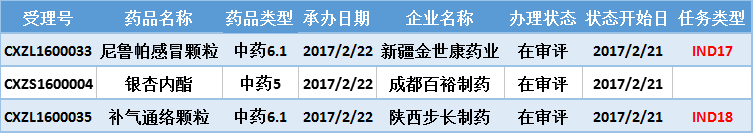
注:排队序号截止至2017年3月1日
从近日举办的国新办发布会上,国家食药监总局局长毕井泉表示对中药药品名称要立规矩:中成药通用名命名的技术守则。毕井泉介绍,为了解决这一问题,2014年国家食药监总局成立科技组,专门研究中药古代方剂命名的特点和规律,并起草了中成药命名的技术指导原则。可见国家对中成药的规范性越来越重视。
三、生物制品
2017年2月份CDE承办新的生物制品注册申请受理号共计50个,新药22个(涉及19个品种,19个厂家),补充申请16个(涉及12个品种,11个厂家),进口8个(涉及6个品种),进口再注册4个(涉及1个品种,1个厂家)。
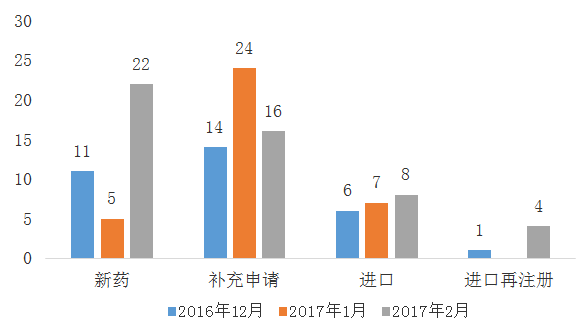
图四 2016年12月与2017年1月、2月CDE生物制品各申请类型受理情况
本月不管是申报的生物制品总数还是申报生物制品新药数较过去一年相比都是历史新高。去年受理的数量均值约为34个,新药约为9个。本月有3个1类预防用生物制品和7个1类治疗用生物制品获得承办,目前均已经进入相应序列排队待审。
表七 2017年2月新承办的生物制品1类新药
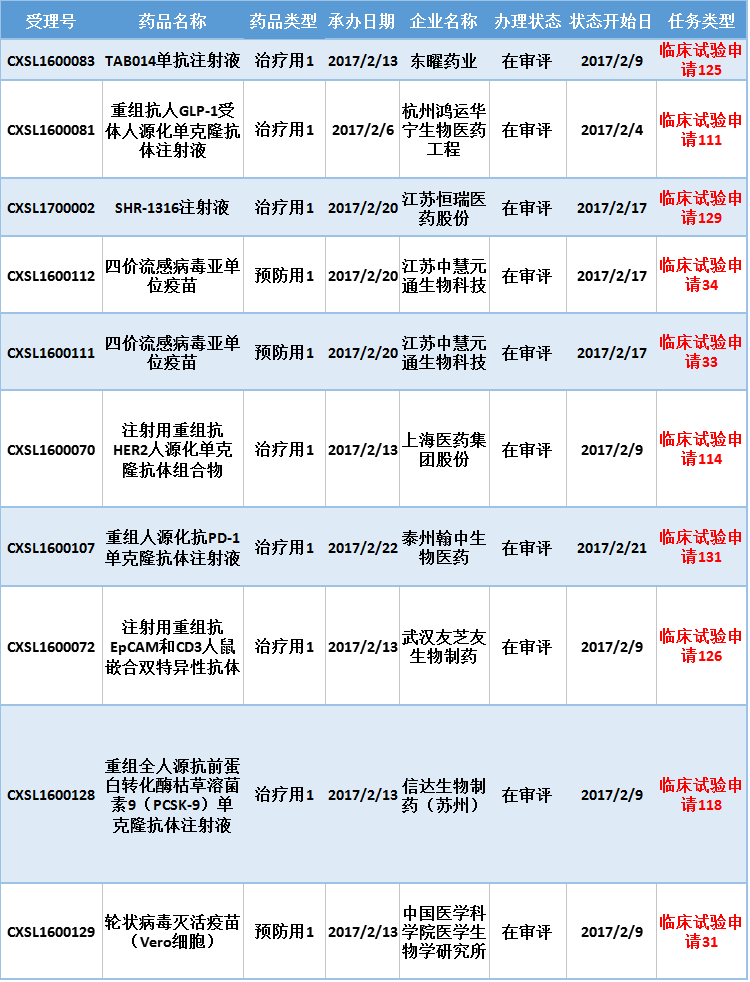
注:排队序号截止至2017年3月1日

数据来源:药智注册与受理数据库
原创申明:本文系药智网原创稿件,欢迎转载,转载请注明来源和作者,谢谢!





合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938


