深度盘点:江苏药品申报总量全国领先!18款1类创新药获批上市,恒瑞、豪森、百济…
看点:
2021江苏省受理总量为1762个(不计复审)。
2021江苏省9个1类化药创新药申报上市,11个1类化药创新药获批上市。
江苏康缘药业中药创新药银翘清热片获批上市。
随着2020年新《药品注册管理办法》的公布,药品审评体系和审评能力的现代化,2021年全国药品申报依旧呈上升趋势,截止2021年12月31日,CDE受理的受理号个数高达11569个,较2020年增加了12.19%;那作为医药大省江苏省2021年的药品申报又是怎样的情况呢?请看以下2021江苏省详细分析报告:
一、2021年江苏省CDE注册申请受理总体情况
1.各药品类型申报情况
根据药智注册与受理数据库最新统计,2021年CDE共承办江苏省新的药品注册申请以受理号计有1762个(以受理号计,下同)其中化药1361个,中药61个,生物制品335个,年度受理总量较2020年增加了187个,占全国的受理总量比重的15.2 %;2017-2021年江苏省药品注册申请受理情况详见图1。
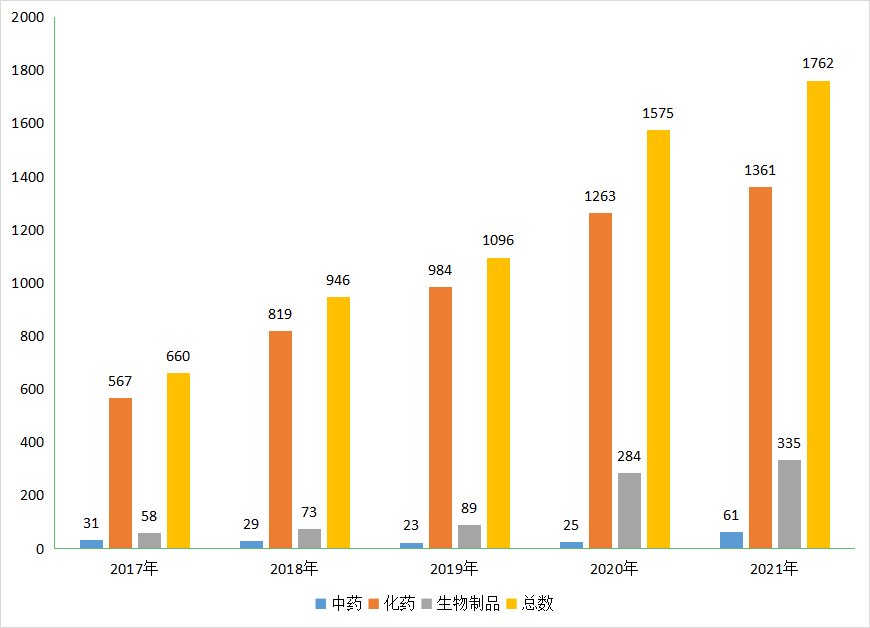
图1 2017-2021年江苏省药品受理情况
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
2.各类申报类型总体情况
2021年江苏省各类申报类型为:补充申请672 个,申请临床630个,申请上市417个,申请再注册26个。2021 年江苏省CDE药品各申请类型受理情况见图2。
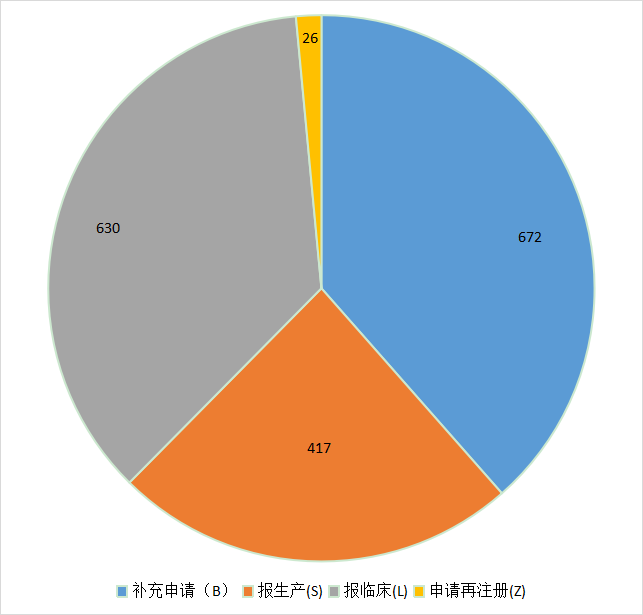
图 2 2021 年江苏省CDE药品各申请类型受理情况
数据来源:药智数据、药智咨询整理
注:统计规则:S、L、B、Z 分别是受理号第 4 位字母
3.国产1类创新药受理情况
2021年CDE受理江苏省国产创新药注册申请625个(以受理号计),其中临床申请465个,上市申请18个,补充申请142个。按药品类型统计,化学药441个,生物制品178个,中药6个;2021年江苏省国产创新药受理情况详见图3。
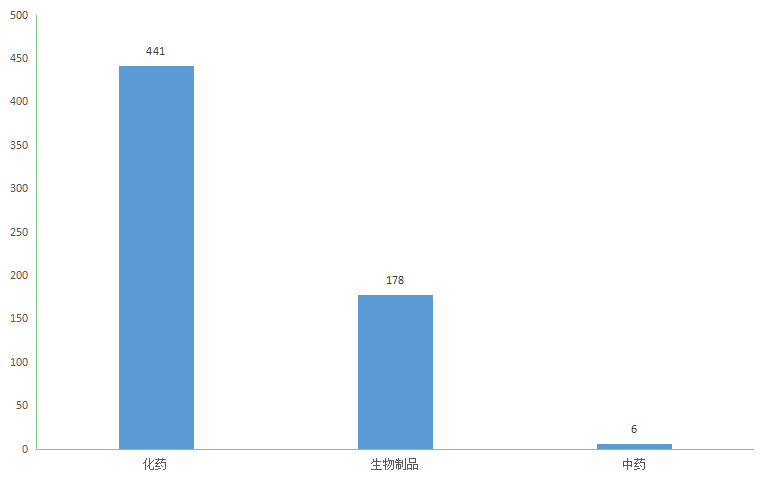
图3 2021年江苏省国产创新药受理情况
数据来源:药智数据、药智咨询整理
4.进口创新药及原研药受理情况
2021年CDE受理江苏省企业5.1类化学药进口原研药注册申请43个,受理1类化药进口创新药注册申请53个;1类治疗用生物制品15个。
5.2021年审评完结情况
根据药智注册与受理数据库最新统计,2021年(注:状态开始日期从2021年1月1日至2021年12月31日)江苏省审评完结受理号数量(指CDE完成技术审评并移交审批的受理号数量,办理状态包括在审批、待审批、审批完毕或制证完毕等状态,以受理号计)共计1766个,其中化药1420个,中药65个,生物制品281个;2021年江苏省CDE各药品类型审结情况详见图4。
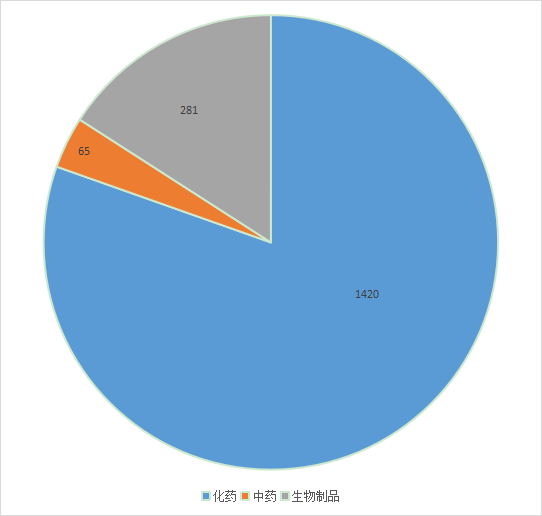
图 4 2021年江苏省CDE各药品类型审结情况
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
以下让我们详细分析一下化药、中药、生物制品的注册受理及审评情况。
二、化药
1.2021年化药申报情况
2021年共计受理化药1361个(以受理号计)其中化学药IND受理申请406个,较2020年增长了96%;受理化学药NDA申请 49个,较2020年增长了28.9%;受理仿制药上市申请(ANDA)315个,较2020年增长了17.5%;受理一致性评价补充申请119个。2021年江苏省化学药各类注册申请受理情况详见图5。2019-2021年江苏省化学药IND申请、NDA、ANDA和一致性评价注册申请受理情况详见图6。
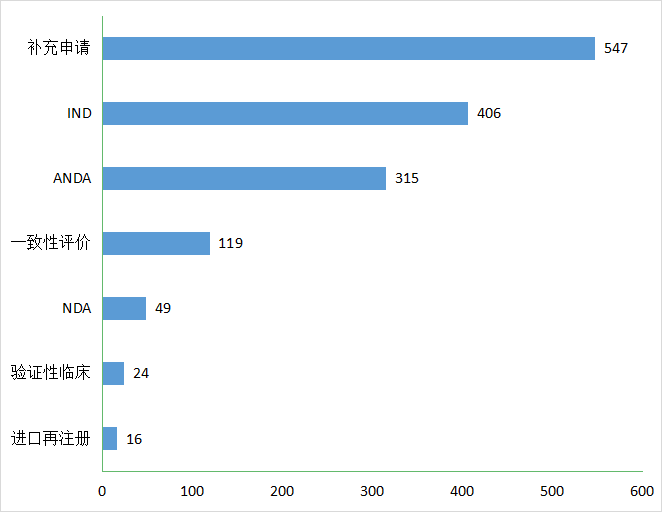
图 5 2021年江苏省化学药各类注册申请受理情况
数据来源:药智数据、药智咨询整理
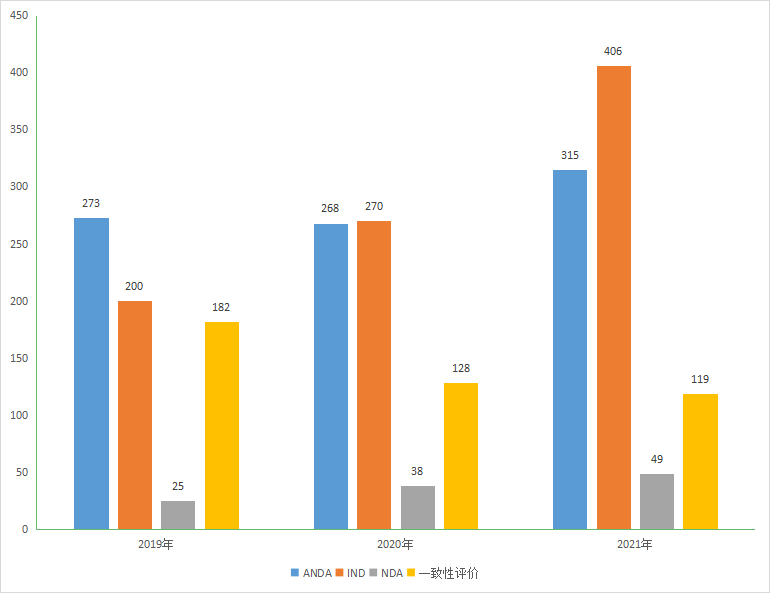
图6 2019-2021年江苏省化学药IND申请、NDA、ANDA和一致性评价注册申请受理情况
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
1.1 化药1 类创新药申报情况
按现行化药注册分类,化药1类定义为:境内外均未上市的创新药。指含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
2021年江苏化药1 类申报为441个(以受理号计),其中,IND受理申请317个,包括国产受理281个,进口受理 36个;国产IND受理中单品种受理最多的为南京艾美斐生物的IPG1094,拟用于实体瘤、银屑病、系统性红斑狼疮、多发性硬化症的治疗,目前均已批准临床;2021年江苏省国产化药1类IND单品种申报TOP5详见表1。
表1 2021年江苏省国产化药1类IND单品种申报TOP5
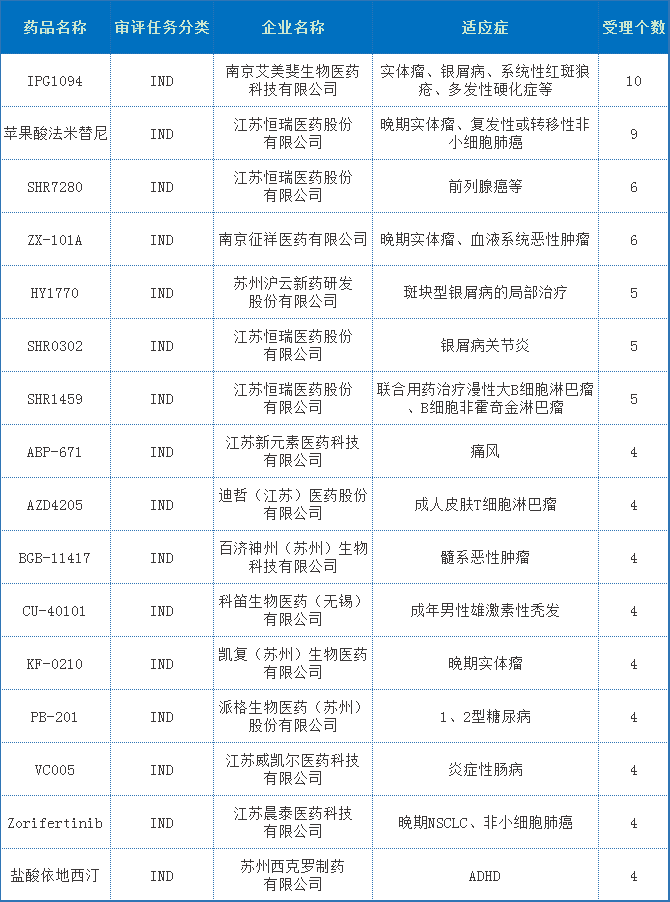
注:数据截止至2022年01月13日。
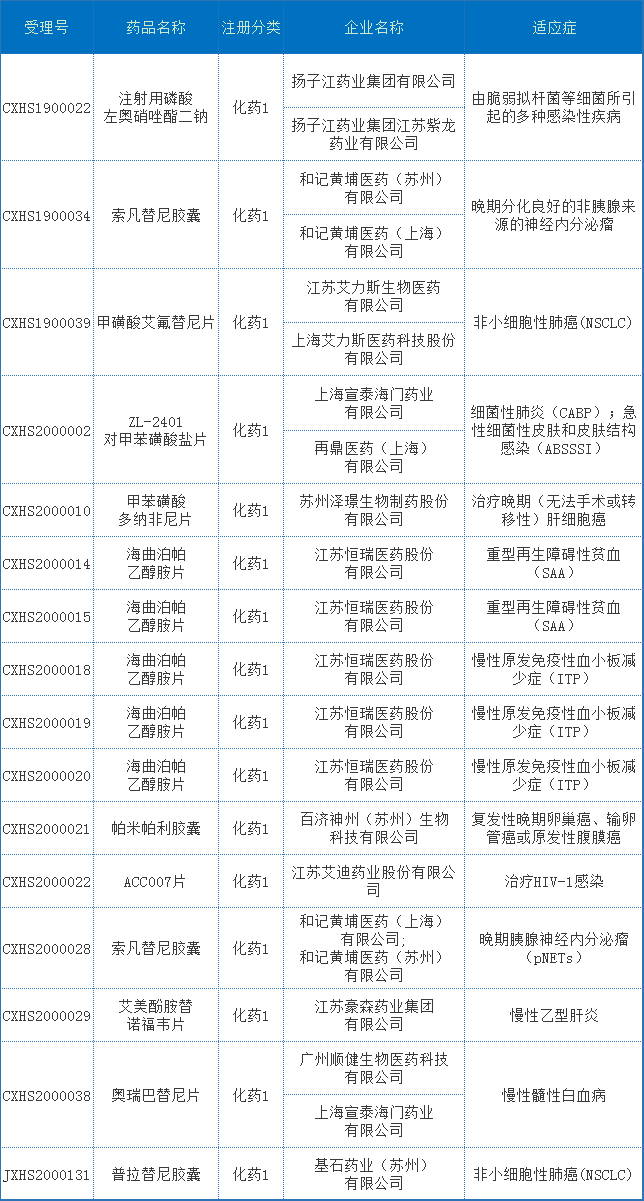
此外,化药1 类申报中NDA受理申请14个,共计9个品种,涉及11个企业;2021年江苏省化药1类NDA申报受理情况详见表2:
表2 2021年江苏省化药1类NDA申报受理情况

注:数据截止至2022年01月13日。
2.2021年化药审评完结情况
2021年江苏省审评完结1420个(以受理号计),其中IND申请382,全部默认批准临床;ANDA申请368个,审评结论为批准生产的246个;NDA申请54个,其中批准1类创新药16个,进口原研药11个。(如想了解具体情况,请关注药智注册受理数据库)。2021年江苏省批准1类化药新药获批上市情况详见表3。
表3 2021年江苏省1类化药新药获批上市情况
注:数据截止至2022年01月13日。
3.一致性评价申报审评情况
目前仿制药一致性评价工作已经进入了常态,2021年江苏省一致性评价受理号申报119个(以受理号计),涉及84个品种,50个企业,占2021年全国一致性评价受理总量的13.4%(如想了解具体情况,请关注药智注册受理数据库)。2021年江苏省企业一致性评价受理数量TOP 5详见图7。
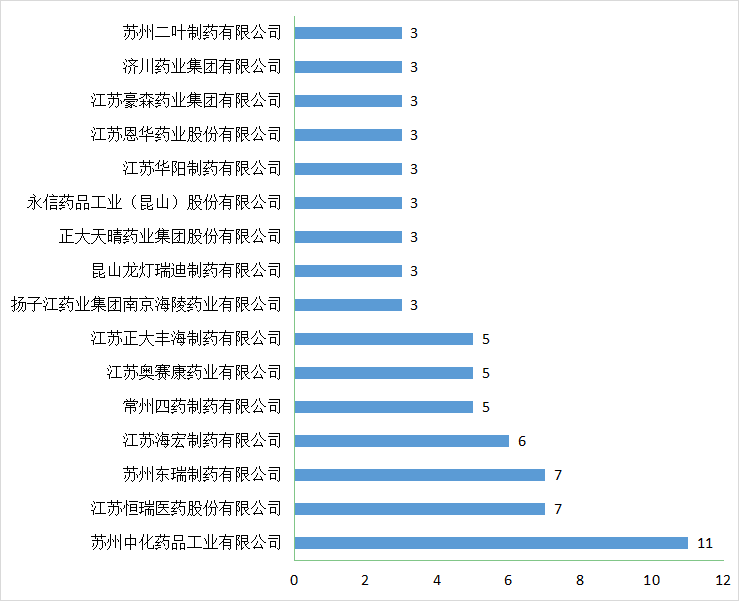
图7 2021年江苏省企业一致性评价受理数量TOP 5
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
2021年江苏省一致性评价完成审评的受理号175个,共涉及93个品种,51个企业,其中获得批准的受理号168个;本年度通过一致性评价最多的企业为正大天晴,通过19个受理号,其次是奥赛康、恒瑞医药通过17个受理号并列第二;2021年江苏省企业通过一致性评价数量TOP 5详见图8:
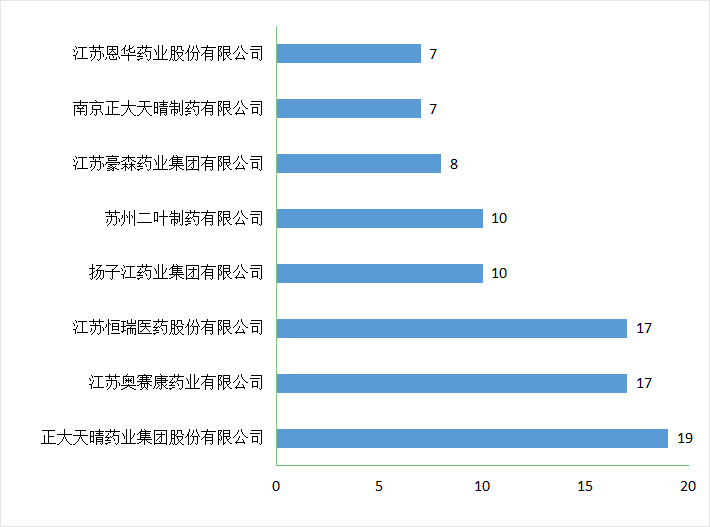
图8 2021年江苏省企业通过一致性评价数量
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
三、中药
1.2021年中药申报情况
2021年CDE承办的江苏省中药注册申请以受理号计共有61个,其中新药申请7个,均为IND申请,补充申请54个;2021年江苏省中药新药申报受理情况详见表4:
表4 2021年江苏省中药新药申报受理情况
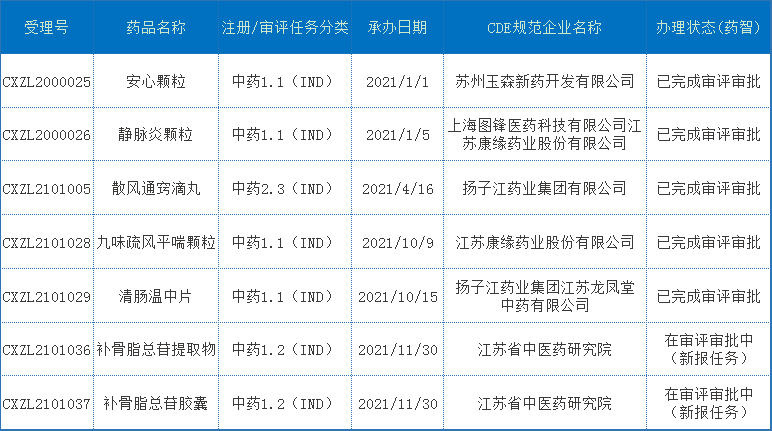
注:数据截止至2022年01月13日。
2.2021年中药审评完结情况
2021年江苏省审评完结65个(以受理号计)中药申请,其中IND申请5,全部默认批准临床;补充申请申请58个;NDA申请1个,为江苏康缘药业的银翘清热片获批上市。(如想了解具体情况,请关注药智注册受理数据库)
银翘清热片
银翘清热片是康缘药业在临床经验方基础上研制的中药创新药,临床试验结果显示可用于外感风热型普通感冒的治疗;该中药新药上市,为普通感冒患者提供了一种新的治疗选择。
四、生物制品
1.2021年生物制品申报情况
2021年江苏省共335个受理号获CDE受理,其中预防用生物制品9个,包括:6个新药临床试验申请,3个补充申请;治疗用生物制品313个,包括:临床试验申请186个,上市申请35个,补充申请81个,再注册申请11个。2021年江苏省生物制品申报受理情况详见图9:
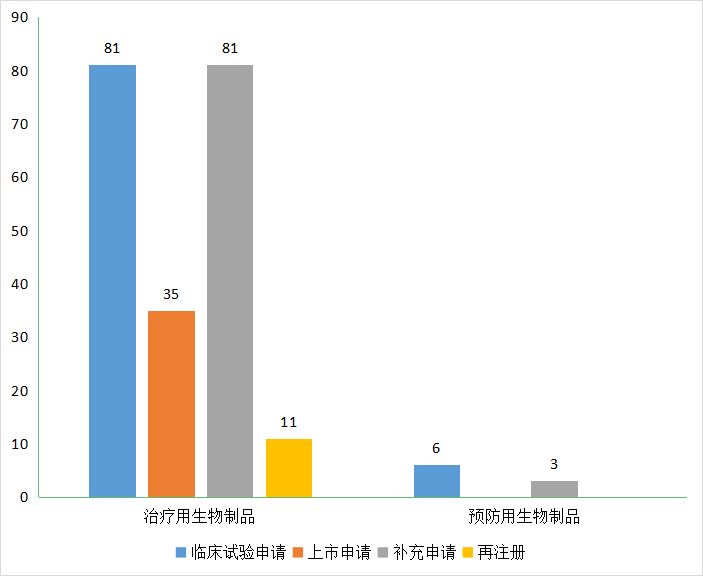
图9 2021年江苏省生物制品申报受理情况
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
2.2021年生物制品审评完结情况
2021年江苏省审评完结281个(以受理号计,下同)生物制品受理号,其中新药申请185个,进口13个,补充申请65个、进口再注册11个,一次性进口申请7个;在新药申请中,上市申请共25个;其中22个获批上市,多数为PD-1靶点治疗药物。(如想了解具体情况,请关注药智注册受理数据库)。2021年江苏省生物制品审评完结情况详见图10。2021年江苏省生物制品新药获批上市情况详见表5:
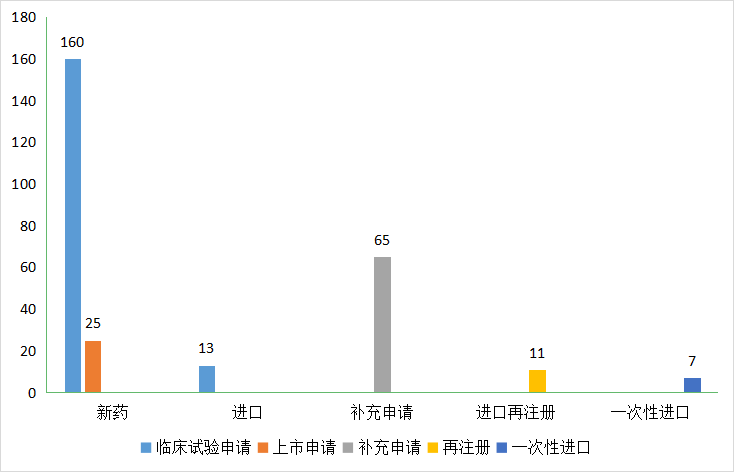
图10 2021年江苏省生物制品审评完结情况
数据来源:药智数据、药智咨询整理
注:数据截止至2022年01月13日。
表5 2021年江苏省生物制品新药获批上市情况
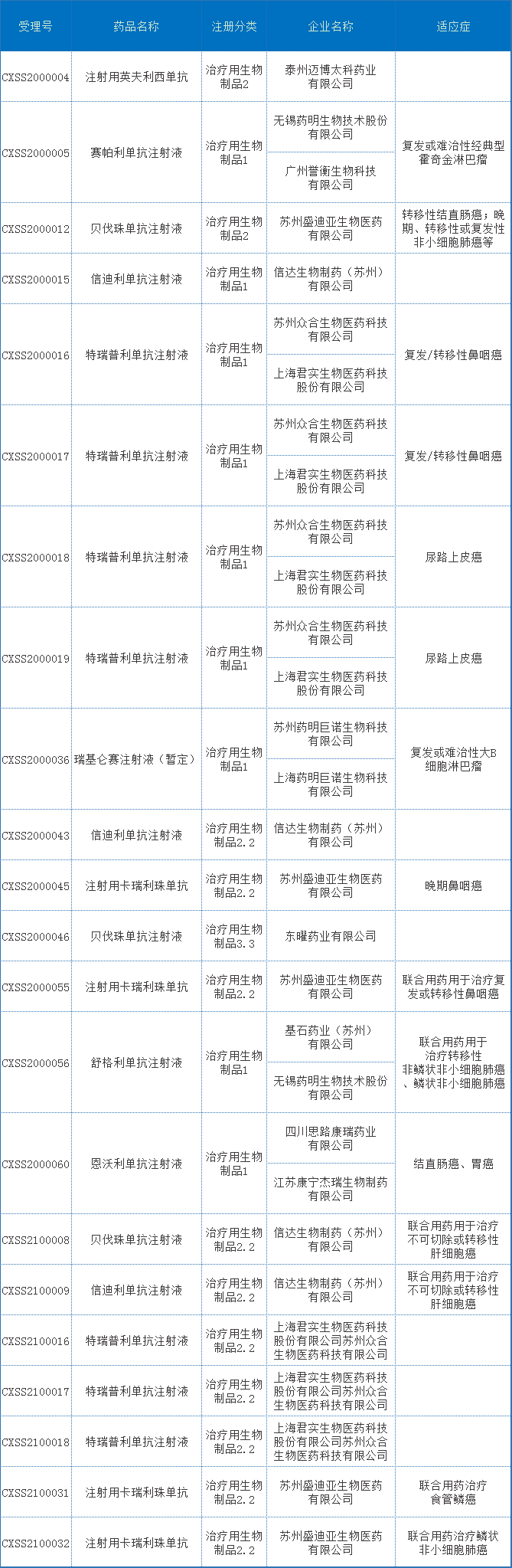
注:数据截止至2022年01月13日。
数据来源:药智药品注册与受理数据库

责任编辑:琉璃
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。




• 51款国产化药1类新药获受理!c-MET抑制剂再传佳音,人福药业、浦润奥、以岭…
• 31款国产化药1类新药获受理,多款PD-1申报新适应症!复宏汉霖、百济神州、罗氏…
• 37款国产化药1类新药获受理,恒瑞医药镇痛新药报产!京新药业、真实生物…
• 13款1类创新药获批上市!优先审评、突破性疗法数量大增,复宏汉霖、恒瑞、康方…
• 4款国产1类新药报上市!超20款改良型新药获受理,豪森药业、正大天晴、兴盟生物…
• 25款化药1类新药获受理!生物创新药申报放缓,京新药业、康缘药业、科伦…
• 32款化药1类新药获受理,2类改良型新药申报量大增!复星医药、百济神州、好医生…
• 53款国产1类新药申报临床,3款国产1类新药申报上市!亿一生物、四环制药、石药…
• 2021年1类新药申报临床数量再创新高!恒瑞位居第一,豪森、广东东阳光药…
• 深度盘点:江苏药品申报总量全国领先!18款1类创新药获批上市,恒瑞、豪森、百济…
合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938



