中国乳腺癌药物临床试验进展总览
乳腺癌(breastcarcinoma)是乳腺导管上皮及末梢导管上皮发生的恶性肿瘤。乳腺癌中99%发生在女性人群,男性仅占1%。据统计,欧美国家妇女乳腺癌占恶性肿瘤的第一位,我国占第二位。近年来有上升的趋势。笔者检索了药智中国临床试验数据库,对乳腺癌药物的临床试验情况进行了简单的汇总。以供参考。
据药智数据统计,截止2016年12月19日,共有229项试验记录,其中包括CFDA公布的药物临床试验登记记录85条(已删除重复项),中国临床试验注册中心登记的144条。本文以CFDA临床试验登记平台公布的数据为例,从以下几个方面对国内乳腺癌药物的临床试验情况进行分析:
该85条临床试验登记记录首次公示日期从2013年7月24日至2016年12月9日。
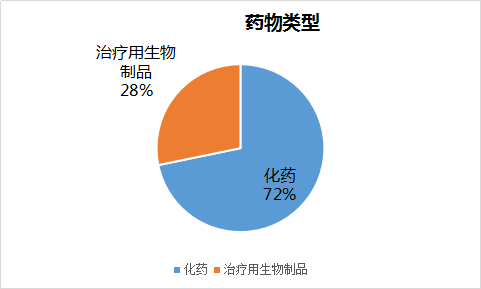
药物类型:
按药物类型角度分析,85项临床试验记录中包括两大类:化药61个,占比72%;治疗用生物制品24个,占比28%。
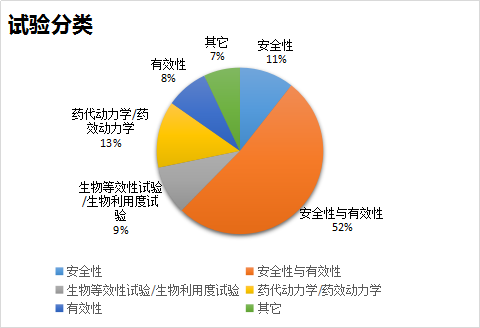
试验分类:
以登记的临床试验分类角度分析,安全性9个(11%);安全性与有效性44个(52%);生物等效性试验/生物利用度试验8个(9%);药代动力学/药效动力学11个(13%);有效性个7个(8%);其它6个(7%)。由以上数据可以看出,药物的安全性与有效性试验(占比71%)最受关注。
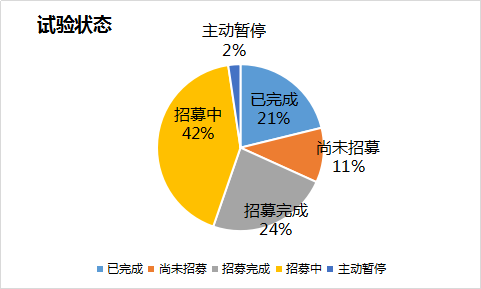
试验状态:
以试验状态角度分析,已完成的有18个(21%);尚未招募9个(11%);招募完成20个(24%);招募中36个(42%),主动暂停2个(2%)。尚未招募和招募中的临床试验占总数的一半(53%),感兴趣的伙伴可以多关注。
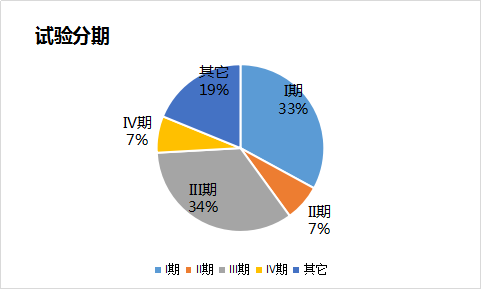
试验分期:
以试验分期角度分析:I期28个(33%);II期6个(7%);III期29个(34%);IV期6个(7%);其它16个(19%)。由以上数据可以看出,III期临床试验最多,其次是I期。
企业分析:
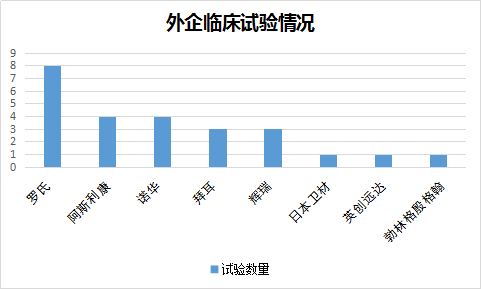
外企的临床试验共26个(占总数的31%)。从临床试验数目上,罗氏8个位列第一、诺华(4个)和阿斯利康(4个)并列第二、辉瑞(3个)与拜耳(3个)并列第三。其余企业分别如下:勃林格殷格翰1个,礼来1个,卫材1个,英创远达1个。
国内企业的临床试验共59个(占总数的69%),齐鲁制药(8个)位列第一,江苏恒瑞(6个)第二,泰格(4个)第三。其余企业的临床试验登记记录数量均在1-3个之间。
比较受关注的公司及药物有:
罗氏:帕妥珠单抗注射剂、注射用Trastuzumab-MCC-DM1、贝伐珠单抗注射液;
诺华:RAD001、BKM120、GW572016片;
阿斯利康:Olaparib、氟维司群注射液;
辉瑞:Palbociclib胶囊、依西美坦片;
拜耳:索拉非尼(多吉美,BAY43-9006)、氯化镭[223Ra]注射液;
齐鲁制药:注射用重组抗HER2人源化单克隆抗体、甲苯磺酸赛拉替尼片;
江苏恒瑞:注射用紫杉醇(白蛋白结合型)、马来酸吡咯替尼片;
泰格:帕妥珠单抗注射液、注射用酒石酸长春氟宁浓溶液
………………
注:本文系药智网作者原创稿件,欢迎转载,转载时请注明出处,谢谢!




合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938



