国产占比超七成!中国医疗器械审评分析
2024年,中国医疗器械审评环境持续优化,审评效率与透明度进一步提升。全年国家药监局共完成21486项医疗器械申请,涵盖新注册、变更与延续注册等多种类型。其中,国产医疗器械表现突出,在新注册产品中占比高达77%,本土创新能力在政策支持及械企加强研发投入等背景下迎来显著增强。
本报告节选自《中国医疗器械研发蓝皮书(2025)》第四章——2024年中国医疗器械审评情况分析报告,从审批情况、国产及进口产品分布、未获批产品品类等方向多维度切入,深入解析2024年中国医疗器械审评情况,为行业参与者提供决策参考。

图片来源:《中国医疗器械研发蓝皮书(2025)》
2024年中国医疗器械注册审评情况分析
国家药监局总体审批完成情况
2024年国家药监局公示的批件发布数量显示,一共完结了21486件器械申请的事项。其中,新注册产品申请3783件,变更许可事项5089件,变更登记事项6872件,延续注册4717件。
在新注册产品中,国产产品2918件,占比为77%;进口产品865件,占比为23%。在延续注册产品中,国产产品1966件,占比为42%;进口产品2751件,占比为58%。在变更许可事项中,国产产品2274件,占比为45%;进口产品2815件,占比为55%。在变更登记事项中,国产产品4974件,占比为72%;进口产品1898件,占比为28%。
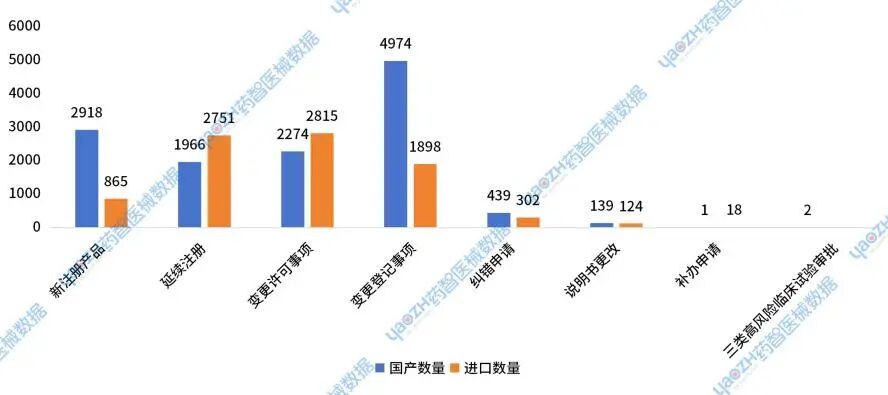
图1 2024国家药监局器械审批批件发布情况
数据来源:药智医械数据
2024年国家局器械批件分布情况
2024年国家药监局器械新注册产品获批数量为3398件,占比90%;终止注册237件,占比6%;不予注册148件,占比4%。
2024年国家药监局器械变更许可事项获批数量为4916件,占比97%;终止注册115件,占比2%;不予注册58件,占比1%。
2024年国家药监局器械延续注册获批数量为4673件,占比99.1%;终止注册40件,占比0.8%;不予注册4件,占比0.1%。
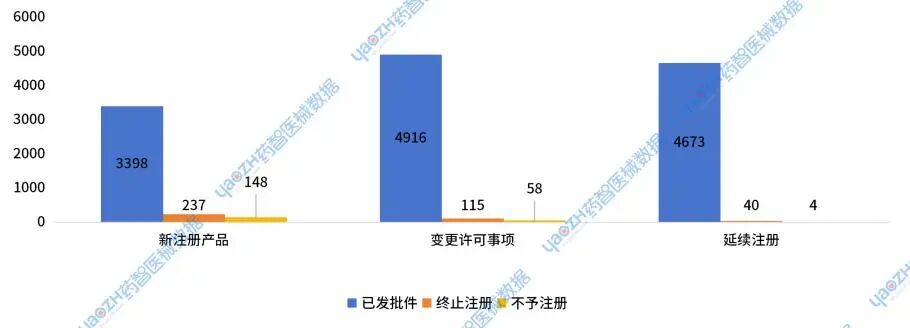
图2 2024年国家药监局器械审批主要审批项批件分布情况
数据来源:药智医械数据
2024年国产Ⅲ类器械新注册产品审批完结情况
2024年国产Ⅲ类器械新注册产品审批完结数量2918件,其中江苏、广东、北京、上海和浙江的数量较多。
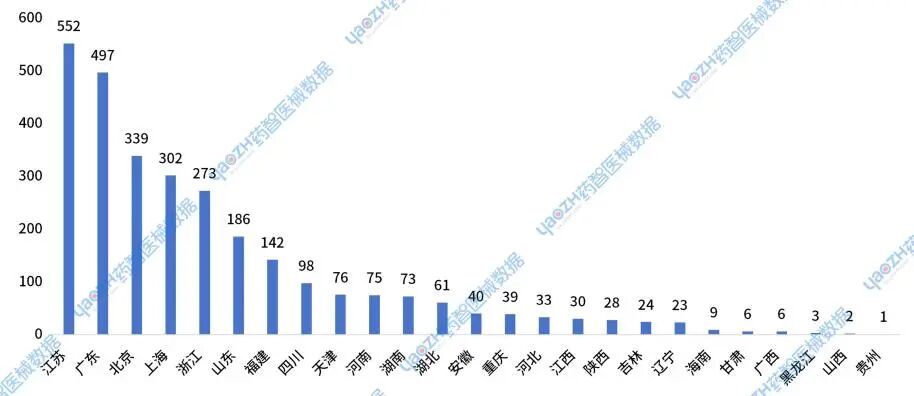
图3 2024年国产Ⅲ类器械新注册审批完结情况
数据来源:药智医械数据
2024年进口器械新注册产品国家或地区分布
2024年,新注册器械中进口产品的主要来源国家或地区为美国、德国、日本和韩国。

图4 2024年进口器械新注册产品国家或地区分布
数据来源:药智医械数据
2024年进口器械新注册获批产品管理类别国家或地区分布
2024年,共有723件进口新注册器械获批。其中,Ⅱ类器械获批320件,占比44%;Ⅲ类器械获批403件,占比56%。

图5 2024年进口器械新注册获批产品管理类别国家或地区分布
数据来源:药智医械数据
2024年国产新注册Ⅲ类器械获批情况
2024年获批的国产Ⅲ类器械主要集中在体外诊断试剂,无源植入器械,神经和心血管手术器械以及有源手术器械这四大类别中。其中体外诊断试剂获批487件,占比18%;无源植入器械获批486件,占比18%;神经和心血管手术器械获批294件,占比11%;有源手术器械获批287件,占比11%。
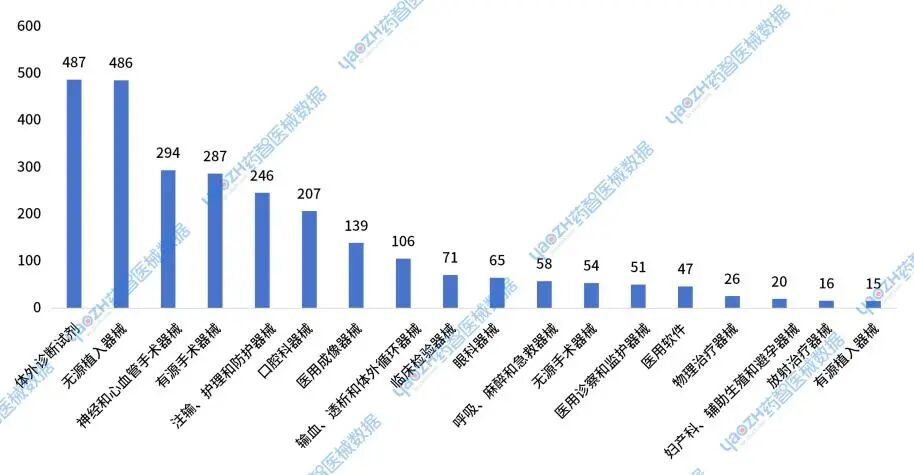
图6 2024年国产新注册Ⅲ类器械获批情况
数据来源:药智医械数据
2024年进口新注册Ⅲ类器械获批情况
2024年获批的进口Ⅲ类器械主要集中在无源植入器械,有源手术器械,口腔科器械和眼科器械等产品类别。其中无源植入器械获批78件,占比19%;有源手术器械获批50件,占比12%;口腔科器械获批46件,占比11%;眼科器械获批36件,占比9%。
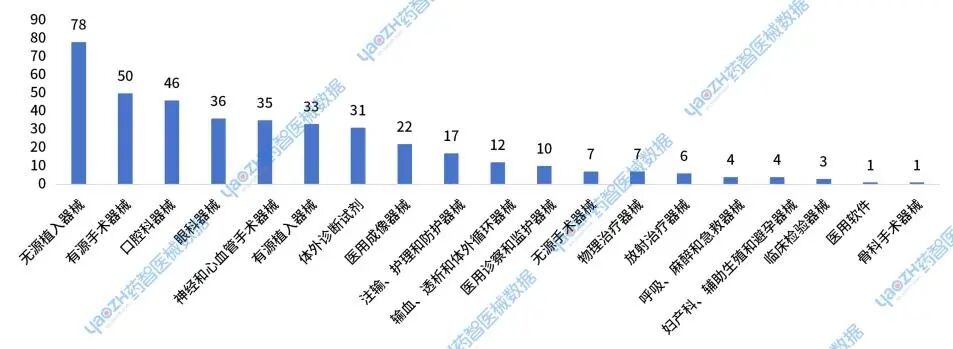
图7 2024年进口新注册Ⅲ类器械获批情况
数据来源:药智医械数据
2024年进口新注册Ⅱ类器械获批情况
2024年获批的进口Ⅱ类器械主要集中在体外诊断试剂,口腔科器械,医用诊察和监护器械,以及临床检验器械等产品类别。其中体外诊断试剂获批80件,占比35%;口腔科器械获批29件,占比9%;医用诊察和监护器械获批28件,占比9%;临床检验器械获批26件,占比8%。
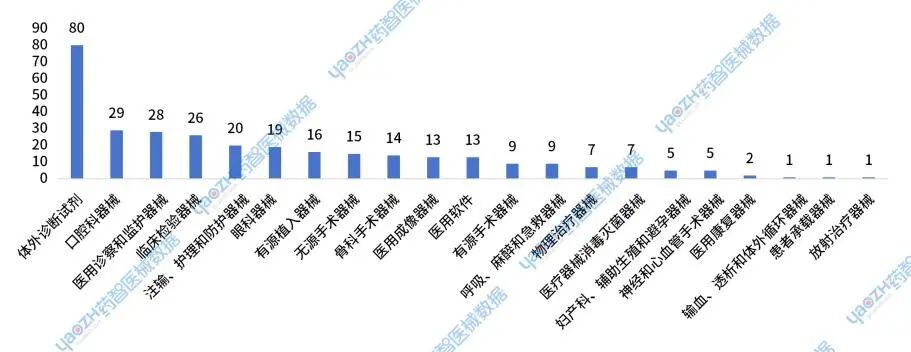
图8 2024年进口新注册Ⅱ类器械获批情况
数据来源:药智医械数据
2024年新注册产品未获批情况
2024年新注册器械产品未通过率较高的分类主要集中在患者承载器械,物理治疗器械,妇产科、辅助生殖和避孕器械,体外诊断试剂这四大类别中。在上述四类产品类别的新注册情况中,患者承载器械未获批1件,未获批率为50%;物理治理器械未获批13件,未获批率为25%;妇产科、辅助生殖和避孕器械未获批8件,未获批率为22%;体外诊断试剂未获批111件,未获批率为16%。
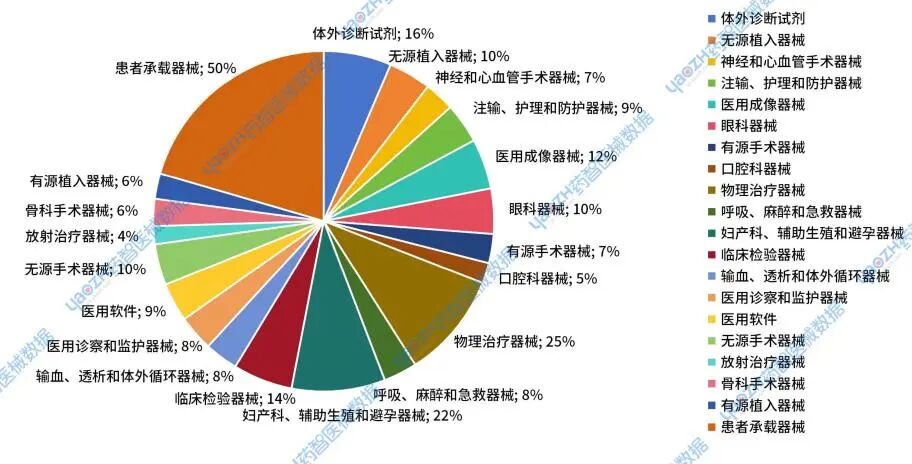
图9 不同类型新注册产品未获批比例
数据来源:药智医械数据
2024年中国医用耗材注册审评情况分析
耗材审批完结情况
2024年国家药监局公示的批件发布数量显示,共有12167件医疗器械耗材申请事项完结。其中新注册产品申请2281件,变更许可事项2790件,变更登记事项3932件,延续注册2551件。
在新注册产品中,国产产品1781件,占比为78%;进口产品500件,占比为22%。在延续注册产品中,国产产品1165件,占比为46%;进口产品1386件,占比为54%。
在变更许可事项中,国产产品1393件,占比为50%;进口产品1397件,占比为50%。在变更登记事项中,国产产品2758件,占比为70%;进口产品1174件,占比为30%。
Ⅲ类国产高值耗材的新注册产品数量是其延续注册数量的一倍左右,同时也高于进口高值耗材的新注册产品数量,表明国产Ⅲ类高值耗材的新品开发仍然处于上升趋势。
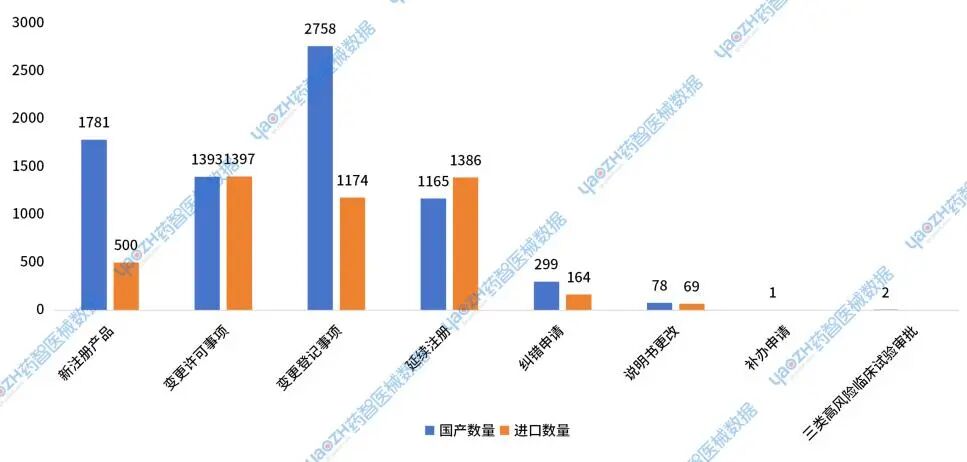
图10 2024年国家药监局医用耗材批件发布统计
数据来源:药智医械数据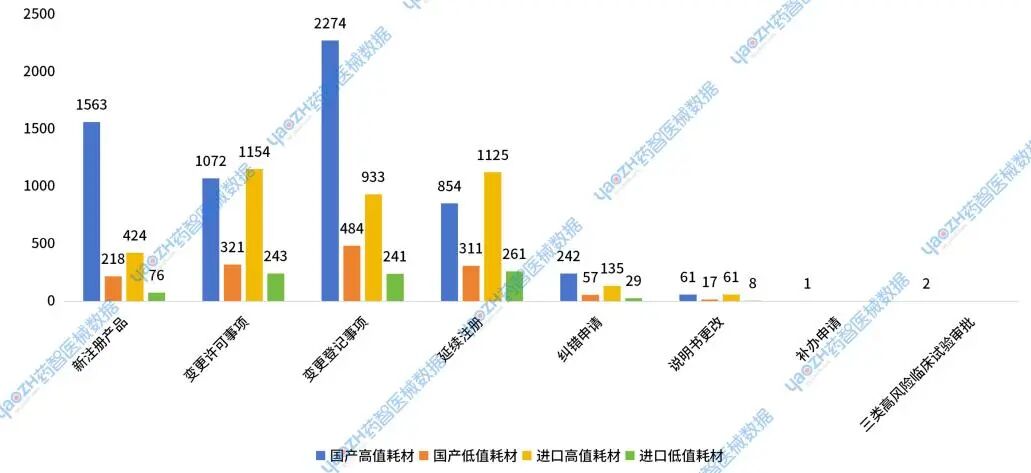
图11 2024年国家药监局不同类型医用耗材批件统计
数据来源:药智医械数据
2024年国家局医用耗材批件分布情况
2024年国家药监局医用耗材新注册产品获批数量为2087件,占比91%;终止注册114件,占比5%;不予注册80件,占比4%。
2024年国家药监局器械耗材变更许可事项获批数量为2687件,占比96%;终止注册64件,占比2%;不予注册39件,占比1%。
2024年国家药监局器械耗材延续注册获批数量为2525件,占比99%;终止注册24件,占比0.9%;不予注册2件,占比0.1%。
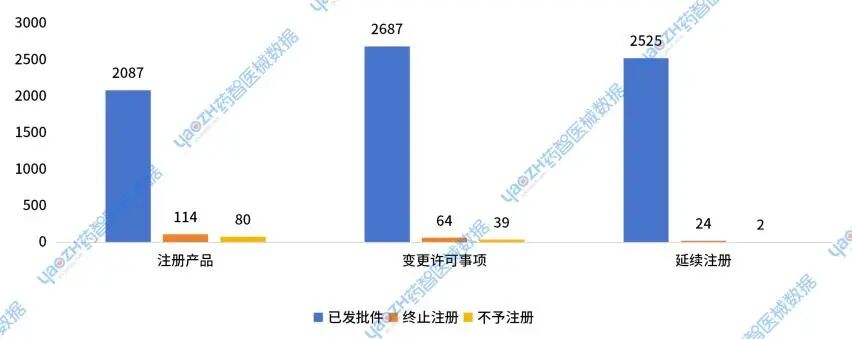
图12 2024年国家局医用耗材批件分布情况
数据来源:药智医械数据
2024年国产Ⅲ类医用耗材新注册产品审批完结省市情况
2024年国产Ⅲ类医用耗材新注册产品审批完结数量1781件,其中江苏、广东、北京、浙江和上海的完结产品数量较多。
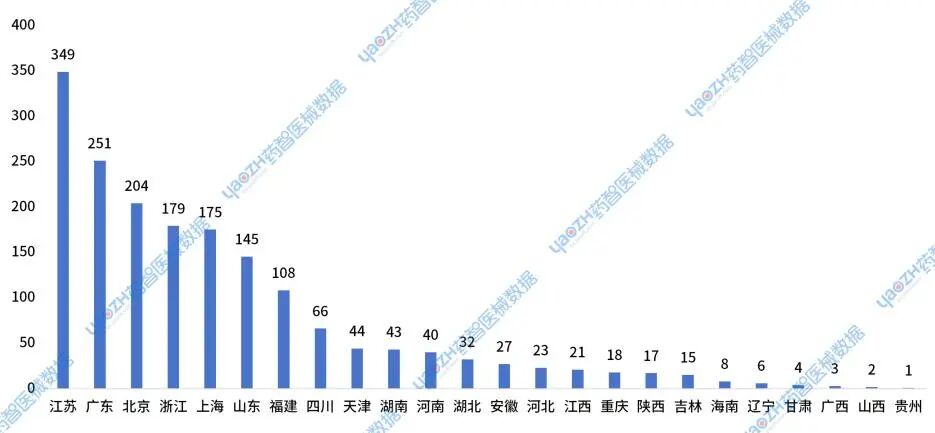
图13 2024年国产Ⅲ类医用耗材新注册产品审批完结省市分析
数据来源:药智医械数据
2024年进口医用耗材新注册产品国家或地区分布
2024年,进口的新注册医用耗材主要来源于美国、德国、韩国和日本等国家或地区。
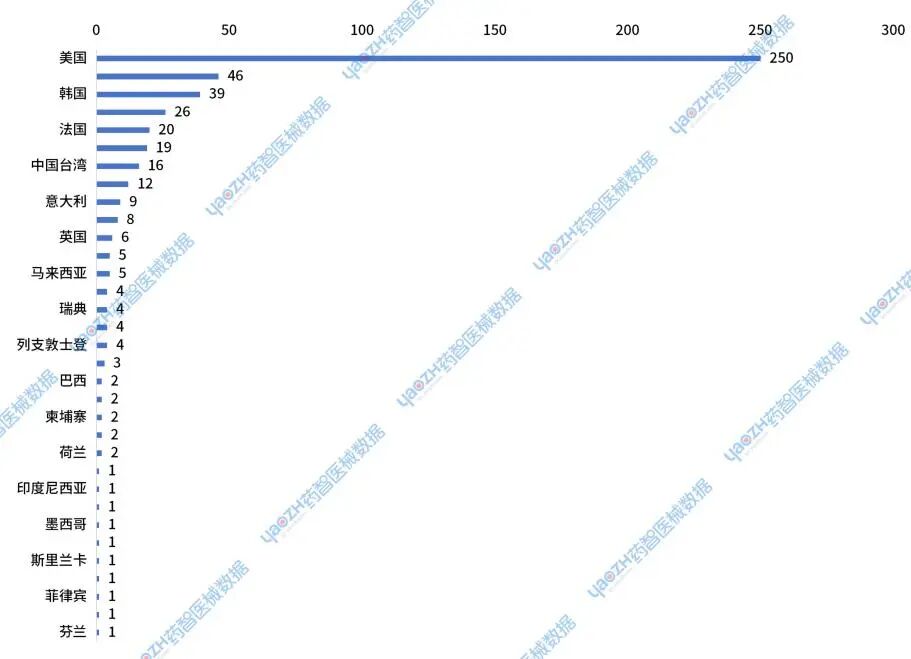
图14 2024年进口医用耗材新注册产品国家或地区分布
数据来源:药智医械数据
2024年进口耗材新注册获批管理类别分布
2024年进口新注册耗材一共获批425件,其中Ⅱ类耗材获批数为134件,占比32%,Ⅲ类耗材获批数为291件,占比68%。
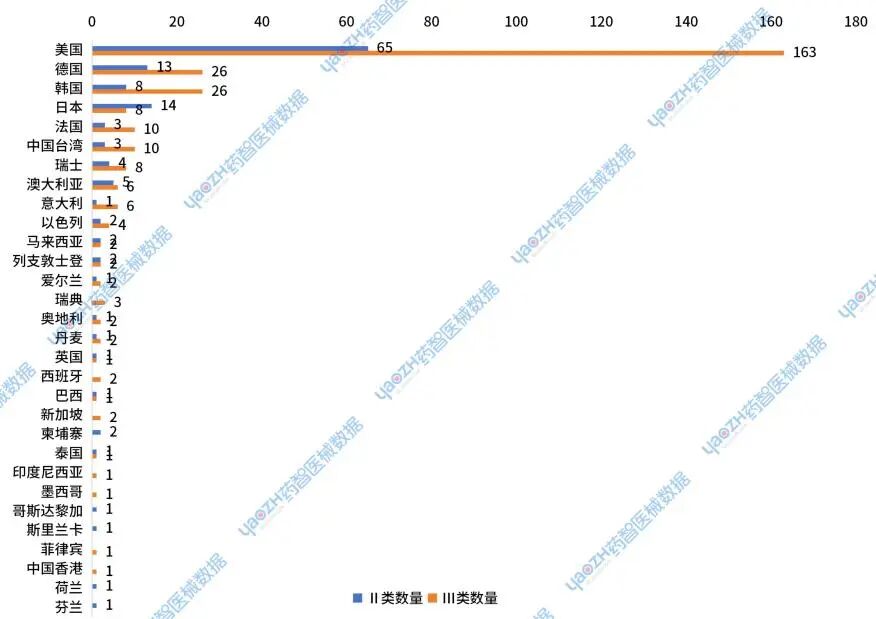
图15 2024年进口耗材新注册获批管理类别分布
数据来源:药智医械数据
2024年国产耗材新注册Ⅲ器械获批分布
2024年获批的国产新注册耗材中,Ⅲ类产品主要集中在无源植入器械,神经和心血管手术器械,注输、护理和防护器械,口腔科器械这四大类别中。其中无源植入器械获批486件,占比29%;神经和心血管手术器械获批294件,占比18%;注输、护理和防护器械获批242件,占比15%;口腔科器械207件,占比12%。
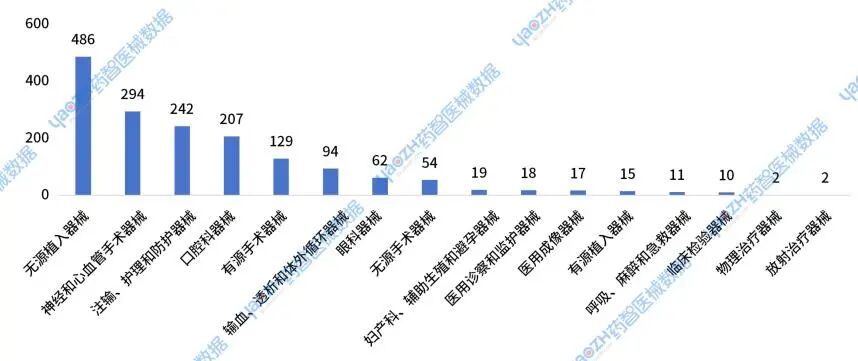
图16 2024年国产耗材新注册Ⅲ器械获批分布
数据来源:药智医械数据
2024年进口耗材新注册Ⅲ类器械获批情况
2024年获批的进口新注册耗材中,Ⅲ类产品主要集中在无源植入器械,口腔科器械,神经和心血管手术器械,有源植入器械这四大类别中。其中无源植入器械获批78件,占比27%;口腔科获批46件,占比16%;神经和心血管手术器械获批35件,占比12%;有源植入器械获批33件,占比11%。
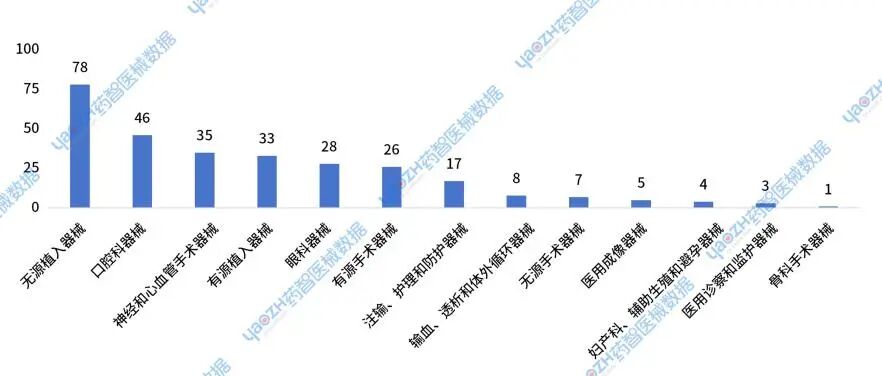
图17 2024年进口耗材新注册Ⅲ类器械获批分布
数据来源:药智医械数据
2024年进口耗材新注册Ⅱ类器械获批分布
2024年获批的进口新注册耗材中,Ⅱ类产品主要集中在口腔科器械,注输、护理和防护器械,无源手术器械,医用诊察和监护器械这四大类别中。其中口腔科器械获批24件,占比18%;注输、护理和防护器械获批19件,占比14%;无源手术器械获批15件,占比11%;医用诊察和监护器械获批14件,占比11%。
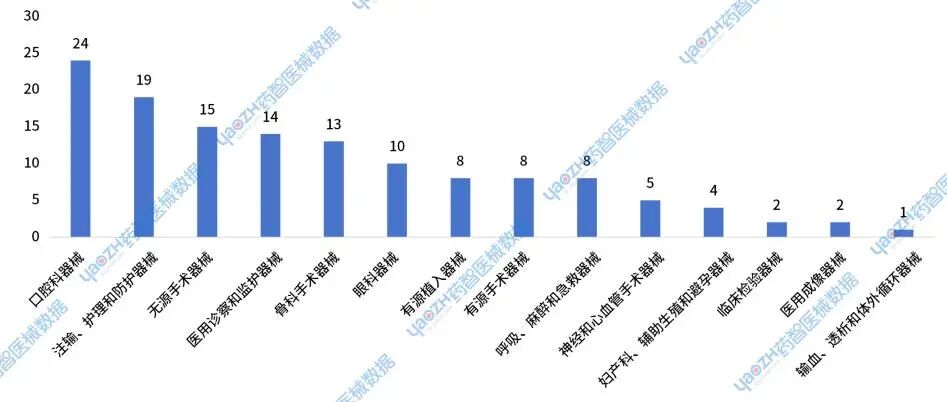
图18 2024年进口耗材新注册Ⅱ类器械获批分布
数据来源:药智医械数据
2024年国家局医用耗材未获批产品分布
2024年新注册医用耗材总审批数量在100件以上的类别中,未通过率较高的有眼科器械,无源植入器械,注输、护理和防护器械,有源手术器械。其中眼科器械未获批12件,未获批率为10.7%;无源植入器械未获批62件,未获批率为9.9%;注输、护理和防护器械未获批29件,未获批率为9.4%;有源手术器械未获批15件,未获批率为8.4%。
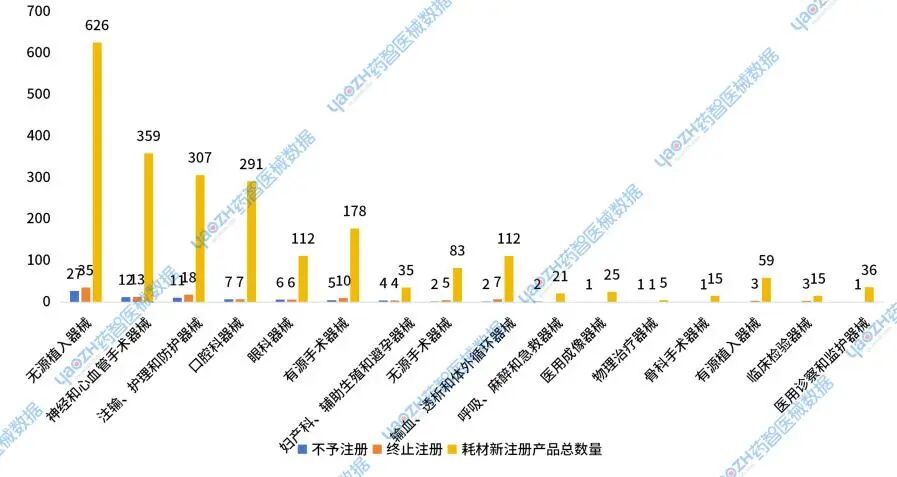
图19 2024年国家药监局新注册医用耗材未获批产品分布
数据来源:药智医械数据
2024年中国医疗设备注册审评情况分析
2024年国家药监局医疗设备批件发布情况
2024年国家药监局公示的批件发布数量显示,共完结3387件医疗设备申请事项。其中新注册产品申请639件,变更许可事项1004件,变更登记事项1193件,延续注册321件。
在新注册产品中,国产产品456件,占比为71%;进口产品183件,占比为29%。在延续注册产品中,国产产品121件,占比为38%;进口产品200件,占比为62%。在变更许可事项中,国产产品364件,占比为36%;进口产品640件,占比为64%。在变更登记事项中,国产产品776件,占比为65%;进口产品417件,占比为35%。
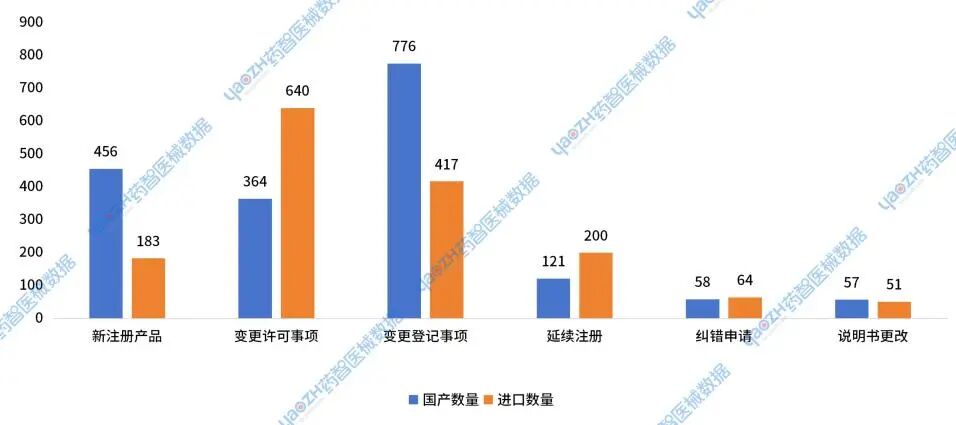
图20 2024年国家药监局医疗设备批件发布数据分布
数据来源:药智医械数据
2024年国家局医疗设备批件分布情况
2024年国家药监局医疗设备新注册产品获批数量为576件,占比90%;终止注册38件,占比6%;不予注册25件,占比4%。
2024年国家药监医疗设备变更许可事项获批数量为962件,占比95.8%;终止注册28件,占比2.8%;不予注册14件,占比1.4%。
2024年国家药监局医疗设备延续注册获批数量为318件,占比99.1%;终止注册2件,占比0.6%;不予注册1件,占比0.3%。
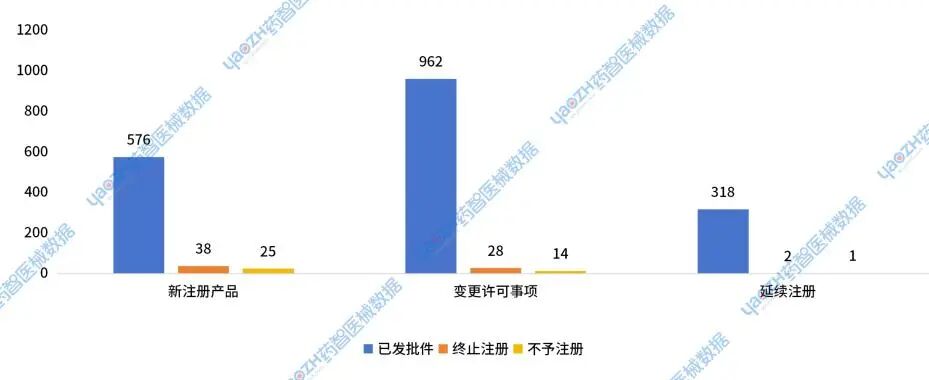
图21 2024年国家局医疗器械设备批件分布情况
数据来源:药智医械数据
2024年国产Ⅲ类医疗设备新注册产品审批完结省市分布
2024年,国产Ⅲ类医疗设备新注册产品审批完结数量453件,其中数量较多的省市为广东、江苏、上海、北京和浙江.
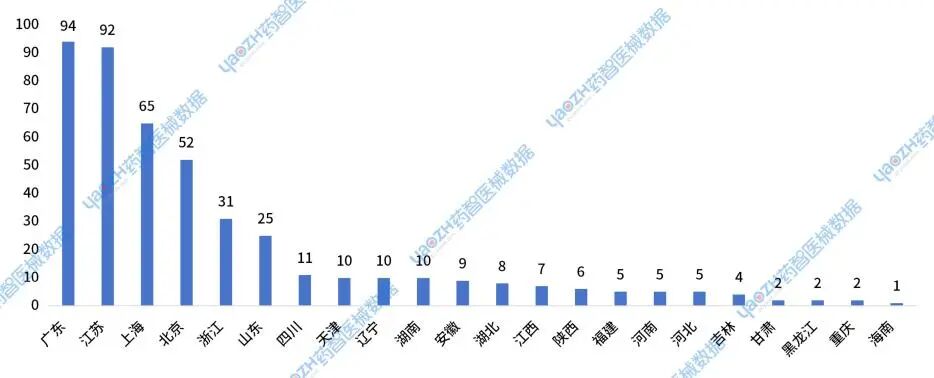
图22 2024年国产Ⅲ类医疗设备新注册产品审批完结省市分析
数据来源:药智医械数据
2024年进口医疗设备新注册产品国家或地区分布
2024年,进口的新注册医疗设备主要来源于美国、德国、日本和以色列等国家或地区。
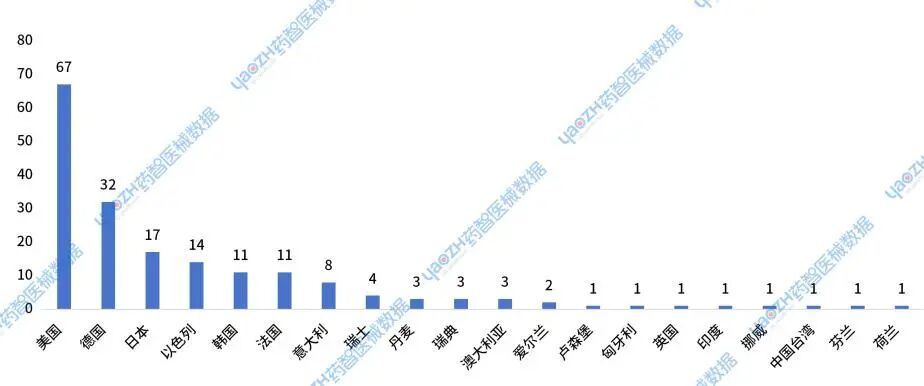
图23 2024年进口医疗设备新注册产品国家或地区分布
数据来源:药智医械数据
2024年进口医疗设备新注册获批管理类别分布
2024年,共147件进口新注册医疗设备获批,其中Ⅱ类器械获批70件,占比48%,Ⅲ类器械获批77件,占比52%。
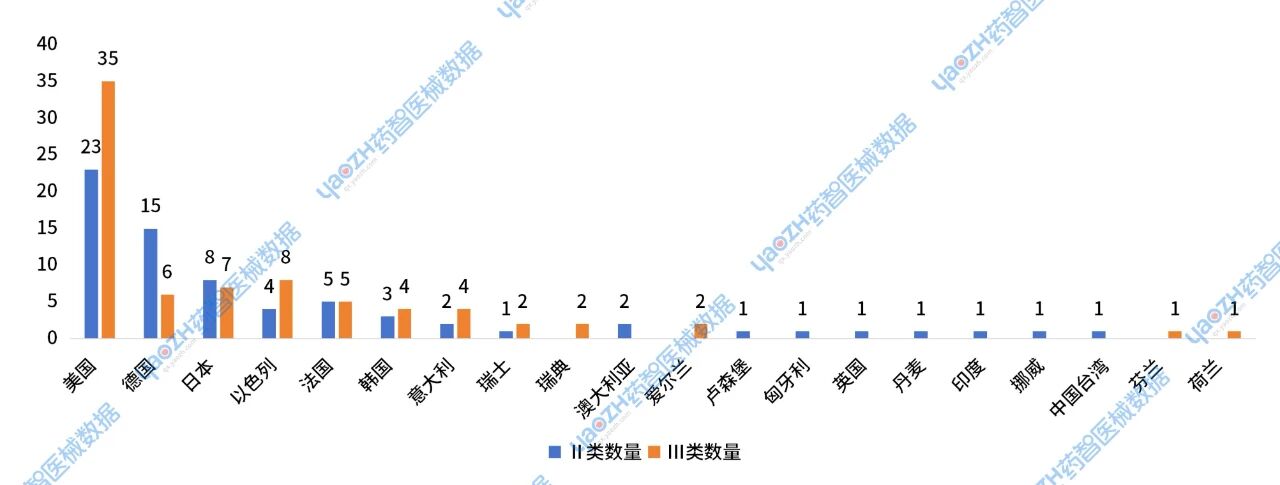
图24 2024年进口医疗设备新注册获批管理类别国家或地区分布
数据来源:药智医械数据
2024年国产医疗设备新注册Ⅲ类器械获批情况
2024年获批的国产Ⅲ类医疗设备主要集中在医用成像器械,呼吸、麻醉和急救器械,医用诊察和监护器械这四大类别中。其中有源手术器械获批158件,占比37%;医用成像器械获批122件,占比28%;呼吸、麻醉和急救器械获批47件,占比11%;医用诊察和监护器械获批33件,占比8%。
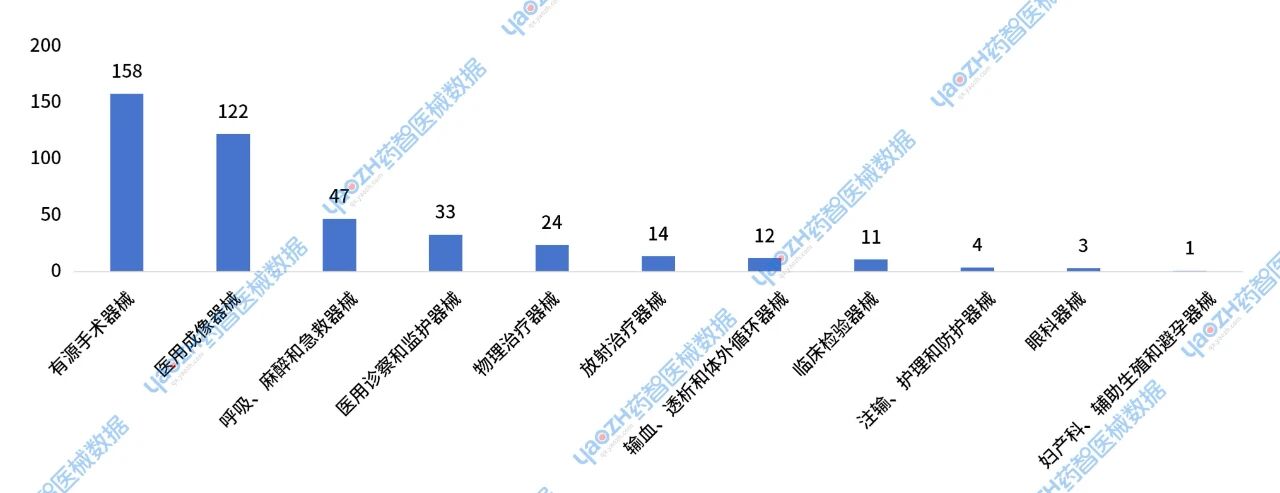
图25 2024年国产医疗设备新注册Ⅲ类器械获批分布
数据来源:药智医械数据
2024年进口医疗设备新注册Ⅲ类器械获批情况
2024年获批的进口Ⅲ类医疗设备主要集中在有源手术器械,医用成像器械,眼科器械等类别中。其中有源手术器械获批24件,占比34%;医用成像器械17件,占比24%;眼科器械获批8件,占比11%。
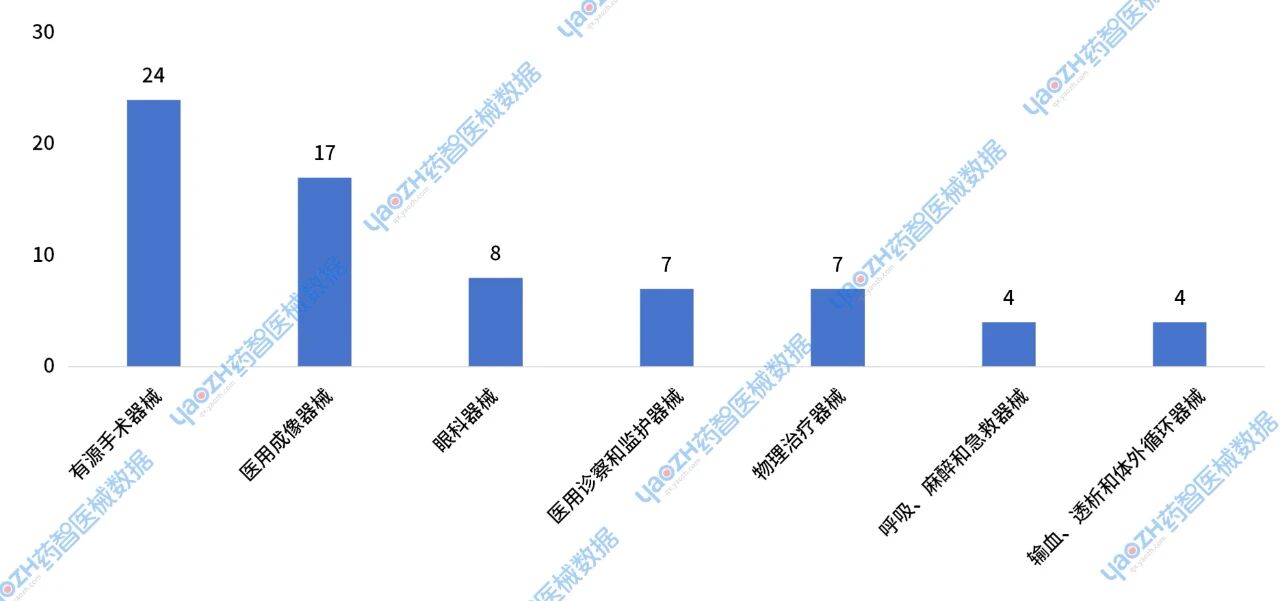
图26 2024年进口医疗设备新注册Ⅲ类器械获批情况
数据来源:药智医械数据
2024年进口医疗设备新注册Ⅱ类器械获批情况
2024年获批的进口Ⅱ类医疗设备主要集中在医用诊察和监护器械,医用成像器械和眼科器械等类别中。其中医用诊察和监护器械获批14件,占比24%;医用成像器械获批11件,占比19%;眼科器械获批9件,占比15%。
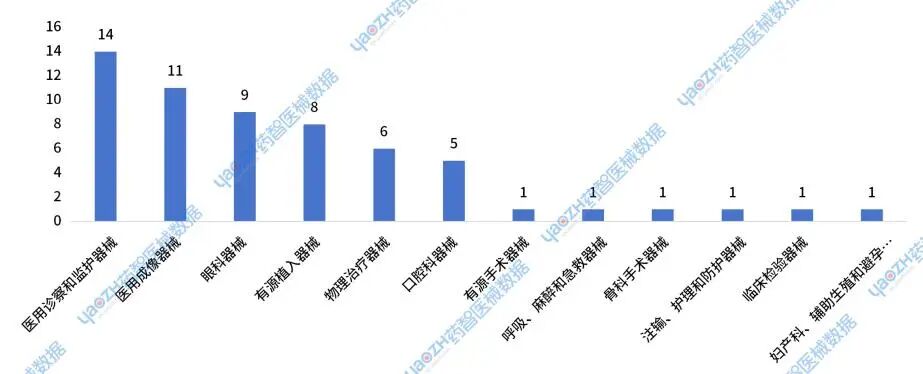
图27 2024年进口医疗设备新注册Ⅱ类器械获批情况
数据来源:药智医械数据
2024年国家药监局新注册医疗设备未获批产品分布
2024年新注册医疗设备总审批数量在50件以上的类别中,11件物理治疗器械未获批,未获批率为23%;22件医用成像器械未获批,未获批率为13%;7件医用诊察和监护器械未获批,未获批率为11%;10件有源手术器械未获批,未获批率为5%。
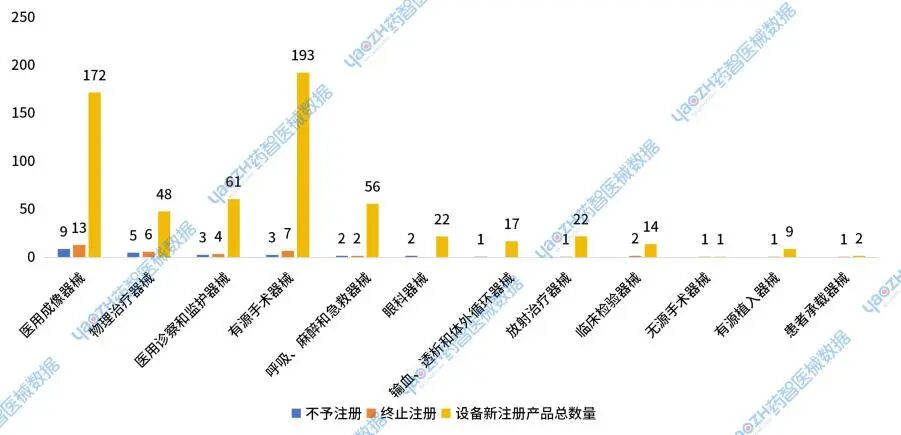
图28 2024年国家药监局新注册医疗设备未获批产品分布
数据来源:药智医械数据
2024年中国体外诊断注册审评情况分析
2024年国家药监局体外诊断产品审批完结情况
2024年国家药监局公示的批件发布数量显示,共完结5691件体外诊断产品申请事项。其中新注册产品申请796件,变更许可事项1266件,变更登记事项1673件,延续注册1802件。
在新注册产品中,国产产品630件,占比为79%;进口产品166件,占比为21%。在延续注册产品中,国产产品674件,占比为37%;进口产品1128件,占比为63%。在变更许可事项中,国产产品511件,占比为40%;进口产品755件,占比为60%。在变更登记事项中,国产产品1388件,占比为83%;进口产品285件,占比为17%。在体外诊断试剂产品中,新注册的国产产品数量远超于进口产品数量。
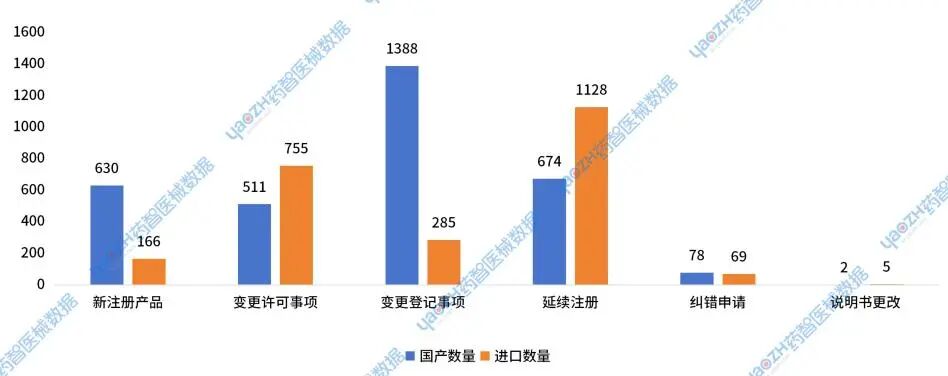
图29 2024年国家药监局体外诊断产品批件发布情况
数据来源:药智医械数据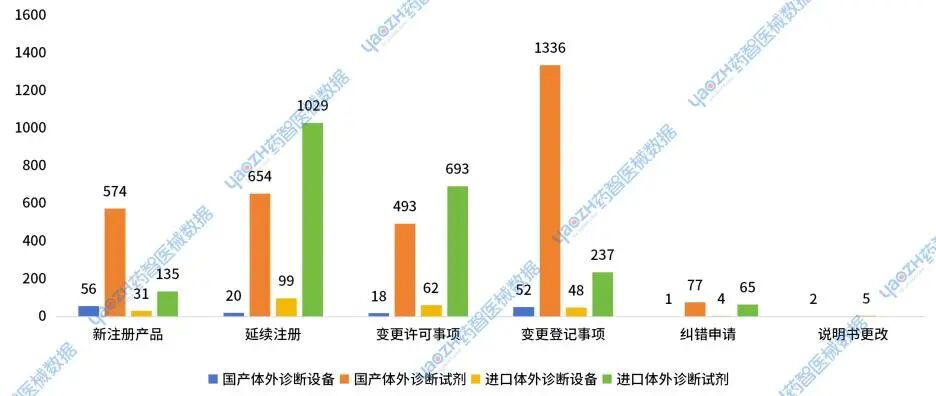
图30 2024年国家药监局体外诊断产品不同申请类型批件发布分布
数据来源:药智医械数据
2024年国家药监局体外诊断产品批件分布情况
2024年国家药监局体外诊断产品新注册产品获批数量为674件,占比85%;终止注册82件,占比10%;不予注册40件,占比5%。
2024年国家药监局体外诊断产品变更许可事项获批数量为1239件,占比97.9%;终止注册22件,占比1.7%;不予注册5件,占比0.4%。
2024年国家药监局体外诊断产品延续注册获批数量为1789件,占比99.3%;终止注册12件,占比0.7%;不予注册1件,占比不足0.1%。
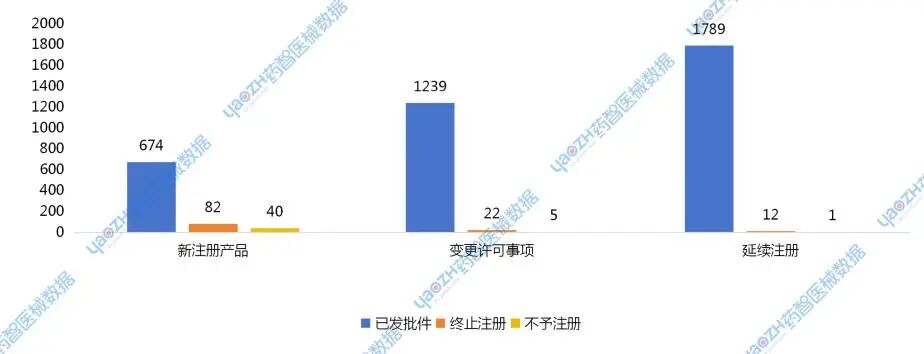
图31 2024年国家药监局体外诊断产品批件分布情况
数据来源:药智医械数据
2024年国产Ⅲ类体外诊断新注册产品审批完结情况
2024年国产Ⅲ类体外诊断新注册产品审批完结数量共630件,其中广东、江苏、北京、浙江和上海的数量较多。
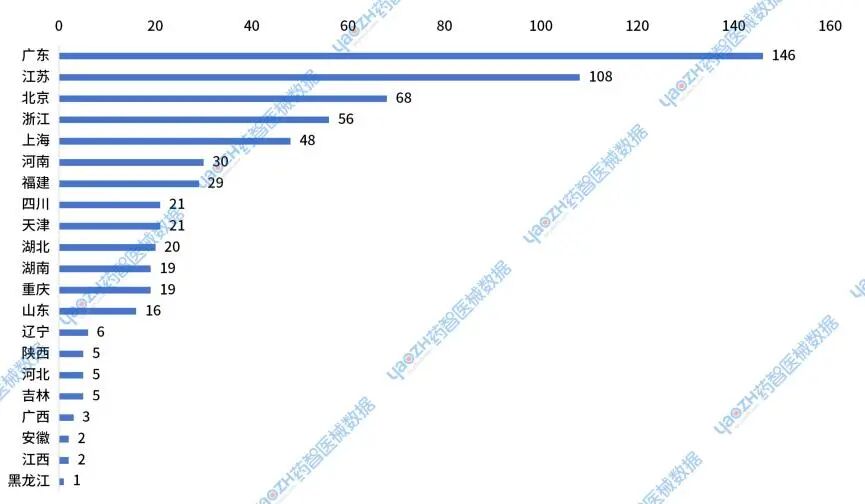
图32 2024年国产Ⅲ类体外诊断新注册产品审批完结分布
数据来源:药智医械数据
2024年进口体外诊断产品新注册产品国家或地区分布
2024年进口的新注册体外诊断产品主要来源于美国、德国、日本和爱尔兰等国家或地区。
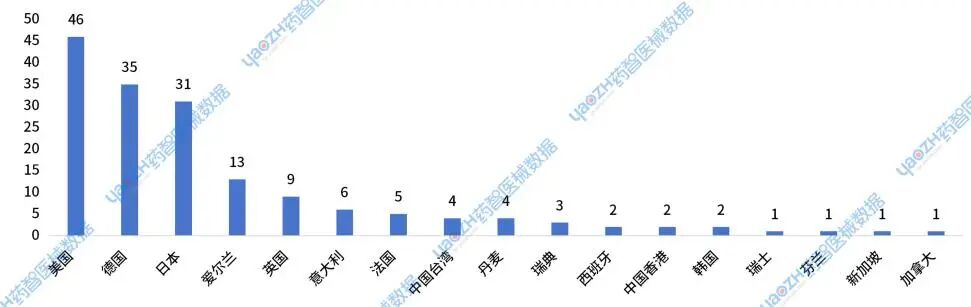
图33 2024年进口体外诊断产品新注册产品国别或地区分布
数据来源:药智医械数据
2024年国产体外诊断试剂新注册Ⅲ类器械获批产品分布
将2024年国产体外诊断试剂新注册获批的Ⅲ类器械按照被测物质分类,共有743个被检测物质类别,主要分布在致病性病原体抗原或抗体以及核酸,肿瘤标志物,人类基因检测这三个种类中。
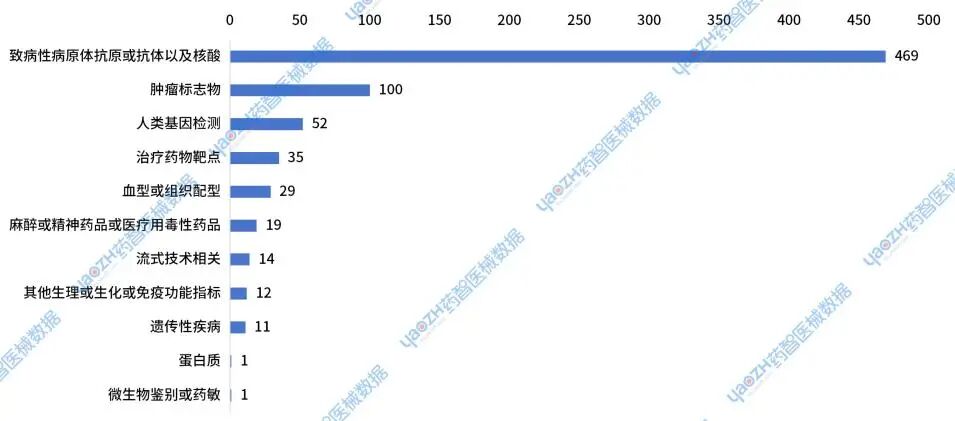
图34 2024年国产体外诊断试剂新注册Ⅲ类器械获批产品分布
数据来源:药智医械数据
2024年进口体外诊断试剂新注册获批产品分布
将2024年进口体外诊断试剂新注册获批的产品按照被测物质分类,共有179个被检测物质类别,主要分布在蛋白质,无机离子,致病性病原体抗原或抗体以及核酸这三个种类里。
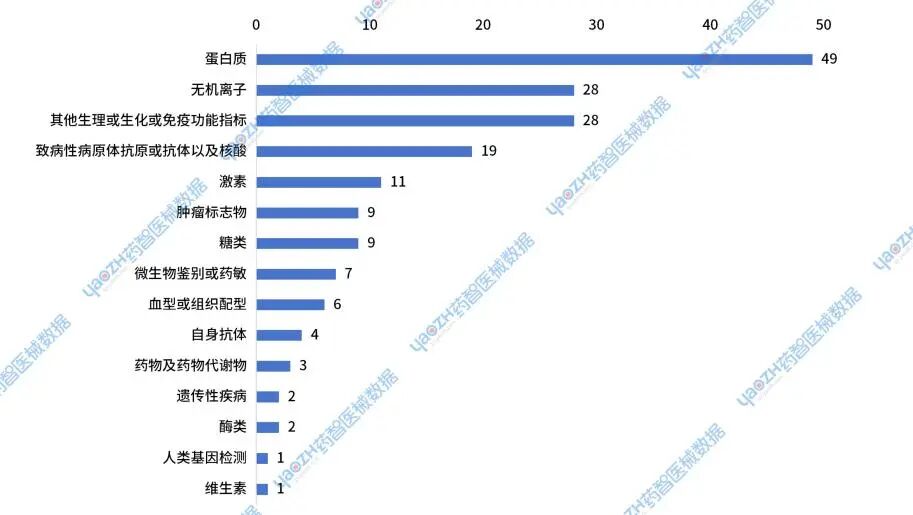
图35 2024年进口体外诊断试剂新注册获批产品分布
数据来源:药智医械数据
2024年国产体外诊断设备新注册Ⅲ类器械获批产品分布
2024年,国产体外诊断设备新注册获批的Ⅲ类器械主要为分子生物学分析设备。

图36 2024年国产体外诊断设备新注册获批的Ⅲ类器械分布
数据来源:药智医械数据
2024年进口体外诊断设备新注册获批产品分布
2024年,进口体外诊断设备新注册获批的产品总体数量较少,共有26个产品获批,其中多数为血液学分析设备。
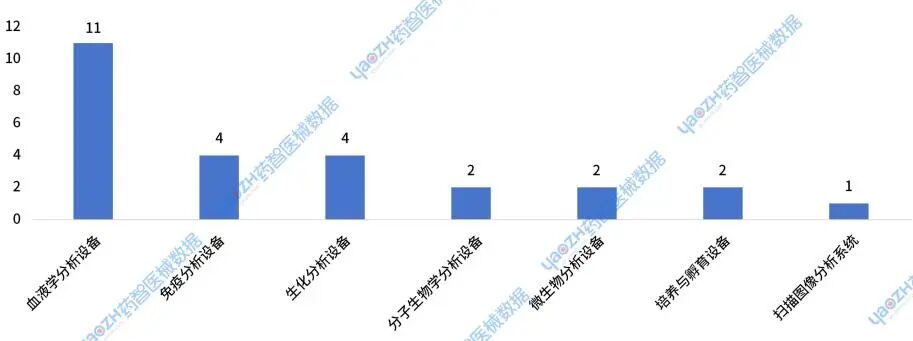
图37 2024年进口体外诊断设备新注册获批产品分布
数据来源:药智医械数据
2024年国家药监局体外诊断试剂产品未获批准被测物质分布
2024年新注册体外诊断试剂产品中,申请被测物质较多的品种为:致病性病原体抗原或抗体以及核酸类,肿瘤标志物类和人类基因检测类。其中,75个致病性病原体抗原或抗体以及核酸类被检物质未获批,未获批率为13.3%;5个肿瘤标志物类未获批,未获批率为4.4%;17个人类基因检测未获批,未获批率为24.3%。
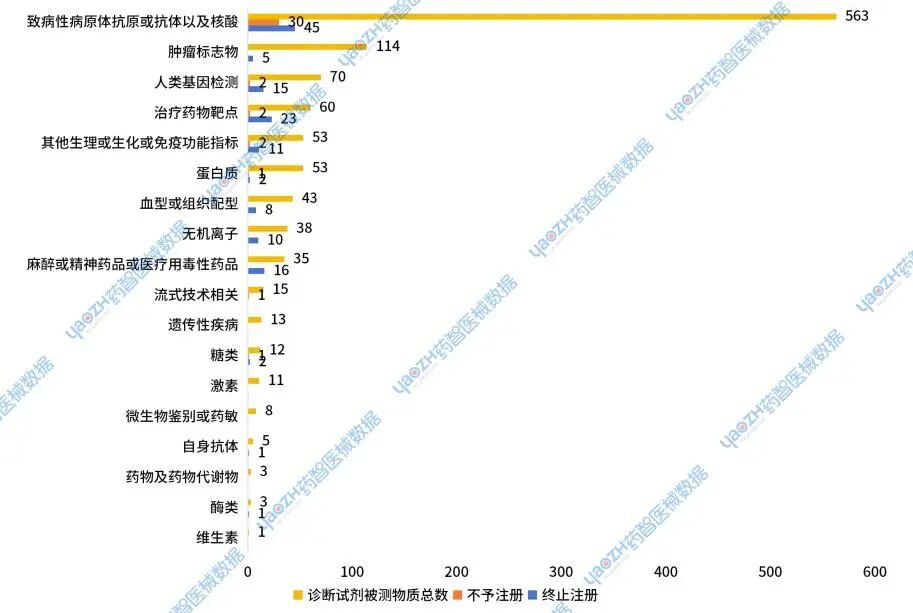
图38 2024年国家药监局体外诊断试剂未获批准被测物质分布
数据来源:药智医械数据
2024年国家药监局体外诊断设备产品未获批准产品类型分布
2024年新注册体外诊断设备产品中,申请数量较多的类型有分子生物学分析设备和血液学分析设备。其中7件分子生物学分析设备未获批,未获批率为13%;1件血液学分析设备未获批,未获批率为7%。
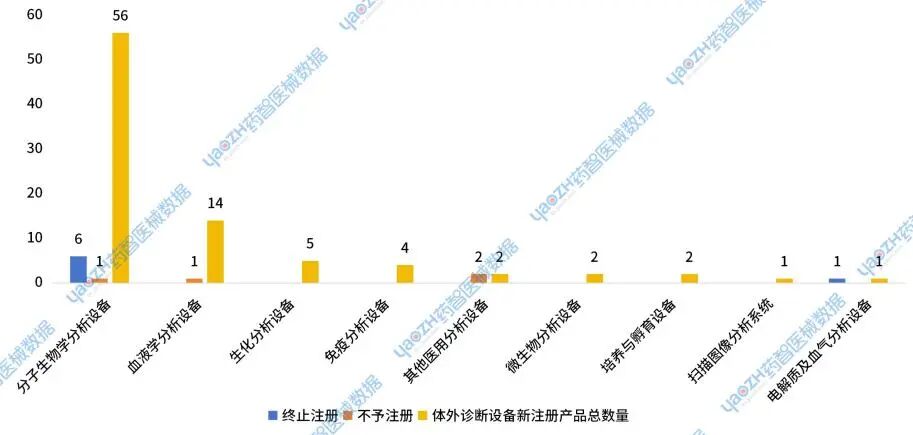
图39 2024年国家药监局体外诊断设备产品未获批产品类型分布
数据来源:药智医械数据
结 语
当前,医疗器械创新已成为健康中国战略的重要支撑。2025MDI-China医疗器械创新·合作大会已圆满落幕,将赋能国械创新促进产业融合,并将通过促进产学研医之间的高效交流与合作,为推动中国医疗器械行业高质量发展注入新动力。
2026 MDI,药智网期待再次与您相约~

责任编辑:木棉
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。

合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





