41款进口药退出中国
近日,国家药监局发布公告,依据《中华人民共和国药品管理法实施条例》《药品注册管理办法》的有关规定,正式决定注销氯雷他定片等80个药品注册证书。
01注销药品概况
本次注销的80个药品注册证书,覆盖临床多个治疗领域与剂型,其中41款被注销药品为进口药,占比超五成,国内药企则以老药、普药注销为主。
从企业维度看,多家跨国药企均有产品退出。例如,默克公司(Merck Sharp&Dohme LLC)注销了4个规格的甲型肝炎灭活疫苗;强生旗下杨森(Janssen-Cilag NV)注销了6个规格的芬太尼透皮贴剂;勃林格殷格翰则注销了6个规格的二甲双胍恩格列净片。此外,辉瑞的注射用盐酸多柔比星(抗肿瘤化疗药)、磷酸雌莫司汀胶囊,诺华的格隆溴铵吸入粉雾剂(呼吸系统用药),拜耳的利伐沙班干混悬剂(抗凝药)也均在注销名单中。
国内药企方面,江苏恒瑞、海南双成、特一药业、金陵药业等企业也有药品注销,品种多为上市多年的老药、普药。例如,太仓制药厂一次性注销了11个品种,包括异烟肼片、复方利血平片等基础药物;海南双成药业集中注销了7个注射剂,涵盖注射用盐酸克林霉素和注射用肌苷多个规格;恒瑞医药注销了酒石酸长春瑞滨软胶囊。
从治疗领域来看,注销药品覆盖范围广泛,其中抗感染、抗肿瘤和心血管代谢类疾病药物占比较高。抗感染类包括异烟肼片、注射用盐酸克林霉素等老药;抗肿瘤类有酒石酸长春瑞滨软胶囊、注射用盐酸多柔比星等常用化疗药;心血管与代谢类涵盖吲达帕胺片(降压)、二甲双胍恩格列净片(降糖复方制剂)、利伐沙班干混悬剂(抗凝)等。其中二甲双胍恩格列净片涉及6个规格,均由勃林格殷格翰申请注销。
从剂型角度分析,片剂与注射剂两类剂型的合计占比超过六成,是注销品种中的主要类别。片剂共有25个,包括氯雷他定片、异烟肼片(太仓制药厂注销100mg和300mg两种规格)等;注射剂共30个,涵盖注射用盐酸多柔比星(抗肿瘤)、盐酸左氧氟沙星氯化钠注射液(抗感染)、利司那肽注射液(降糖)等。
此外,滴眼液、乳膏剂、栓剂(如美沙拉秦栓)、贴剂(如芬太尼透皮贴剂)等局部用药,以及甲型肝炎灭活疫苗、注射用重组人II型肿瘤坏死因子受体-抗体融合蛋白(治疗类风湿关节炎)等生物制品,也均在注销名单中。
02依申请注销,是唯一原因
根据国家药监局公告及注销药品目录,80个药品均为“依申请注销”,即由药品上市许可持有人主动向监管部门提出申请,而非因安全性问题被强制退市。
医药行业的竞争力源于创新,当新型药品在疗效、安全性、便利性上形成优势,老药自然缺乏竞争力。
以此次注销品种为例,抗感染领域的注射用盐酸克林霉素虽为常用抗生素,但近年来新型β-内酰胺类抗生素(如头孢他啶阿维巴坦)在抗菌谱、耐药性上更具优势,临床使用占比持续提升,导致老药市场需求下滑。降糖领域的利司那肽注射液(每日一次给药),则因司美格鲁肽、替尔泊肽等长效GLP-1药物(一周一次给药、兼具减重效果)的普及而被挤压市场空间,此次赛诺菲申请注销其6个规格,正是产品迭代的直接体现。这种“新替旧”的逻辑,是医药行业持续进步的必然结果。
药品作为特殊商品,其生产与销售始终受到成本、利润与市场需求的影响。在医药市场竞争日趋激烈的背景下,企业倾向于将有限资源集中于核心产品,因此会主动注销销量低、利润薄或不符合战略方向的产品。本次注销名单中,不少品种属于市场竞争极度激烈的普药、仿制药,如肌苷片、维生素B2片等,由于这类产品利润微薄,生产厂家众多,价格战激烈,对企业而言,注销此类品种,有助于将资源转移到高价值药或优势专科药上,这是应对市场竞争的理性选择。
归根结底,无论是产品迭代、资源优化还是战略调整,这些药品被注销的根本原因在于——不赚钱了。
03外企撤退的背后
7月1日,国家药监局发布公告,宣布注销56个药品的注册证书。值得关注的是,在注销名单中,外资企业的产品超过30个,占比过半,涉及辉瑞、诺华、葛兰素史克、勃林格殷格翰等多家知名药企旗下的部分原研药。这些退市产品大多为专利已到期或面临仿制药激烈竞争的成熟品种。例如,辉瑞的利奈唑胺葡萄糖注射液、诺华的依维莫司片等,均因在国家集采中中标价格大幅下降(部分降幅超过80%),难以维持原有利润空间,最终选择退出。
8月,市场再度传出消息,赛诺菲中国正在调整其心血管领域的市场策略和产品管线,旗下重点降脂药波立达(阿利西尤单抗)将停止在中国市场的推广,并逐步退出。退出原因主要有两方面:一是2025版《中国国家医保药品目录》中纳入了更多国产PCSK9抑制剂,使得胆固醇管理治疗选择更加多元;二是受到全球原料供应紧张的影响,该药物在中国市场的供应也面临挑战。
对外资企业而言,全球产品战略调整是申请注销药品或者退出市场的一个重要原因。部分产品因在全球市场中不再是战略重点,或已有新一代替代品上市,企业会选择从某些区域市场退出,以集中资源深耕核心领域。
本次注销涉及41个进口药,背后折射出外资企业进口药或者原研药退出中国市场的三大现实因素:
其一,集采政策的影响。集采政策通过“以量换价”模式对药品利润进行压缩,部分未参与或未中选的产品其市场布局面临调整,这也推动了外资企业对现有产品组合的评估与调整。
其二,药企低价竞争。在氯雷他定等专利过期药品领域,国内仿制药企凭借价格优势占据市场,外企因运营成本高难以参与价格战,不得不退出激烈竞争的“红海”。
其三,企业战略转向。面对激烈的仿制药竞争,越来越多外企选择将资源转向创新药领域,主动退出低利润、高竞争的普通药品市场。
04结语
国家药监局此次批量注销80个药品注册证书,主要是淘汰那些市场竞争力弱的产品,进而优化临床上的用药结构。对医药企业而言,聚焦创新研发、契合临床未满足的需求等等是在激烈的竞争中实现可持续发展的关键。
附表:注销药品注册证书目录
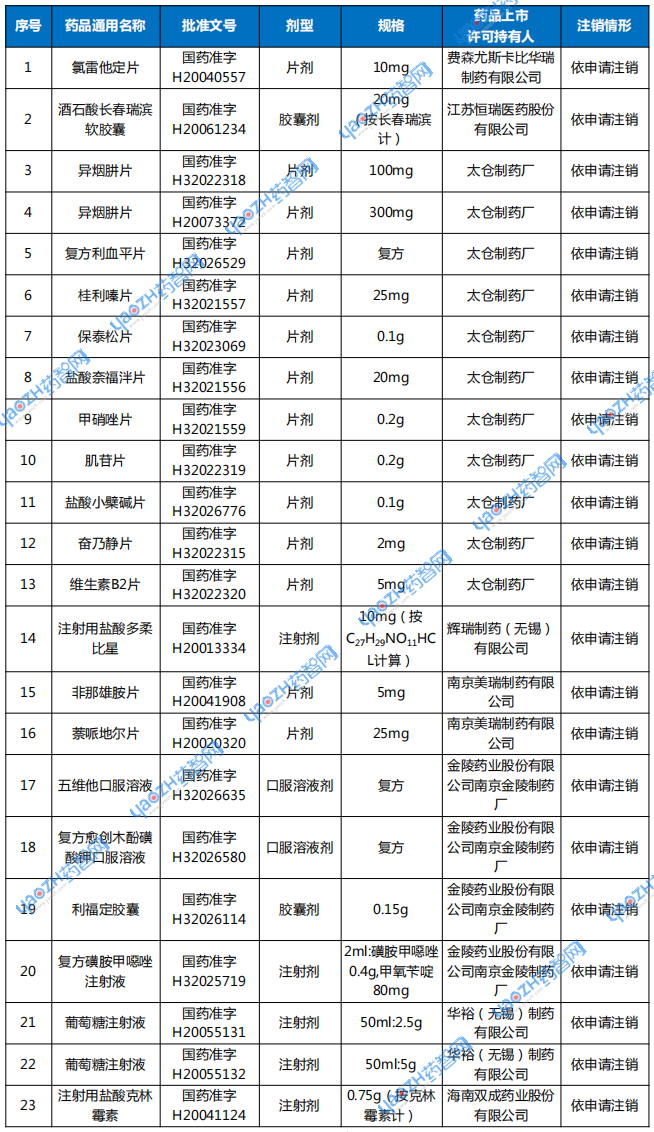
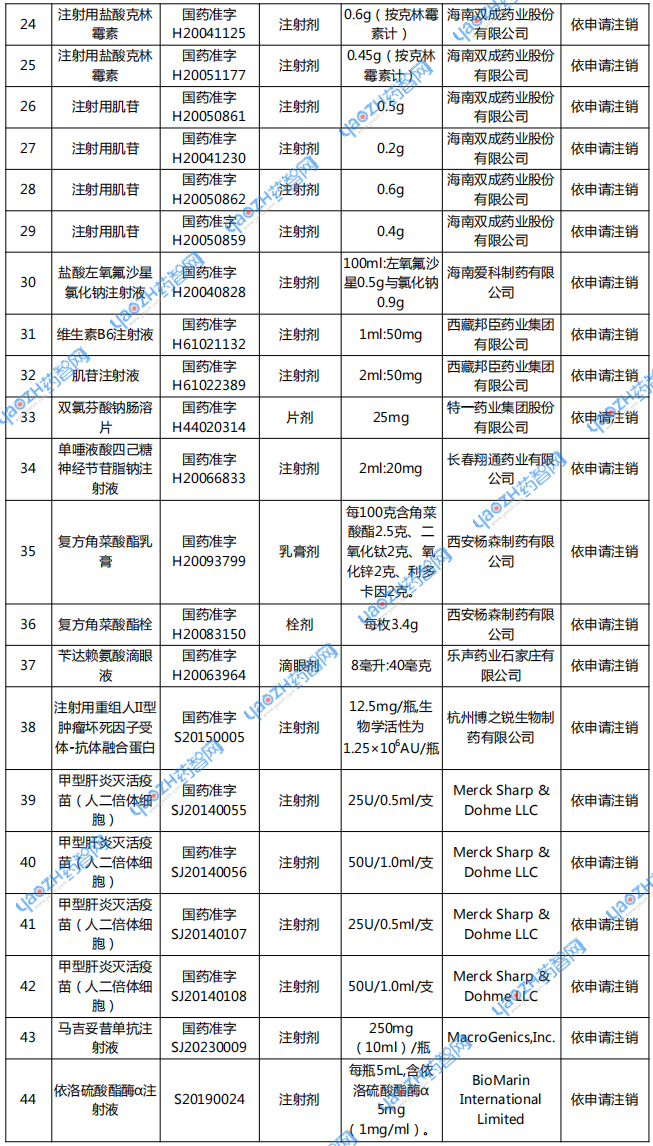
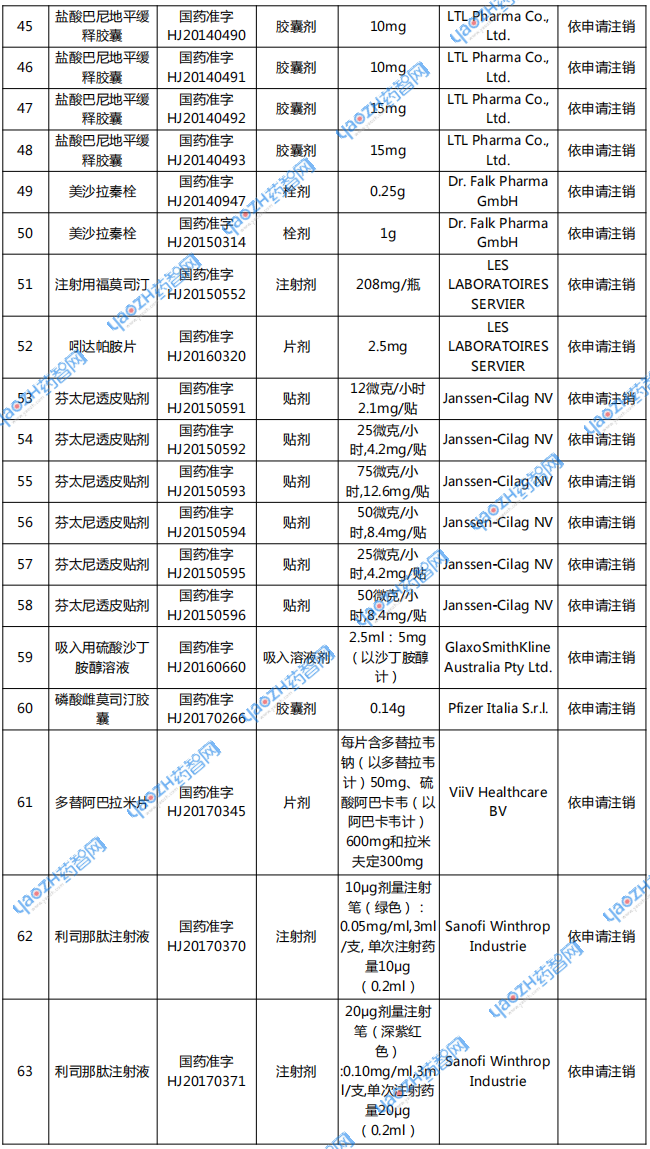
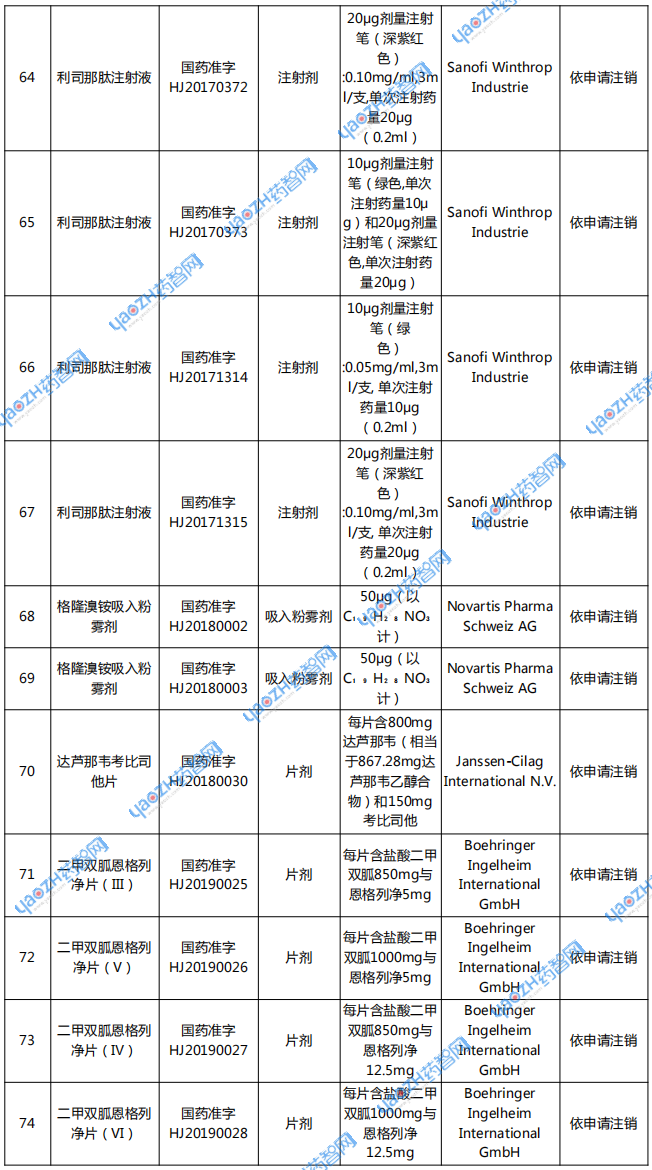
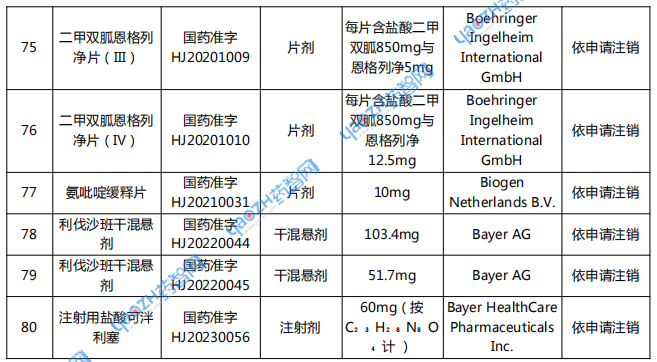
资料来源:国家药监局


责任编辑:琉璃
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。
合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





