优先审批产品遇冷,数量骤减30%!中国医疗器械审批全景分析
政策助力、前沿技术深度融合的双轮驱动下,我国医疗器械行业正经历着从“跟随式创新”到“源头式突破”的战略转型,创新医疗器械研发呈现加速涌现态势,2024年全年,我国进入创新通道的医疗器械数量达到165款,其中涵盖了手术机器人、PFA、脑机接口等多个高端领域,中国医疗器械产业已进入高质量发展的新阶段。
本报告节选自《中国医疗器械研发蓝皮书(2025)》第三章——2024年中国医疗器械创新和优先审批分析报告,从创新审批、优先审批、国产与进口产品差异多维度切入,深入解析2024年中国医疗器械发展方向,为行业参与者提供决策参考。

图片来源:《中国医疗器械研发蓝皮书(2025)》
2024年中国医疗器械创新发展现状
国家药监局于2014年发布《创新医疗器械特别审批程序(试行)》,于2016年发布《医疗器械优先审批程序》,并于2018年发布《创新医疗器械特别审查程序》。此后,各省药监局根据各地实际情况,相继发布了相应的医疗器械创新产品注册程序和医疗器械优先注册程序。相关文件明确,对于可以进入创新审批的器械产品享有:早期介入,专人负责,检测、体系核查、审评优先等权益。
可以进入创新医疗器械特别审查通道的产品的一般要求是:
(一)申请人通过其主导的技术创新活动,在中国依法拥有产品核心技术发明专利权,或者依法通过受让取得在中国发明专利权或其使用权,创新医疗器械特别审查申请时间距专利授权公告日不超过5年;或者核心技术发明专利的申请已由国务院专利行政部门公开,并由国家知识产权局专利检索咨询中心出具检索报告,报告载明产品核心技术方案具备新颖性和创造性。
(二)申请人已完成产品的前期研究并具有基本定型产品,研究过程真实和受控,研究数据完整和可溯源。
(三)产品主要工作原理或者作用机理为国内首创,产品性能或者安全性与同类产品比较有根本性改进,技术上处于国际领先水平,且具有显著的临床应用价值。
2018-2024年进入器械创新审批通道的产品情况
整体趋势上看,2024年进入器械创新审批通道的数量比2023年略有下降,此前自2019年以来一直呈现出的上升趋势被打破,2023年进入器械创新审批通道的产品数量成为近5年来的最高峰值。
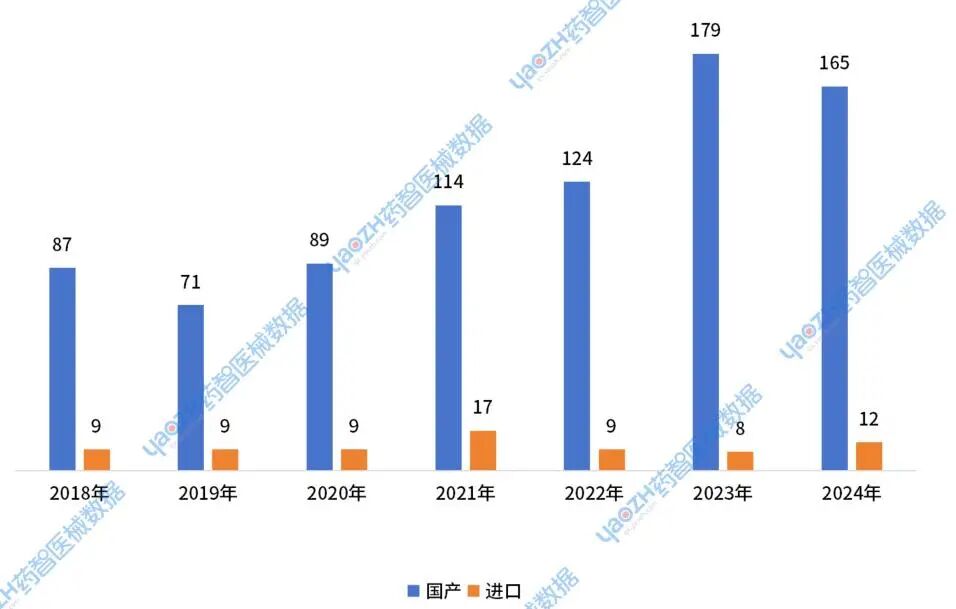
图1 2018-2024年进入器械创新审批通道数量
数据来源:药智医械数据
2018-2024年完成审批的创新医疗器械产品分布
2018-2022年,创新医疗器械完成审批的数量持续增长,增速突破20%。虽然2023年略有下降,但2024年该数量重归增长行列,相比2023年完成审批的数量增加40%。
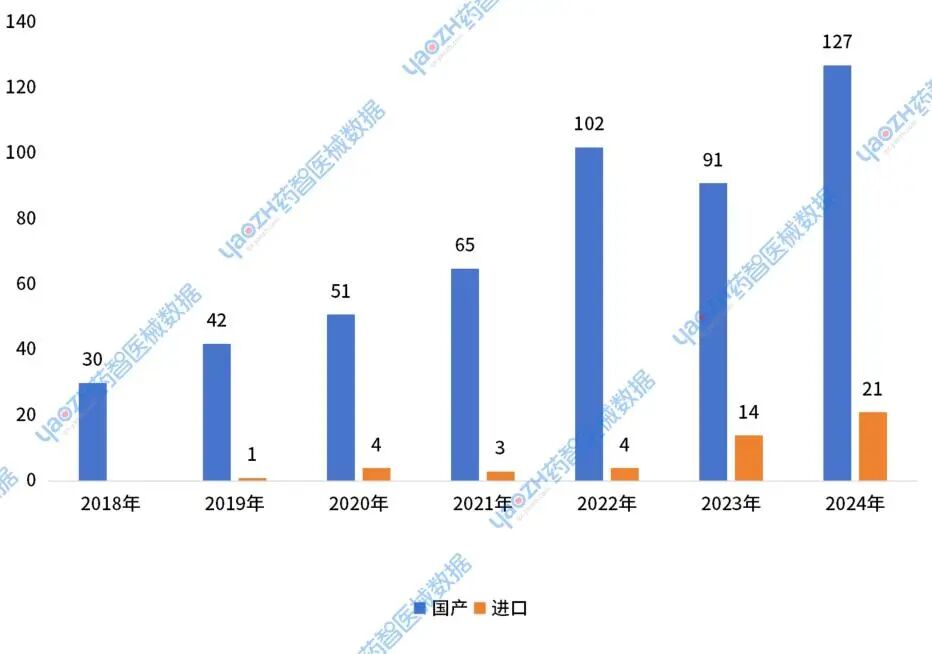
图2 2018-2024年完成审批的创新医疗器械产品分布
数据来源:药智医械数据
2018-2024年进入创新审批通道的产品在各个审核机构的分布
2018-2024年,各审核机构进行审评的创新器械数量分布中,创新器械产品基本集中在国家药品监督管理局,地方药监局中浙江、江苏、北京、广东等地的药监局审核进入创新审批通道的产品数量相对其他省份更为突出。

图3 2018-2024年进入创新审批通道的产品在各个审核机构的分布
数据来源:药智医械数据
2018年-2024年进入器械创新审批通道和完成审批的产品分布
2018-2024年,进入器械创新审批通道的产品类别主要包括:有源手术器械(占比15%),无源植入器械(占比14%),体外诊断试剂(占比10%),医用成像器械(占比10%)。而主要完成审批的产品类别有:有源手术器械(占比12%),无源植入器械(占比11%),医用成像器械(占比11%),体外诊断试剂(占比10%)。从进入创新审批通道和获得批准上市的数量来看,有源手术器械,无源植入器械,医用成像器械和体外诊断试剂仍然是创新产品研发最活跃的领域。其中,近6年的数据统计显示,有源手术器械进入创新通道的数量已经超过无源植入器械。
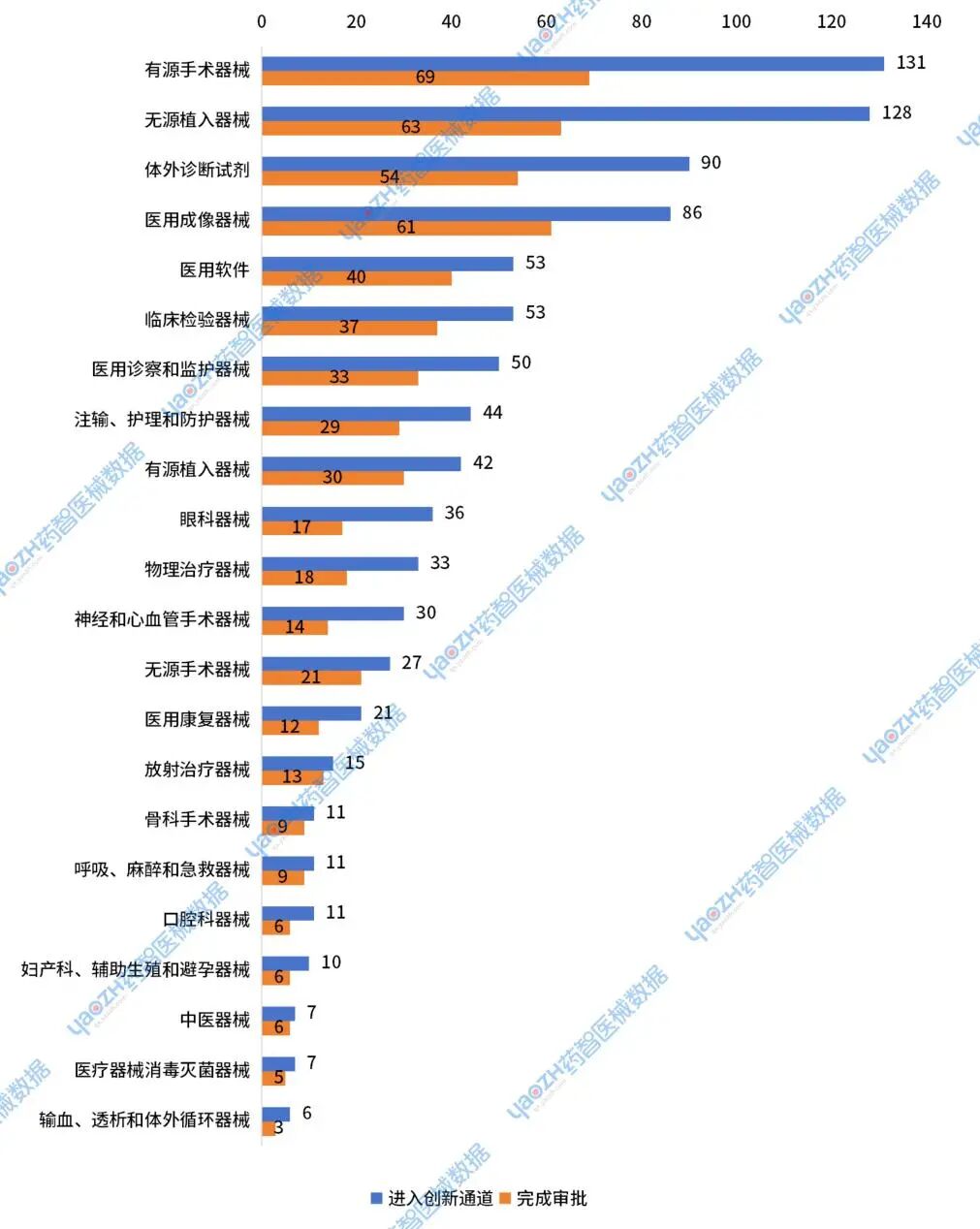
图4 2018-2024年进入器械创新审批通道和完成审批的器械产品分布
数据来源:药智医械数据
2018-2024年国产器械进入器械创新审批通道和完成审批的企业所在地分布
2018-2024年累计进入器械创新审批通道的产品,按照企业所在省市主要分布在北京(占比17%),江苏(占比15%),浙江(占比14%),广东(占比13%)和上海(占比12%)。累计完成审批的创新器械产品,按照企业所在省市主要分布在北京(占比19%),浙江(占比17%),上海(占比13%),广东(占比13%)和江苏(占比11%)。
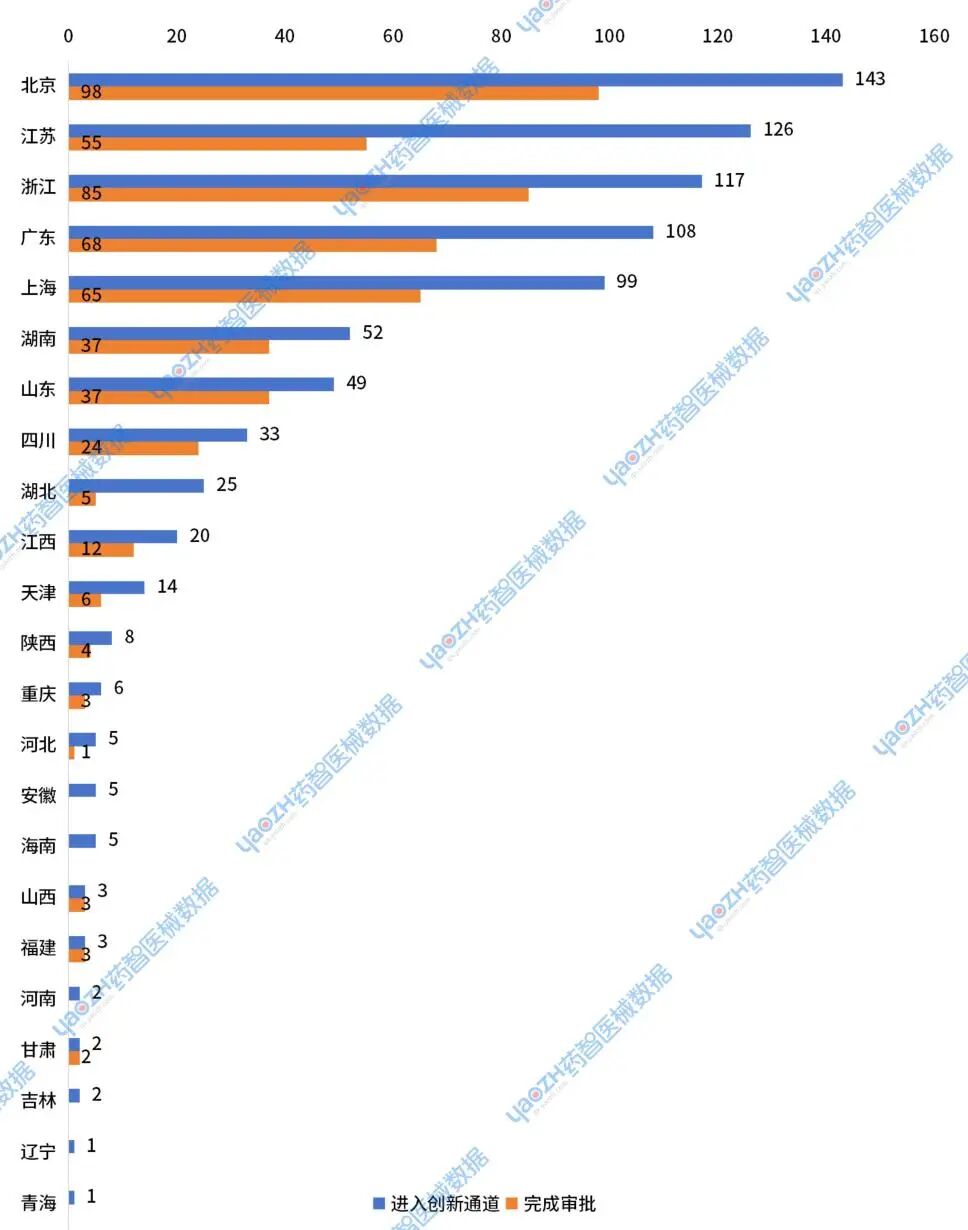
图5 2018-2024年国产器械进入器械创新审批通道和完成审批的企业所在地分布
数据来源:药智医械数据
2024年中国创新审批器械情况分析
2024年进入器械创新审批通道的数量
创新审批的产品以国家药监局进行审核的国产Ⅲ类器械为主,同时也有部分Ⅱ类器械也进入创新审批通道,它们主要分布在江苏、北京、上海等药监局。
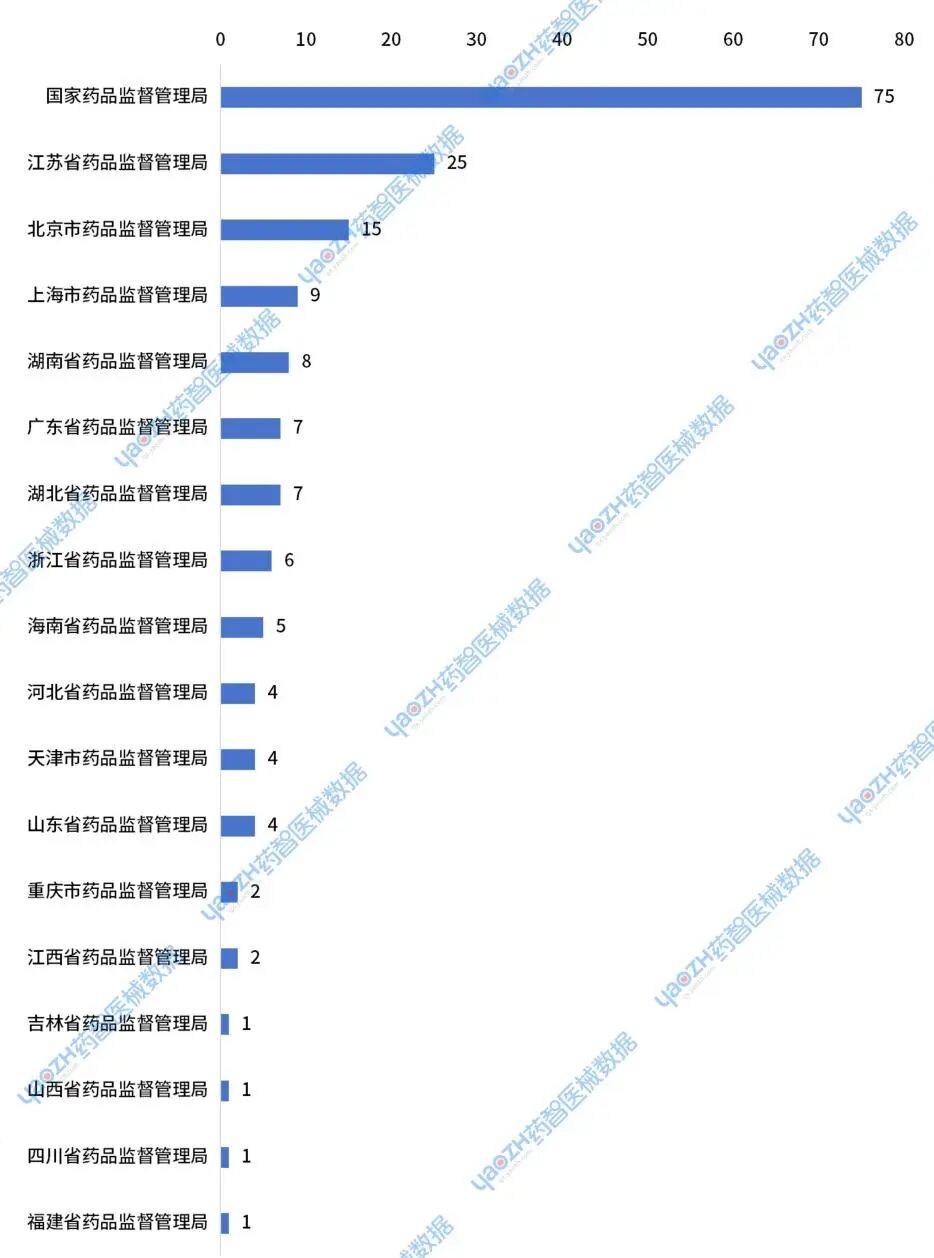
图6 各个药监局公示的进入器械创新审批通道的数量
数据来源:药智医械数据
2024年进入器械创新审批通道的省市分布
从2024年进入创新审批通道的企业分布来看,这些企业主要分布在江苏、北京、上海、广东等省市。
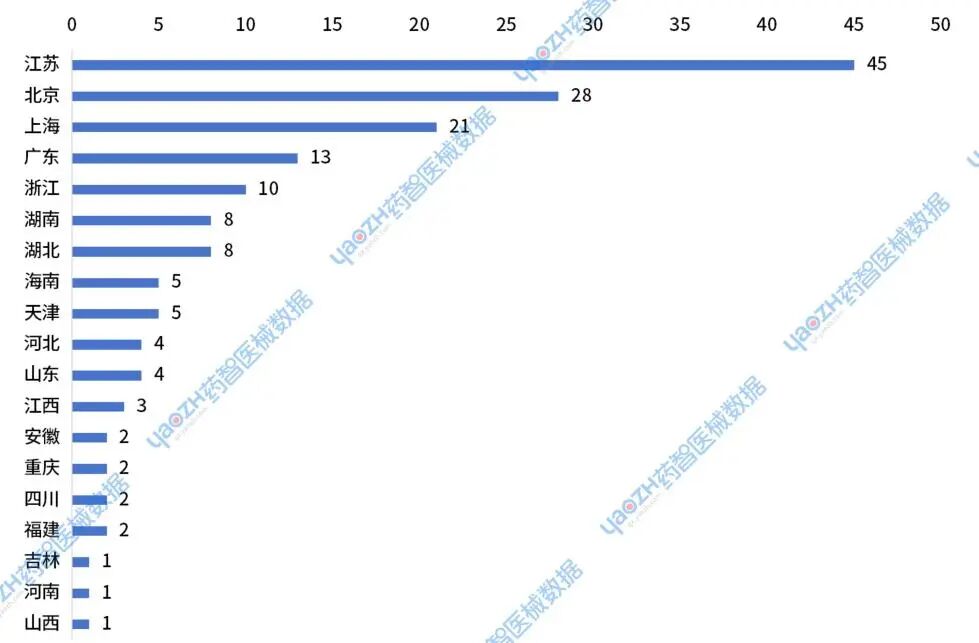
图7 2024年进入器械创新审批通道的企业所在省市
数据来源:药智医械数据
2024年进入器械创新审批的产品类别分布
2024年共有177件医疗器械进入创新审批通道,从2024年进入器械创新审批通道的产品分布来看,有源手术器械,无源植入器械,体外诊断试剂和医用成像器械的数量较多,相关领域的研发活跃度较高。
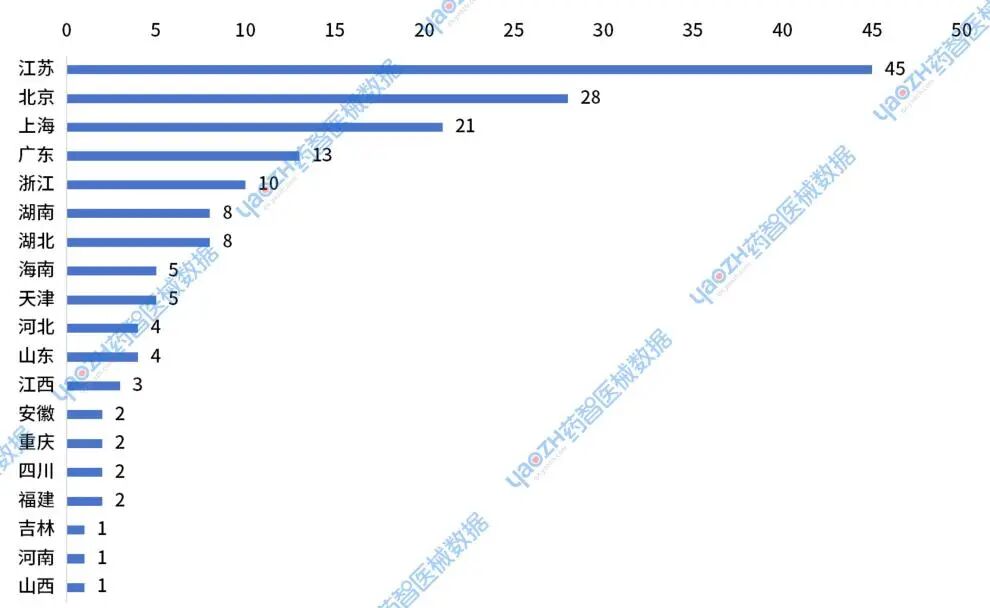
图8 2024年进入器械创新审批通道的企业所在省市
数据来源:药智医械数据
2024年完成审批的创新器械类别分布
2024年一共有148件创新医疗器械产品完成审批,其中145件获批上市,3件终止注册。完成审批的器械产品数量以有源手术器械,体外诊断试剂和无源植入器械为主。
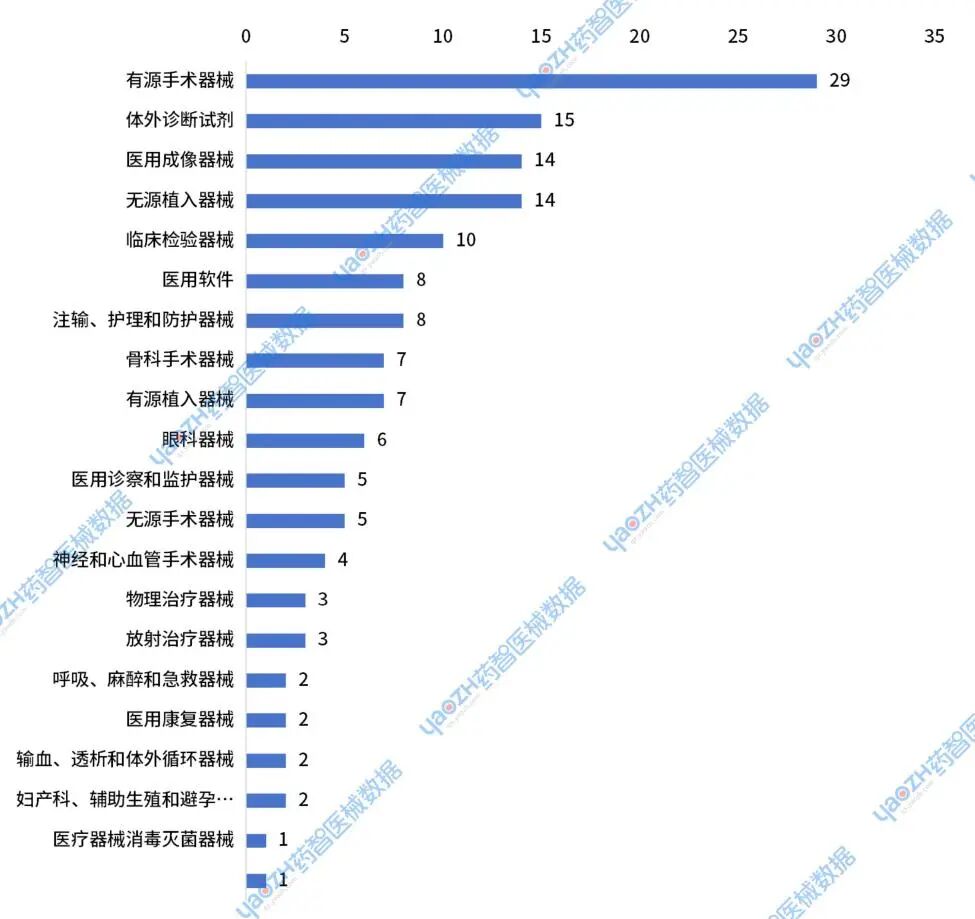
图9 2024年完成审批的创新器械产品分布
数据来源:药智医械数据
2024年中国优先审批器械情况分析
2024年进入器械优先审批通道的数据量
2024年,进入器械优先审批通道的数量为99件,相比去年有近30%的下降。国家局和地方药监局的器械优先审批政策存在部分差异,目前有公示的理由主要产品有技术创新、产品是国家或省市项目。
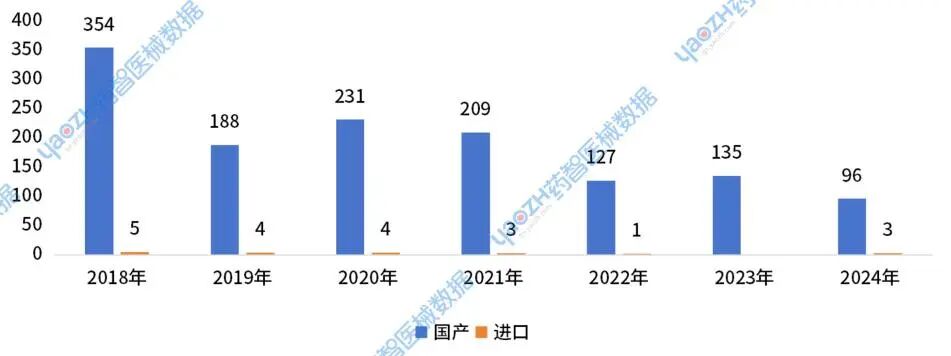
图10 2018年-2024年进入器械优先审批通道数量
数据来源:药智医械数据
进入器械优先审批通道的企业所在省市分布
2024年,江苏、天津、重庆、湖南和海南等地器械优先审批的企业数量排名较靠前。
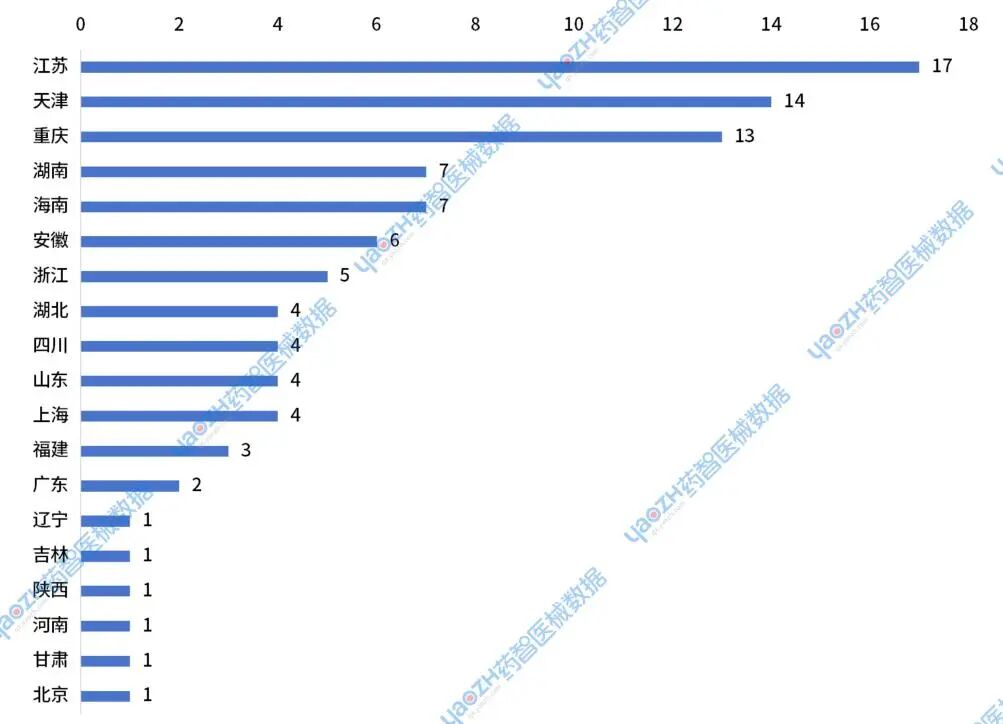
图11 2024年进入器械优先审批通道的企业所在省市分布
数据来源:药智医械数据
2024年进入器械优先审批的各审核机构分布
2024年,从审核机构来看,器械优先审批主要集中在国家药监局、天津、江苏、重庆等药监局。
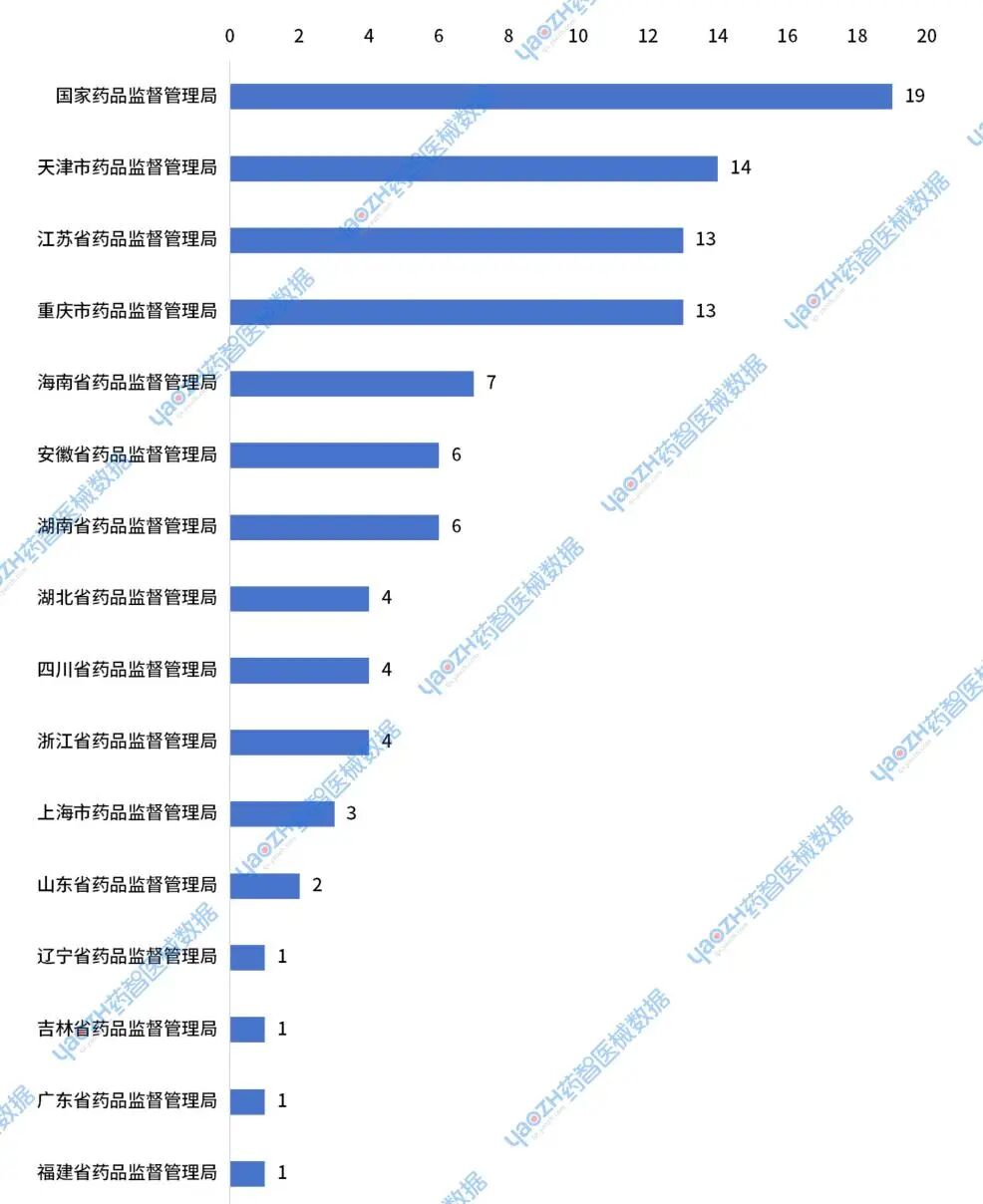
图12 2024年进入器械优先审批的各审核机构分布
数据来源:药智医械数据
2024年进入器械优先审批通过和完成审批的产品类别分布
2024年,共有99件器械产品进入器械优先审批通道,从2024年进入器械优先审批通道的产品分布来看,体外诊断试剂和临床检验器械的数量较多,表明这类产品比较容易获得进入优先审批的资格。进入优先审批的产品一般审批时间较短。2024年通过优先审批通道完成审批的有95件,其中93件获批上市,2件终止注册。完成审批的产品分布主要是体外诊断试剂、医用诊察和监护器械为主。

图13 2024年进入器械优先审批通道与获批上市的产品类别分布
数据来源:药智医械数据
结 语
当前,医疗器械创新已成为健康中国战略的重要支撑。2025MDI-China医疗器械创新·合作大会已圆满落幕,将赋能国械创新促进产业融合,并将通过促进产学研医之间的高效交流与合作,为推动中国医疗器械行业高质量发展注入新动力。
2026 MDI,药智网期待再次与您相约~

责任编辑:木棉
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。

合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





