【独家】2018国内临床试验登记年终报告,一致性评价BE试验占比30%
随着“临床试验数据自查核查”和“仿制药质量和疗效一致性评价”等政策的出台,临床试验的关注度不断提高。药物临床试验登记平台的数据也逐年增加,截止2018年12月31日,平台公示获得CTR号的临床试验总数为7423项。
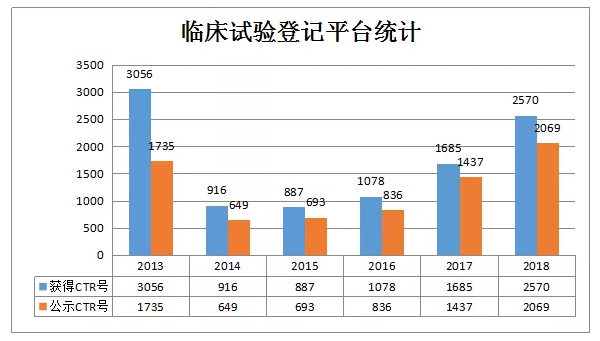
2018年已公开的临床试验分析
2013年28号公告要求,获得药物临床试验批件的,申请人须在获批件后1个月内完成试验预登记,以获取试验唯一登记号。但是,部分药企获得登记号后并未完善和公示临床试验信息,所以笔者接下来仅对2018年12月31日前公示的2570项临床试验进行全面分析。
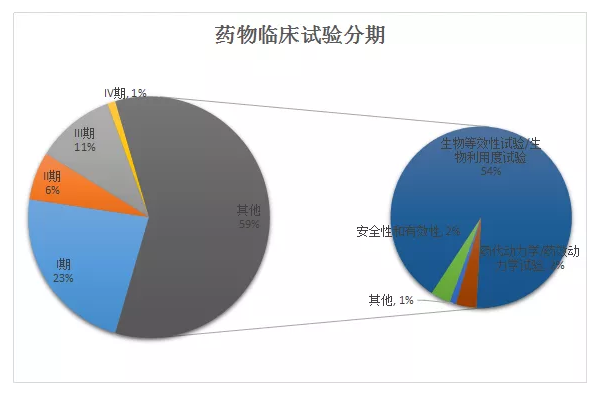
1、2018年临床试验分期
2018年临床试验分期中“其他”的占比急速上升,达到59%。究其原因,主要是随着仿制药质量和疗效一致性评价的开展,生物等效性/生物利用度试验登记增加。对“其他”分期进行试验类型统计,生物等效性/生物利用度试验占比高达54%。
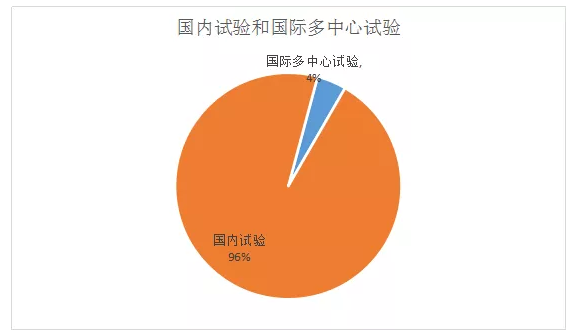
2、国内试验和国际多中心试验
目前药物临床试验平台中的临床试验多以国内试验为主,2018年总计86个国际多中心试验,其中3期试验78个,占比90%。从药品来看,基本均为新药临床试验。
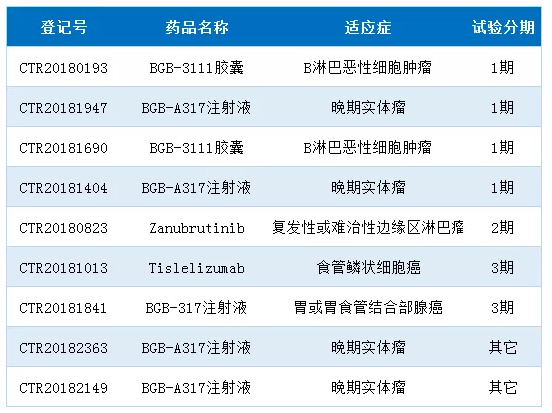
国际多中心试验大多是外企开展的,国内仅百济神州开展了9个多中心试验。以下是百济神州2018年登记的多中心试验。
表1:百济神州2018年登记的多中心试验
3、2018年临床试验最受关注的药品
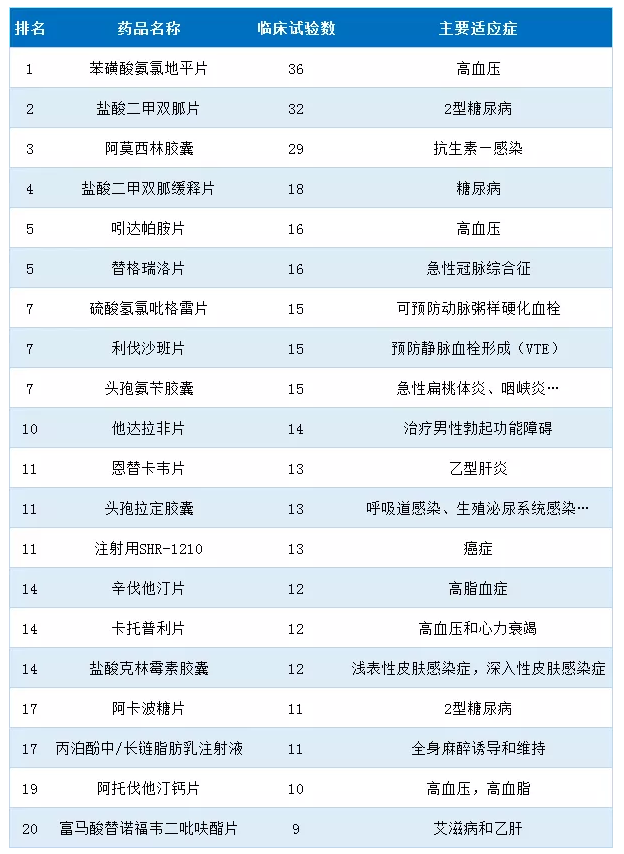
对药品的临床试验登记情况统计发现,2018年最受关注的药品为苯磺酸氨氯地平片,其次是盐酸二甲双胍片和阿莫西林胶囊。进一步分析计发现,最受关注的药品TOP10基本都是开展的生物等效性试验。仅3个药代动力学/药效动力学试验和1个安全性和有效性试验。
表2:最受关注的临床试验药物TOP20
4、2018年临床试验登记最积极的企业
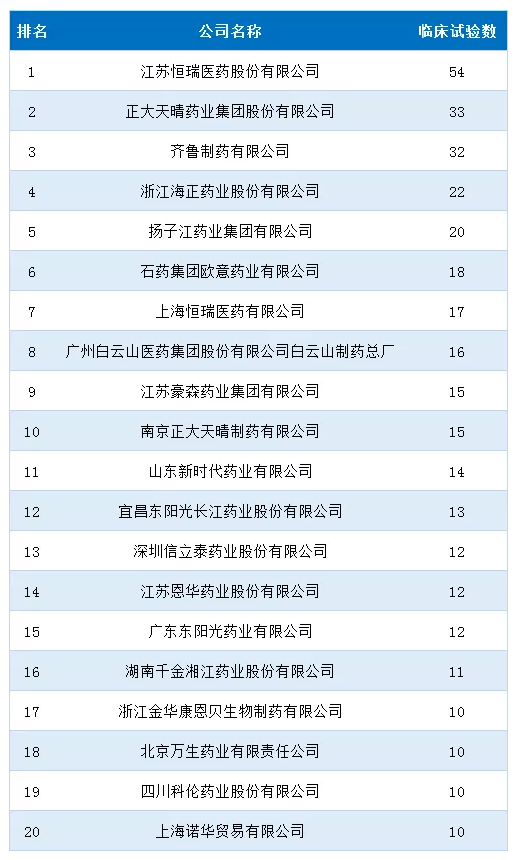
总的来说,2018年临床试验登记和各企业的整体实力呈正相关,整体排名与2017年保持一致。本次统计未按照母公司进行统计,子公司独立计算。江苏恒瑞临床试验登记数量最多,其次是正大天晴药业。不过正大天晴和恒瑞不同之处在于,正大天晴登记的临床绝大多数为生物等效性试验(占比58%),而江苏恒瑞以药代动力学/药效动力学试验居多(占比31.5%)。齐鲁、华海、海正、扬子江等企业也有较多的生物等效性试验,可见,2018仿制药质量和疗效一致性评价依旧是各企业的重头戏。
表3、2018年临床试验登记最积极的企业
5、一致性评价BE试验
2018年,仿制药一致性评价已登记的BE试验有613个,登记的BE试验主要格局如下:BE试验已经有278个完成,同时还有25%尚未招募,15%的临床试验正在进行中。
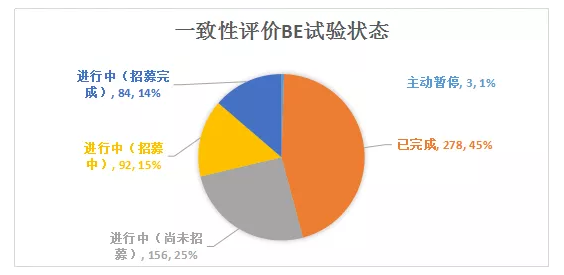
BE试验登记数量最多的药品分别是苯磺酸氨氯地平片(29)、阿莫西林胶囊(28)和盐酸二甲双胍片(28)。登记号最多的企业是广州白云山医药集团股份有限公司白云山制药总厂。
综上所述:纵观2018年已登记的临床试验,可以发现BE试验所占比重较大,大型药企临床试验数量较多。本文数据来源于CDE药物临床试验登记与公示平台和药智中国临床试验数据库(点击这里即可进入)。
数据来源:药智数据
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。




• 苯磺酸氨氯地平片一致性评价最新进度分析
• 仿制药一致性评价最新进展:受理号达1289个,通过308个
• 2019年国内临床试验年中报告,一致性评价BE试验占19%
• 盘点:2019上半年中国药企获FDA批准的ANDA再添47个,同比增加30.56%
• 一致性评价最新进展:受理号达1197个,通过216个,视同通过77个
• 【独家】一致性评价最新进展:受理号达1117个,通过200个,视同通过67个
• 【独家】2019中国药企ANDA已添23个,昔日霸主华海毫无斩获,各企业赴美热情降低?
• 【独家】一致性评价最新进展:受理号达1051个,通过183个,视同通过65个
• 【独家】2018国内临床试验登记年终报告,一致性评价BE试验占比30%
• 【独家】100个ANDA,24家药企,2018年中国制药国际化道路再创佳绩
合作
 扫码关注-药智网公众号
扫码关注-药智网公众号Copyright © 2009-2025 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938



