授予孤儿药?今天吉利德表示:我不要
今日,吉利德科学(Gilead Sciences)公司发布声明,宣布已经向美国FDA提出申请,要求FDA收回授予瑞德西韦的孤儿药资格,并且放弃与孤儿药资格相关的所有优惠权益。其中就包括免去在新药申请前递交儿科研究计划(pediatric study plan),这一过程的审评时间可能长达210天。
吉利德表示,即使在没有孤儿药资格的情况下,瑞德西韦监管审评过程也将加速完成。

吉利德科学公司声明英文全文
关于美国食品和药品管理局(FDA)批准美国Gilead科学公司Remdesivir(瑞德西韦)孤儿药认证(OrphanDrugDesignations)的报道如下:
北京时间3月24日早4:30(美东时间23日4:30pm),美国食品和药品管理局(FDA)发布消息:批准美国Gilead科学公司的Remdesivir(瑞德西韦)孤儿药认证(OrphanDrugDesignations),适应症为新型冠状病毒病(COVID-19)。
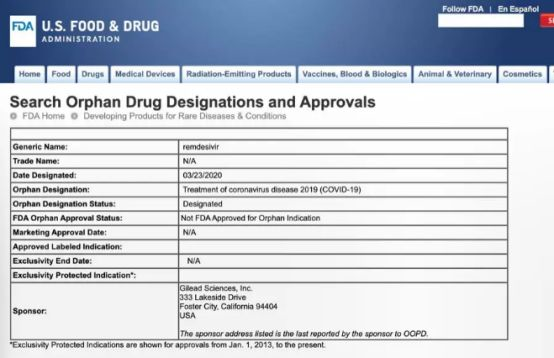
并非上市,瑞德西韦的临床试验尚未结束,目前,吉利德正在开展6项临床试验评估瑞德西韦治疗COVID-19患者的疗效。其中,在中国进行的两项临床试验有望在4月获得结果。
何为孤儿药?
孤儿药是指专门用于治疗或控制罕见病的药物。罕见病,是指影响到少数人群的疾病,具体比例各国定义不同。在美国,病例数目在20万人以下的疾病被定义为罕见病,很多癌症属于罕见病的种类。
为何全球大流行,却戴孤儿药帽子?
此番瑞德西韦获得孤儿药认证,是特殊时期的特殊办法。
在追求利润和投资回报的情况下,由于病例数目少,医药企业不倾向对罕见疾病药物的研发。为了鼓励罕见病治疗用药研发,1983年开始美国FDA给针对孤儿症的研究项目提供绿色通道,对孤儿药物有特殊的激励措施,其中包括:7年研发市场独占(且不受专利影响)、加速审批、研发期间税费优惠、专项研发基金资助,免除新药申请费、协助药物的研究和实验设计等。
瑞德西韦本次孤儿药身份的认证,一方面利好企业,既能降低新药研发的投入,折抵税收;又可以保护新药研发后的收益,7年内无仿制药抢占市场;更可以加速审批的速度。另一方面其实已经表明了对于该药品的方向性认可。
作为疫情中重症患者最有希望的药物,各方面开通绿色通道,大大加快了在美上市的进程,更快的验证结果和最短的时间过流程足以让药物走在新冠病毒之前!
期待瑞德西韦“高光时刻”
瑞德西韦从诞生至今不到10年,因疫情举世瞩目,并有可能迎来“高光时刻”。我们期待它在临床试验中能够发挥积极的作用,为全球抵抗新冠病毒作出贡献。
日前,Gilead表示:迄今为止,已为美国、欧洲和日本的数百名患者提供了同情用药。但由于需求过大,暂停受理大部分瑞德西韦同情用药的个人申请,将逐渐转为“扩展用药”,这样将加速重症患者获得瑞德西韦的机会,并能够收集所有参与患者的数据。目前正在与全球各国监管机构联合快速开发。
另外,为了满足可能出现的未来需求,Gilead已经扩大瑞德西韦的生产能力,并且将生产两种瑞德西韦的配方(液体和冻干)。
都是利好消息,期待瑞德西韦4月的最终临床结果!

责任编辑:杰尼龟
声明:本文系药智网整合内容,不代表本平台观点。如涉及作品内容、版权和其它问题,请与本公众号留言联系,我们将在第一时间删除内容。


研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






