小核酸药物「再次出发」
小核酸药物,是近年来新药研发的重要类型之一。虽然,其分支ASO、siRNA正处于高产出阶段,但仍存在一些技术问题无法解决。
有研究者将目光聚焦到激活机制的saRNA,以期寻求技术与领域的突破,并已有产品进入到临床开发。
小核酸药物「再次出发」。
01
saRNA发现历史&技术特点
最早提出激活RNA的概念,可追溯到上世纪60年代,有研究者认为存在一类只分布于细胞核的RNA,可与受体基因结合,形成序列特异性复合物并诱导相关基因转录对应的RNA。但在当时并未引起足够的重视。
2006年,科学研究发现在p21、VEGF等多个基因的一定距离的转录起始点启动子区域设计短双链RNA(dsRNA),可上调相应靶基因的表达,并将这种具有靶向激活靶基因的短核苷酸双链命名为saRNA。
saRNA,作为一类非编码RNA,结构类似于siRNA,但生物学功能完全相反。siRNA可以分别与AGO1、AGO2、AGO3和AGO4四种蛋白结合以获得活性,而saRNA只能被特异性地加载到AGO2蛋白行使功能。
目前接受程度较高的RNAa基因调控模型为:
1)外源性saRNA被加载到细胞质中的AGO2蛋白上;
2)AGO2蛋白通过切割和丢弃其中一条RNA链,形成一个活性的AGO2-RNA复合物,并进入细胞核;
3)AGO2-RNA复合物将结合到基因组DNA序列或DNA相连的反义转录本序列,进一步形成RNA诱导的转录激活复合物;
4)该复合物与hnRNPs、RNAPⅡ和各种转录因子结合,诱导靶基因表达。
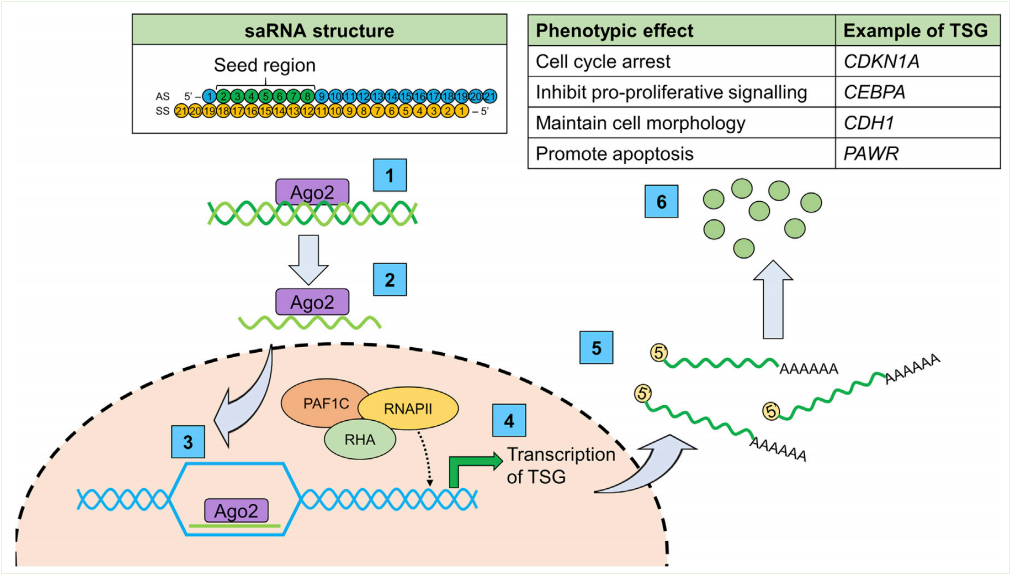
图1saRNA结构与作用机制
图片来源:MolecularTherapy:NucleicAcidsVol.31March2023
02
saRNA药物设计
相较于siRNA,saRNA技术的开发投入远不如siRNA广泛及具商业化特点的积累,目前有研究者提出如下序列设计原则:
1)目标序列从靶基因的正义链序列上筛选;
2)saRNA靶点选择在正义链转录起始位点上游-1200~-200bp的区域;
3)每个靶点长度的碱基数相对固定;
4)靶点碱基的GC含量在40%~65%范围内;
5)不能够出现连续4个以上相同的核苷酸;
6)第19个碱基是A;第18个碱基是A或T,最好是A;第七个碱基最好是T;第20-23个碱基最好是A或T;
7)选择目标序列时避开易受DNA甲基化影响的位点。
类似于siRNA,saRNA同样可能引发脱靶效应,即以序列特异性或非序列特异性的方式诱发非预期的基因活性。为了避免序列特异性脱靶反应,所设计的序列还应该进行序列BLAST以避免与人类基因组其他核苷酸序列有显著同源性。另外,saRNA结构的修饰被证明可以阻断脱靶效应,这部分的工作进行的相对广泛。
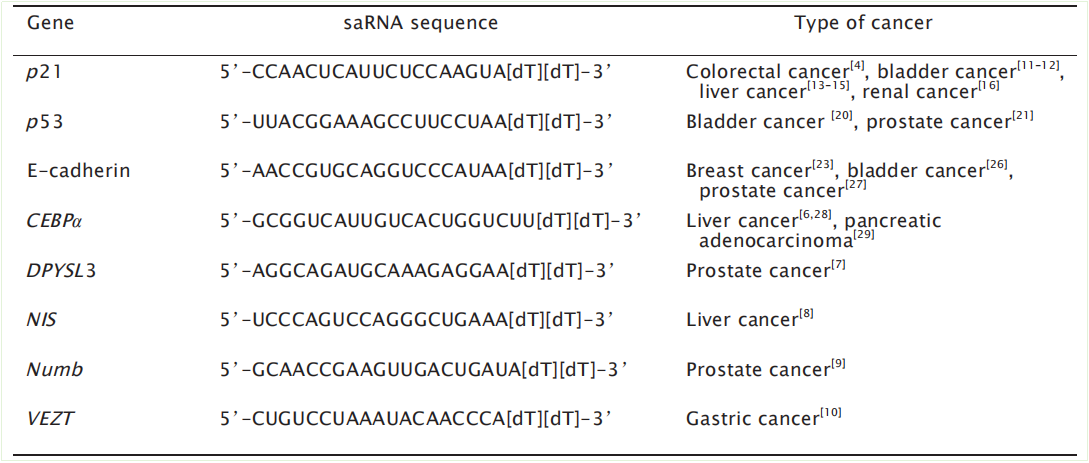
图2特异性上调抑癌基因表达的saRNA序列
图片来源:DOI:10.3781/j.issn.1000-7431.2019.55.495
03
saRNA抗肿瘤特点及主要品种
saRNA,通过作用于基因调控序列的特异位点,诱导基因转录,这已经得到学者们的普遍认同,并成为新的肿瘤研究热点。这一点不同于早期的siRNA,以及ASO类药物。
目前,技术较成熟的小核酸领域药物当属ASO和siRNA,但上述二者的获批适应症主要集中于遗传疾病、罕见病领域,众多已上市品种中,无肿瘤适应症获批。而saRNA开发的起点,即以肿瘤领域为主,这大不相同于“传统”小核酸药物,这也是其受关注的重点原因之一。如p21、p53等肿瘤领域著名靶基因及靶点,均为saRNA开发的方向内容。
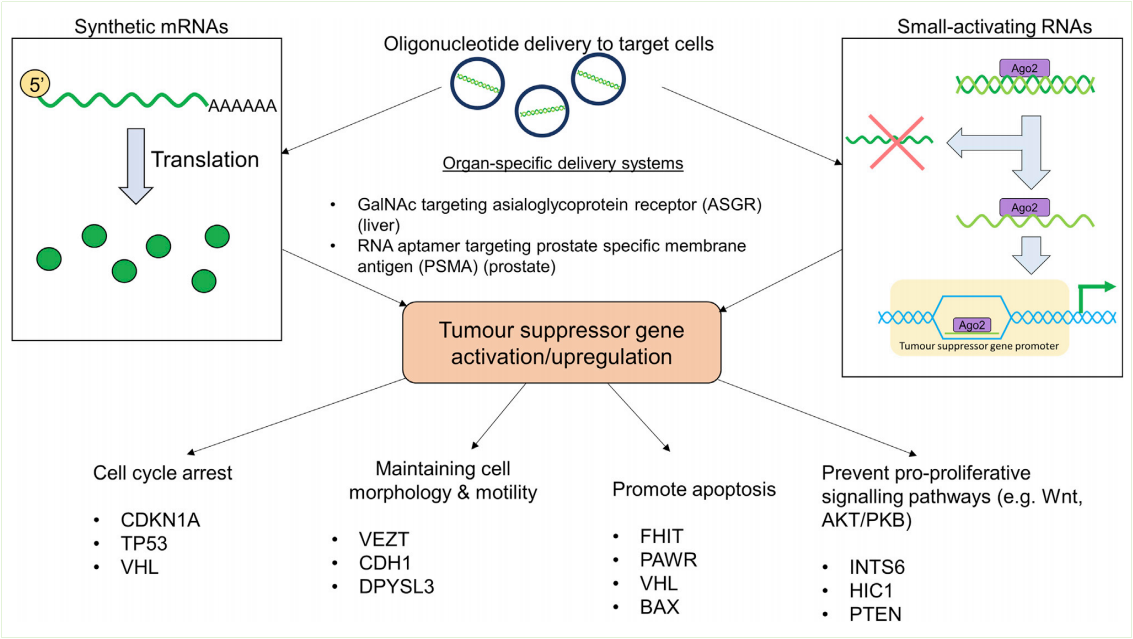
图3激活寡核苷酸靶向肿瘤抑癌基因
图片来源:MolecularTherapy:NucleicAcidsVol.31March2023
但由于saRNA药物开发仍处于早期阶段,目前进入临床的品种并不多。最具代表性的saRNA产品当属MTL-CEBPA,临床用于肝癌的治疗,目前最高临床阶段为II期。
据文献报道,CEBPA是一种转录因子,可调节肝脏稳态,CEBPA表达下调与多种致癌过程有关。研究者将小鼠结肠癌细胞系CT26注射到对抗PD-1治疗敏感的小鼠中用以构建小鼠结直肠癌模型,然后注射MTL-CEBPA和PD-1抑制剂。MTL-CEBPA或PD-1抑制剂单独处理的动物肿瘤体积差异并无统计学意义,而同时注射PD-1抑制剂和MTL-CEBPA组的肿瘤体积明显小于对照组,说明MTL-CEBPA和PD-1抑制剂具有协同作用,且同时注射PD-1抑制剂和MTL-CEBPA的肿瘤组织CEBPAmRNA表达量更高(8.69倍,P<0.0001)。
另,同样可重点关注的品种还有我国国内开发的RAG-01,处于临床I期,是一款首创作用机制的特异性靶向激活肿瘤抑制基因p21的双链saRNA药物,通过RNAa机制激活p21基因的表达,以抑制肿瘤细胞增殖、诱导细胞凋亡和衰老。临床前药效研究表明,通过开发公司的小核酸递送系统,RAG-01的治疗能够显著抑制动物模型中膀胱癌肿瘤的生长,并展示充分的安全性。

图4全球范围开发的saRNA相关肿瘤靶点进展(文献举例)
图片来源:MolecularTherapy:NucleicAcidsVol.31March2023
04
saRNA技术布局公司
当前,基于saRNA技术进入临床的产品极少,从而对应的开发公司也相对不多。
如上所述的MTL-CEBPA,原研单位为TheUniversityofTexasSouthwesternMedicalCenter,其在药物研发领域的布局较广,技术类型涉及小分子化药、aav产品、RNA产品等,疾病领域集中于肿瘤和神经系统。另,MiNATherapeutics公司的pipeline对MTL-CEBPA相关信息进行了重点介绍,具体如该品种的AACR年会公开信息、临床Ib期对实体瘤的联合治疗、单药用于肝癌治疗的I期临床等。
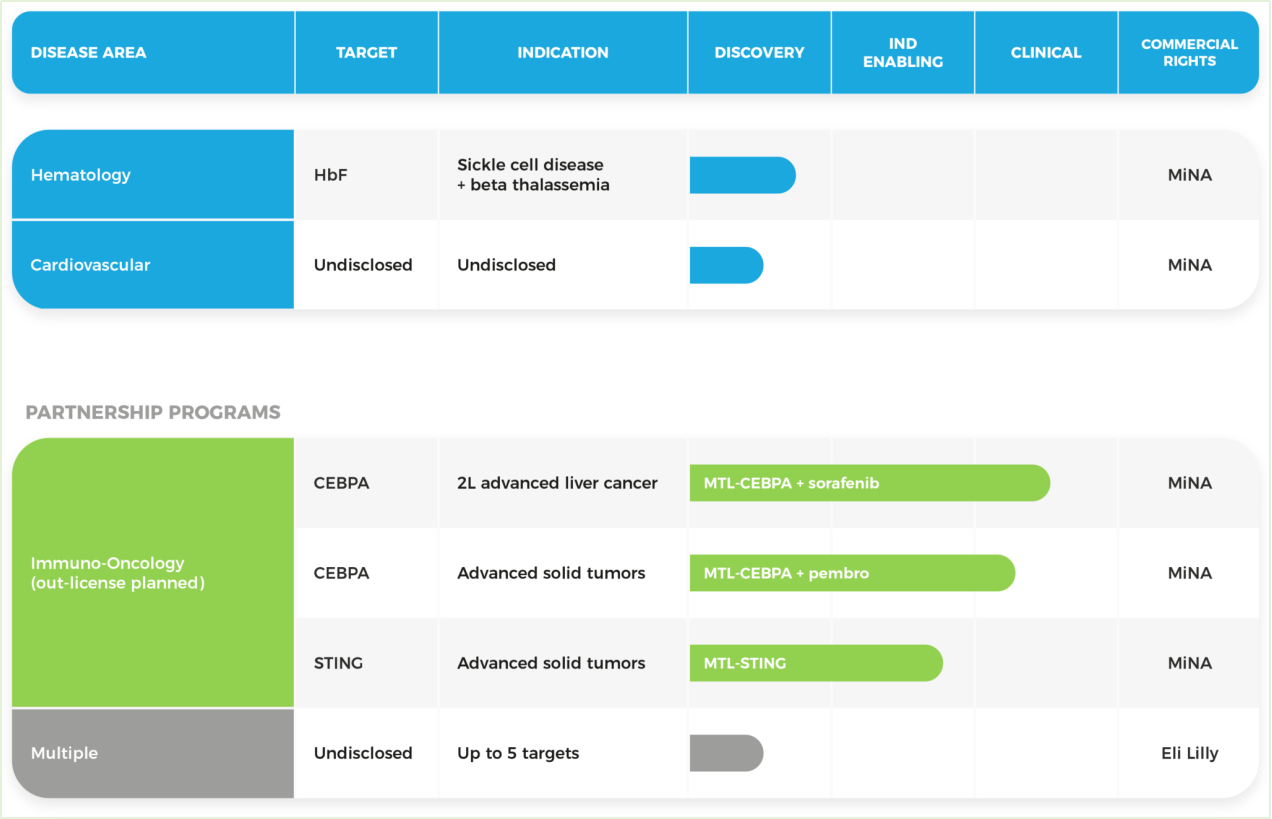
图5MiNATherapeutics聚焦的疾病领域与开发项目
图片来源:https://minatx.com/pipeline/#section_three
值得一提的是,RAG-01的开发公司中美瑞康,其技术重点布局于saRNA,在国内以及国外均处于领先地位。
其研发管线聚焦于目前尚无靶向治疗药物的疾病,包括单基因遗传病(例如基因突变导致的单倍体剂量不足)。对于这些疾病,RNA激活通过增强转录来补偿或消除基因活性的损失。借助于全球领先的SCAD™,LiCO™,和GLORY™递送平台技术,中美瑞康布局了多样化的管线项目,涵盖中枢神经系统、神经肌肉、眼科、肝脏和肿瘤等疾病治疗领域。

图6中美瑞康-pipeline
图片来源:https://cn.ractigen.com/pipeline/
05
结语
新技术的开发与推进,是新药领域前进的要素之一,saRNA无疑满足这一点,尤其是从基因治疗的角度来看。
RNA激活技术在存在较大潜力的同时,同样存在着诸多问题,如不成熟的激活序列筛选、稳定性较差的人工合成saRNA、目标基因的激活效果不佳、不同细胞调控方式的差异性、很难满足肿瘤组织长周期的抑制作用等等。
但上述存在的技术问题很难阻止saRNA的开发与发展,且已有显著的研究成果产生,并获得资本方的认可。未来几年,该领域很大可能会快速产出部分产品,但更期待的无疑是最终的临床数据。
参考资料:
1.中国血液流变学杂志.2022;32(1).doi:10.3969/j.issn.1009-881X.2022.01.035
2.MolecularTherapy:NucleicAcidsVol.31March2023.doi.org/10.1016/j.omtn.2022.12.016.
3.TUMORVol.39,January2019.DOI:10.3781/j.issn.1000-7431.2019.55.495
4.JournalofChineseOncology,2019,Vol.25,No.9.doi:10.11735/j.issn.1671-170X.2019.09.B012
5.https://cn.ractigen.com/about-us/
6.https://cn.ractigen.com/pipeline/

责任编辑:豌豆射手
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。

研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






