【好药记】两药品未通过,创一致性评价戏剧性一幕;两药品弯道超车,助力安必生成为首家持有药品上市许可的研发机构
一致性评价工作紧锣密鼓,截止7月19日,CDE受理一致性评价申请共计247个(按受理号计,下同),涉及到103个品种。本周(7月13日至7月19日)出现戏剧性一幕,白云山两药品想要弯道超车豁免BE试验过一致性评价,然CDE认为其资料不充分,不能豁免,未能通过一致性评价;此外也有好消息,扬子江药业、国药致君、乐普医疗和上海安必生制药的5个品种通过了一致性评价,值得提及的是,安必生此次有两个品种药品获得生产批文,除了是新4类仿制药申报弯道超车获得一致性评价名额外,还有一个亮点是安必生也因此成为国内首家药品研发机构持有药品上市许可的机构。
广州白云山两药品未通过一致性评价
7月16日,广州白云山发布了关于公司头孢氨苄胶囊和头孢拉定胶囊未通过药品一致性评价的公告说明。
公告指出:白云山制药总厂根据2017年8月25日国家食药监总局发布的《关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)》的相关要求,于2017年12月和2018年1月分别向国家食药监总局提交头孢氨苄胶囊和头孢拉定胶囊豁免人体生物等效性一致性评价的补充申请。然根据国家食药监总局药品审评中心审评报告,两个品种申请结论为“不予通过仿制药一致性评价申请”。主要原因系国家食品药品监督管理局药品审评中心认为白云山制药总厂提供的资料尚不能充分支持头孢氨苄胶囊和头孢拉定胶囊为BCS1类(即具有高溶解性、高渗透性),因此不批准上述产品基于BCS1类豁免人体生物等效性研究。
公告进一步指出:两产品未通过一致性评价并非因为质量与疗效不一致,而是因为申请豁免人体生物等效性研究的依据不充分。针对本次未通过一致性评价,公司积极采取行动补救,目前已安排相关研发工作,准备开展BE试验(人体生物等效性研究),重新提交一致性评价申请。
头孢氨苄胶囊
头孢氨苄属于第一代头孢类抗生素,用于治疗中耳炎、链球菌性咽炎、骨与关节感染、肺炎和尿路感染等细菌性感染;是首批“289”目录中的基药之一,同时也是中检院公布的参比制剂备案数目总排名第2的品种。其原研企业为日本盐野义,1971年在美国上市,1973年在日本上市,白云山制药总厂的头孢氨苄胶囊于1990年4月在国内获批上市。据Pharmarket数据,头孢氨苄制剂2017年全球销售额约为4.82亿美元,2017年白云山制药总厂销售收入为810.41万元,占公司2017年营业收入的0.04%。
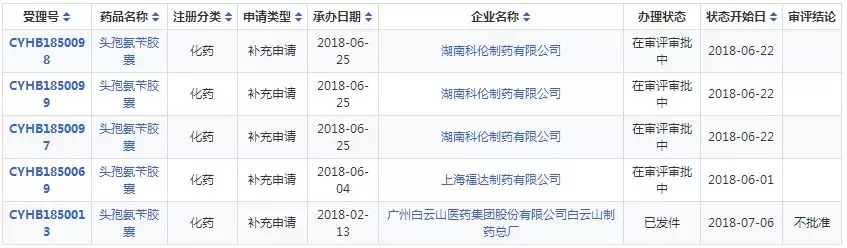
据药智数据,目前国内头孢氨苄胶囊的市场批文有349条,生产企业众多,申报一致性评价的企业有上海福达制药、广州白云山制药和湖南科伦制药,上海福达与湖南科伦的目前还在审评审批中,白云山面临重新提交,首家通过之争还在进行中。详情如下表一:
表一 头孢氨苄胶囊一致性评价申报详情
头孢拉定胶囊
头孢拉定是第一代头孢菌素,用于治疗敏感细菌所致的急性咽炎、扁桃体炎、中耳炎、支气管炎、肺炎等感染。原研企业为百时美施贵宝,1972年在爱尔兰上市,1982年在美国上市。1992年白云山制药总厂头孢拉定胶囊在国内获批上市。据Pharmarket数据,头孢拉定制剂2017年全球销售额约为0.73亿美元,2017年白云山制药总厂销售收入人民币918.16万元,占公司2017年度营业收入的0.04%。
据药智数据,目前头孢拉定胶囊国产市场批文有246条,申报一致性评价的仅白云山制药总厂,未通过一致性评价。
4药企的5品种通过一致性评价
国药致君的头孢呋辛酯片
7月17日,上海现代制药发布公告称其子公司国药集团致君(深圳)制药,收到国家药品监督管理局核准签发的头孢呋辛酯片(0.125g)《药品补充申请批件》,该药品通过仿制药质量和疗效一致性评价。
头孢呋辛酯片是国家基本药物第二代经典口服抗生素,适用于敏感细菌造成的感染治疗。因其强大的抗菌作用和安全性备受临床青睐,是20世纪90年代世界最畅销的抗感染药物之一。据悉,头孢呋辛酯片2017年在全球销售额为6.74亿美元,同比增长3.98%。2017年,国药致君头孢呋辛酯片(0.125g)销售收入约为7980万元。
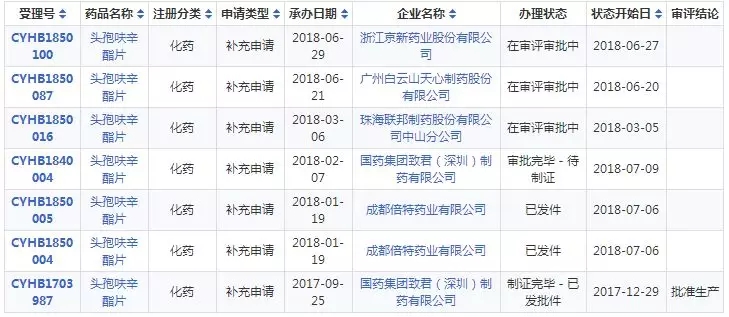
据药智数据,目前头孢呋辛酯片的国产批文有20条,申报一致性评价的企业有5家,其中成都倍特药业规格为0.25g和0.125g的头孢呋辛酯片已通过一致性评价,国药致君头孢呋辛酯片(0.25g)也已于2017年12月29日通过一致性评价,本次国药致君的头孢呋辛酯片(0.125g)通过一致性评价将进一步丰富公司产品规格,有利于该产品未来的市场销售和市场竞争,且将会对公司的经营业绩产生积极影响。
表二 头孢呋辛酯片一致性评价受理详情
乐普医疗的阿托伐他汀钙片
7月17日,乐普医疗发布公告称其子公司浙江新东港药业收到国家药品监督管理局核准签发的关于“阿托伐他汀钙片”的《药品补充申请批件》,该药品20mg和10mg规格均通过了仿制药质量和疗效一致性评价。
阿托伐他汀钙片作为心血管疾病治疗领域的第一大药,是血脂控制的基石用药,国内市场容量近160亿。原研辉瑞立普妥市场占有率近60%,市场高度集中和垄断。据悉,2017年前三季度立普妥的市场份额约占73.84%,阿乐紧跟其后,约占17.25%,其次为尤佳和优力平,市场份额为5.88%和1.47%。
据药智数据,目前阿托伐他汀钙片国产市场批文仅7条,涉及辉瑞中国、北京嘉林和浙江新东港药业。日前北京嘉林的“阿乐”(10mg、20mg)已通过一致性评价,此次新东港药业10mg和20mg剂型同时通过一致性评价,使得该公司具备了与原研和国内领先企业同在一个起跑线上重新出发的机会,并在20mg和10mg领域里同时抢夺立普妥和阿乐的存量市场。
扬子江药业的盐酸右美托咪定注射液
7月17日,扬子江药业发布公告称获得CFDA核准签发的新化3类药品“盐酸右美托咪定注射液”的生产批件。
根据总局2015年第230号文规定,新注册分类实施后申报并批准上市的仿制药将是按与原研药质量和疗效一致的原则进行受理和审评审批。意味着扬子江药业获批的“盐酸右美托咪定注射液”首家通过一致性评价,并进入《中国上市药品目录集》。
盐酸右美托咪定注射液是一种相对选择性α2-肾上腺素拮抗剂,适用于外科手术和其他手术之前或手术期间非插管患者的镇静。由Orion公司和雅培开发,1999年在美国获批上市,2009年江苏恒瑞作为首仿企业批准在中国上市,根据中国IQVIA数据库显示,2017年中国麻醉剂市场容量约118亿,其中右美托咪定占整个麻醉剂市场的15.49%,2017年国内销售超过18亿元。
据药智数据盐酸右美托咪定注射液的国产市场批文有12条,生产企业有江苏恒瑞、湖南科伦、四川国瑞药业等,其中申报注册一致性评价的企业仅江苏恒瑞,且已于6月4日获得承办。此次扬子江药业弯道超车,首家通过一致性评价,抢占右美托咪定麻醉市场更大份额的同时完善了企业的产品管线,为进一步进军麻醉药品市场奠定有力基础。
上海安必生制药的孟鲁司特钠咀嚼片和普通片
近日,上海安必生制药和杭州民生滨江制药联合申报的新4类药--孟鲁司特钠咀嚼片和普通片获得国家药品监管局批准。根据一致性评价相关政策,孟鲁司特钠咀嚼片和普通片也成为第一个通过仿制药一致性评价的同类药品;同时孟鲁司特钠两个制剂品种在我国上市销售后,将成为第一个在中国和美国两个市场同时上市的孟鲁司特钠咀嚼片和普通片,其与美国市场销售的孟鲁司特咀嚼片和普通片为共线生产,生产线和配方工艺等完全相同,质量疗效完全相同。
孟鲁司特钠是一种白三烯受体拮抗剂,用于治疗和预防儿童和成人哮喘,也可治疗过敏性鼻炎。由默沙东开发,1998年在美国上市,1999年进入中国市场,据悉,孟鲁司特钠2017年国内医院销售额超过16亿元,原研品市场份额超70%。
据药智数据,目前孟鲁司特钠国产市场批文仅9条,生产企业较少,主要生产企业为四川大冢制药、鲁南贝特制药,还没有企业申报注册一致性评价,此次上海安必生制药的孟鲁司特钠咀嚼片和普通片首家通过一致性评价,将逐鹿原研。
此外此次安必生获得孟鲁司特钠咀嚼片和普通片的生产批文也使得上海安必生成为国内首家药品研发机构持有药品上市许可的机构。近两年,国家大力推行药物MAH试点,安必生的成功,产品上市时间得到提速是MAH试点工作推行的可喜案例。
一药品一致性评价获承办
哈药蒙脱石散
7月16日,哈药集团中二厂的一致性评价获CDE承办。
蒙脱石散由益普生药业研发,于1980年3月在法国上市。蒙脱石散在国内临床适应症为:成人及儿童急、慢性腹泻。用于食道、胃、十二指肠疾病引起的相关疼痛症状的辅助治疗。据悉,2017年蒙脱石散医院终端销售额接近四亿元,药店终端销售额接近五亿元,同比增长18.25%。2017年两大终端市场销售额接近9亿元。
据药智数据,目前蒙脱石散国内市场生产批文有31条,生产企业众多。其中申报一致性评价的目前已达6家,其中四川维奥制药和先声药业已经相继通过一致性评价,可见蒙脱石散竞争激烈。详情如下表所示:
表三 蒙脱石散一致性评价受理详情
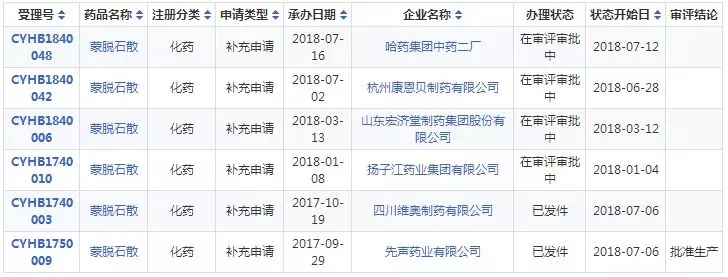
数据来源:药智数据
信息来源:药智网、赛柏蓝、研如玉及相关企业公告等
【好药记】专栏为您追踪一周一致性评价最新动态!请关注药智网微信服务号yaozh_service(15696212300)

研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






