51款国产化药1类新药获受理!c-MET抑制剂再传佳音,人福药业、浦润奥、以岭…
看点:
9月药审中心受理总量为1189个(不计复审)
9月51个国产化药1类新药品种获CDE受理
9月新增68个按仿制药质量和疗效一致性评价申报的受理号
武汉光谷人福1类中药创新药广金钱草总黄酮胶囊获批上市
根据药智数据最新统计(数据统计截止2022年9月29日,下同),2022年9月份CDE共承办新的药品注册申请以受理号计有1189个(复审除外,下同)其中化药受理865个,中药受理149个,生物制品受理174个,体外诊断试剂1个;2022年4-9月各类药品注册申请受理情况详见图一。
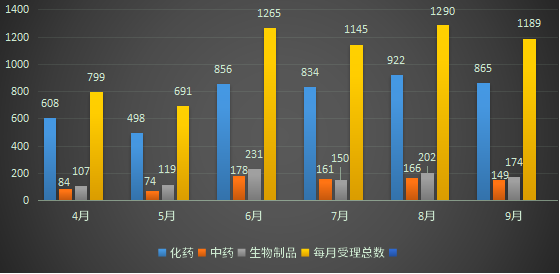
图一 2022年4-9月CDE药品受理情况
数据来源:药智数据、药智咨询整理
2022年9月份(注:状态开始时间(药智)从2021年9月1日至2021年9月29日)完成审评的受理号共998个,其中化药受理671个,中药受理160个,生物制品受理167个;2022年4-9月各类药品完成审评情况详见图二。
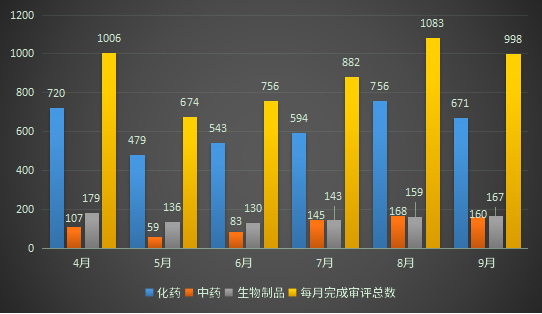
图二 2022年4-9月CDE药品完成审评情况
数据来源:药智数据、药智咨询整理
以下且看化药、中药、生物制品的注册受理及审评情况详细分析。
一、化药申报与审评情况
(一)化药受理情况
9月份CDE承办新的化药注册申请865个(以受理号计),其中新药申请受理号102个,进口受理号81个,仿制申请受理号236个,补充申请416个,进口再注册30个;
以审评任务类别统计(以受理号计),IND申请116个,ANDA申请207个,NDA申请20个,进口再注册申请26个;2022年4-9月CDE化药各审评任务类别申请受理情况详见图三。
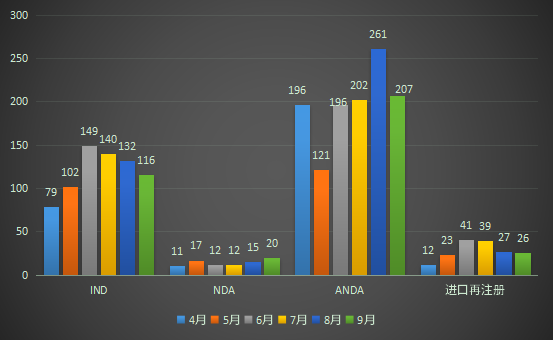
图三 2022年4-9月CDE化药各审评任务类别申请受理情况
数据来源:药智数据、药智咨询整理
1.化药1类国产申报情况
9月CDE受理化药国产1类新药共计92个(按受理号计),其中IND申请90个,NDA申请2个,涉及51个品种(按药品+企业维度统计),当前大部分受理号已进入对应的审评序列排队待审评;下表为9月新承办的1类国产新药。
表一 2022年9月新承办的化药1类国产新药
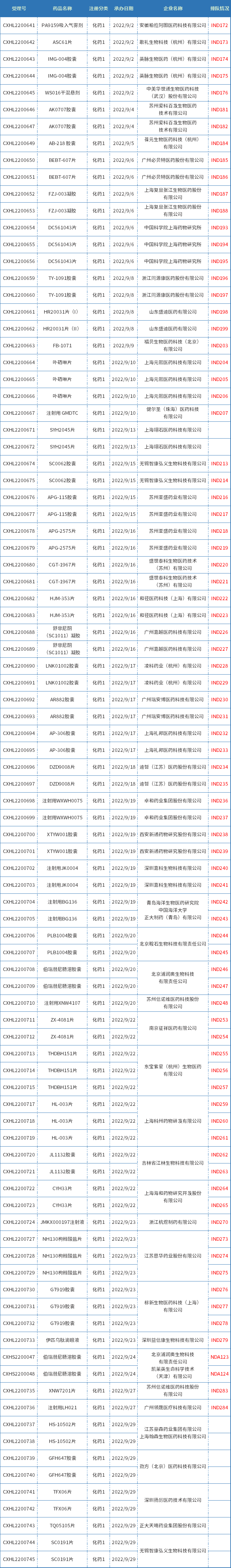
注:排队序号截止至2022年09月29日。
2.化药1类进口药品申报情况
9月共18个进口化药1类受理号获得承办,其中是IND申请17个,NDA申请1个,共11个品种,目前,均已进入相应序列排队待审;下表为9月新承办的1类进口新药。
表二 2022年9月新承办的化药1类进口新药
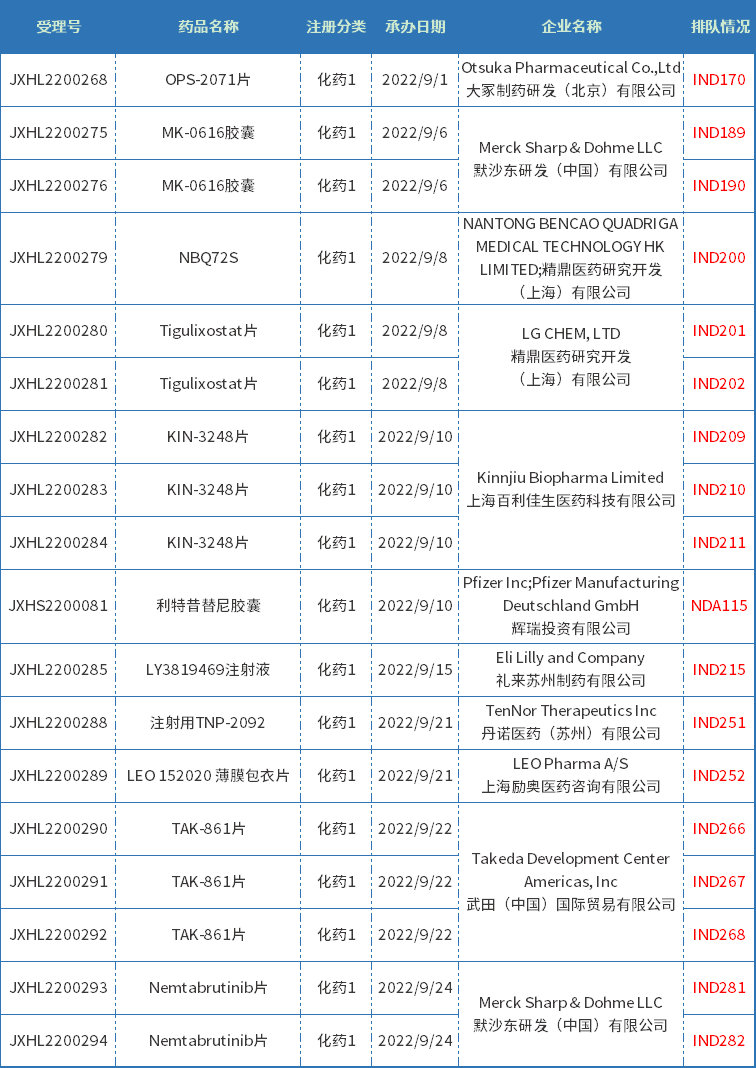
注:排队序号截止至2022年09月29日
伯瑞替尼肠溶胶囊
伯瑞替尼是一款有效的高选择性 c-MET 抑制剂,于2014年在国内首次申请临床试验,于2021年2月纳入突破性治疗程序,目前浦润奥伯瑞替尼肠溶胶囊上市申请已获CDE受理,适应症为:用于具有间质-上皮转化因子(MET)外显子 14 跳变的局部晚期或转移性非小细胞肺癌成人患者。
利特昔替尼胶囊
利特昔替尼是一种口服靶向JAK3抑制剂,与第一代泛JAK抑制剂相比,利特昔替尼在降低毒性方面更有优势。目前辉瑞利特昔替尼胶囊新药上市申请已获CDE受理,适应症为:用于治疗12岁及以上青少年和成人斑秃。
ASC61片
ASC61是一款口服PD-L1小分子抑制剂前药。2022年8月,歌礼宣布其治疗晚期实体瘤的美国I期临床试验完成首例患者给药。
FB-1071
FB-1071是福贝生物通过内部研发和授权引进相结合的方式打造了一条原创新药的产品管线。FB-1071可以高亲和力和选择性地抑制和杀伤神经系统中的小胶质细胞,有效地阻断驱动疾病发展的神经炎症反应,减缓神经损伤,帮助神经细胞修复。
THDBH151片
THDBH151是一款XO/Urat1双靶点抑制剂用于治疗痛风的药物,是通化东宝在研1类创新药。THDBH151片通过平衡好XO/Urat1在降尿酸中的作用,在提高药效的同时也降低副作用,大幅提高患者依从性,有望成为同领域中Best-in-Class药物。
3.化药改良型新药申报情况
9月新增化药2类改良型新药20个(按受理号计),其中IND申请17个,NDA申请3个,共涉及15个品种;2022年1-9月CDE化药改良型新药申请受理情况详见图四。
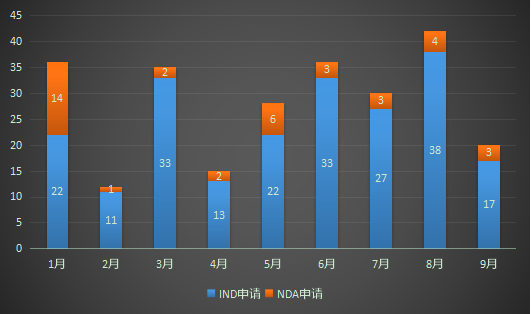
图四 2022年1-9月CDE化药改良型新药申请受理情况
数据来源:药智数据、药智咨询整理
(二)化药完成审评情况
9月份CDE完成审评的化药注册申请671个(以受理号计),其中新药申请受理号93个,进口受理号92个,仿制申请受理号105个,补充申请358个;以审评任务类别统计(以受理号计),IND申请143个,ANDA申请106个,NDA申请6个,进口再注册申请23个,一致性评价82个;2022年9月CDE化药各审评任务类别完成审评情况详见图五;

图五 2022年9月CDE化药各审评任务类别完成审评情况
数据来源:药智数据、药智咨询整理
以受理号审评结论来看,其中批准临床 188个,批准生产 76个,批准进口 8个,未被批准51个;2022年9月CDE化药化药完成审评结论情况详见图六;
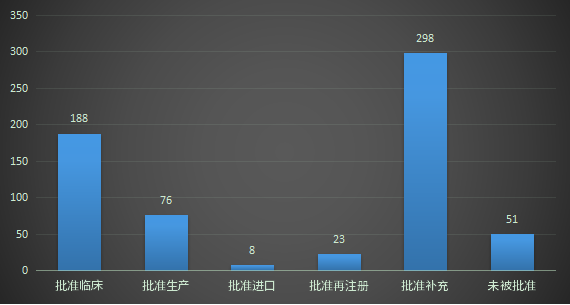
图六 2022年9月CDE化药化药完成审评结论情况
数据来源:药智数据、药智咨询整理
1.化药新药获批情况
9月共4个新药批准上市,其中3个2类改良型新药和1个进口原研;下表为9月化药批准上市新药信息。
表三 2022年9月化药获批新药信息
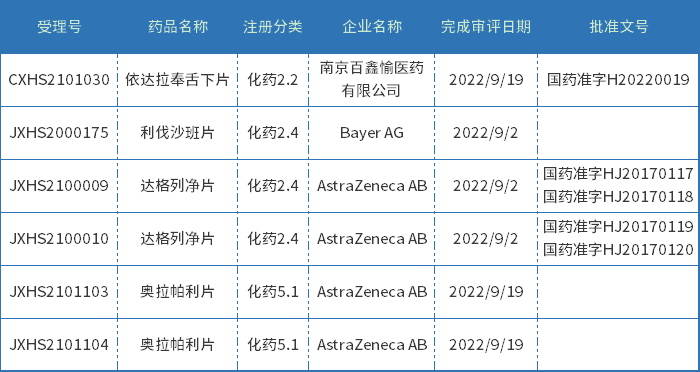
依达拉奉舌下片
依达拉奉舌下片是南京百鑫愉医药有限公司和北京天坛医院共同开发、具有独立自主知识产权的2.2类改良型新药,用于抑制肌萎缩侧索硬化所致功能障碍的进展,是全球首个渐冻症舌下给药上市药物。
2.化药仿制药获批情况
9月共62个化药仿制药批准上市,其中注册分类为3类的20个,注册分类4类的41个和注册分类5.2类的1个;ATC分类主要包括:系统用抗感染药、消化道及代谢、神经系统和心血管系统等;2022年9月获批化药仿制药ATC分类详见图七;9月获批化药仿制药信息情况见表四;
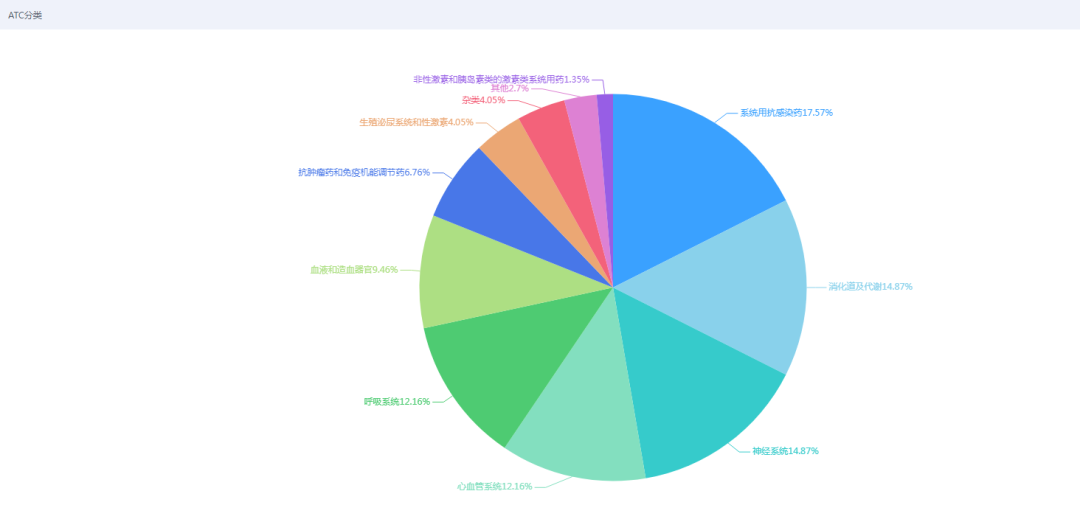
图七 2022年9月获批化药仿制药ATC分类(来源于药智数据)
数据来源:药智数据、药智咨询整理
表四 2022年9月获批化药仿制药信息

注:数据统计截止至2022年09月29日
二、中药申报与审评情况
(一)中药受理情况
9月份CDE承办的中药注册申请受理号共计149个,其中新药8个,补充申请141个;2022年4-9月CDE中药各申请类型受理情况详见图八。
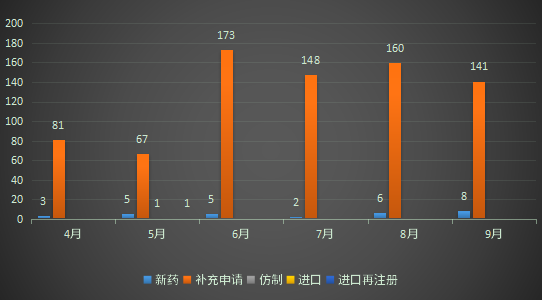
图八 2022年4-9月CDE中药各申请类型受理情况
数据来源:药智数据、药智咨询整理
1.中药新药申报情况
9月共承办6个中药1类创新药和2个中药2类改良型新药,共涉及7个品种,其中是IND申请4个,NDA申请4个;下表为9月新承办的中药新药。
表五 2022年9月新承办的中药新药
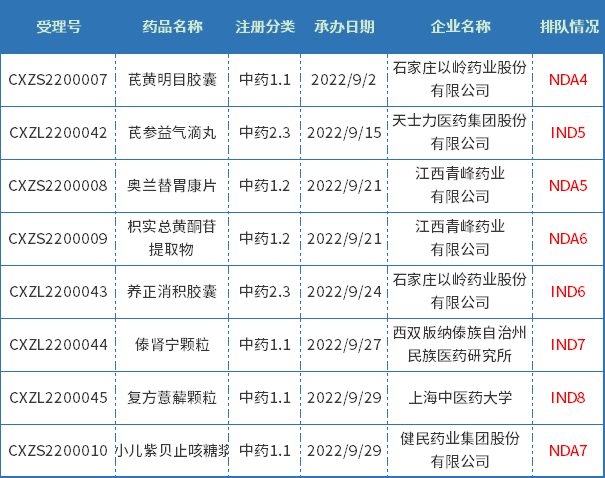
注:排队序号截止至2022年09月29日
(二)中药完成审评情况
9月份CDE完成审评的化药注册申请160个(以受理号计),其中新药受理号7个,补充申请153个;以审评任务类别统计(以受理号计),IND申请5个,NDA申请2个,补充申请153个。
1.中药新药获批情况
9月共1个中药创新药获批上市,为武汉光谷人福的广金钱草总黄酮胶囊;下表为9月批准上市新药信息。
表六 2022年9月获批中药新药信息

广金钱草总黄酮胶囊
广金钱草总黄酮胶囊是武汉光谷人福生物医药有限公司自主研发的1类创新药,主要采用现代化工艺从广金钱草单味药材中分离纯化广金钱草总黄酮有效部位,并以该有效部位组方,研制开发成现代中药创新制剂,产品用于输尿管结石中医辨证属湿热蕴结证者,功能主治为清热祛湿、利尿排石。
三、生物制品审评情况
(一)生物制品受理情况
9月份CDE承办新的生物制品注册申请受理号共计174个,新药69个,补充申请61个,进口40个(其中包括一次性进口16个),进口再注册4个;2022年4-9月CDE生物制品各申请类型受理情况详见图九。

图九 2022年4-9月CDE生物制品各申请类型受理情况
数据来源:药智数据、药智咨询整理
1.生物制品1类新药申报情况
9月有58个1类治疗用生物制品受理号获得承办,其中均是临床试验申请,目前都已经进入相应序列排队待审;下表为9月新承办的治疗用生物制品1类创新药。
表七 2022年9月新承办的治疗用生物制品1类新药

注:排队序号截止至2022年09月29日。
(二)生物制品完成审评情况
9月份CDE完成审评的生物制品注册申请167个(以受理号计),其中新药申请受理号45个,进口受理号37个,补充申请83个;以审评任务类别统计(以受理号计),临床试验申请71个,上市申请7个,补充申请83个;2022年9月CDE生物制品各审评任务类别完成审评情况详见图十;
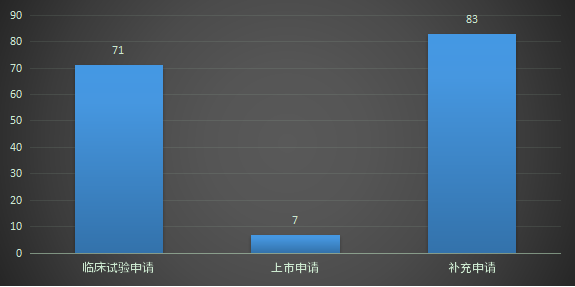
图十 2022年9月CDE生物制品各审评任务类别完成审评情况
数据来源:药智数据、药智咨询整理
1.生物制品获批情况
9月共4个生物制品获批上市;下表为9月获批生物制品信息。
表八 2022年9月获批生物制品信息
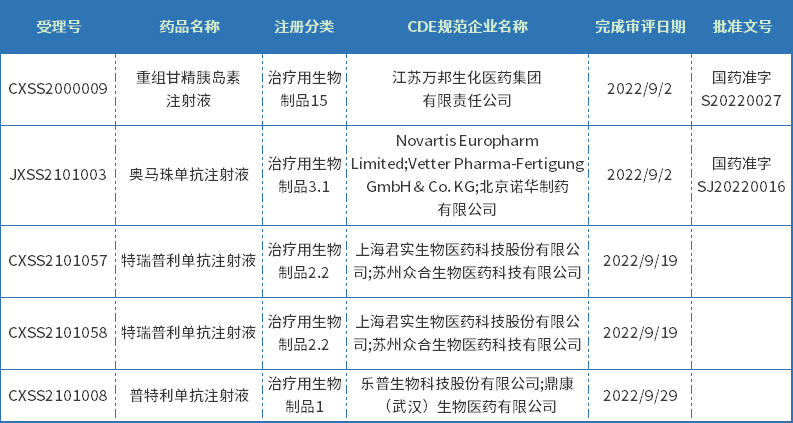
注:数据统计截止至2022年09月29日。
四、按一致性评价申报品种情况
9月新增68个按一致性评价要求进行申报的受理号和263个视同受理号。(篇幅限制仅展示一致性信息,视同及具体信息请关注药智企业版药品注册与受理数据库);2022年1-9月一致性评价受理数量详见图十一;表九为9月新增一致性评价受理号信息。
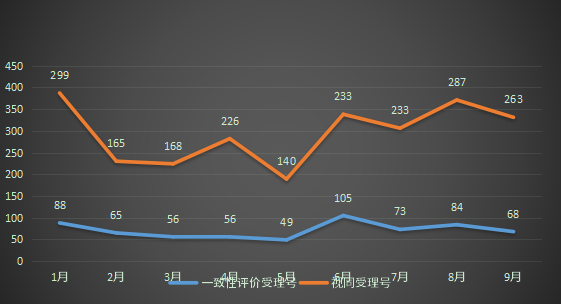
图十一 2022年1-9月一致性评价受理数量
数据来源:药智数据、药智咨询整理
表九 2022年9月新增一致性评价受理数据

数据来源:药智药品注册与受理数据库

责任编辑:琉璃
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。

• 51款国产化药1类新药获受理!c-MET抑制剂再传佳音,人福药业、浦润奥、以岭…
• 31款国产化药1类新药获受理,多款PD-1申报新适应症!复宏汉霖、百济神州、罗氏…
• 37款国产化药1类新药获受理,恒瑞医药镇痛新药报产!京新药业、真实生物…
• 13款1类创新药获批上市!优先审评、突破性疗法数量大增,复宏汉霖、恒瑞、康方…
• 4款国产1类新药报上市!超20款改良型新药获受理,豪森药业、正大天晴、兴盟生物…
• 25款化药1类新药获受理!生物创新药申报放缓,京新药业、康缘药业、科伦…
• 32款化药1类新药获受理,2类改良型新药申报量大增!复星医药、百济神州、好医生…
• 53款国产1类新药申报临床,3款国产1类新药申报上市!亿一生物、四环制药、石药…
• 2021年1类新药申报临床数量再创新高!恒瑞位居第一,豪森、广东东阳光药…
• 深度盘点:江苏药品申报总量全国领先!18款1类创新药获批上市,恒瑞、豪森、百济…
研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






