糖尿病治疗添新武器!华领医药全球首创新药多扎格列艾汀获《药品生产许可证》
今日,华领医药宣布,经过药品上市许可持有人(MAH)体系审核和现场核查后,公司已获得由上海市药品监督管理局颁发的在研全球首创新药多扎格列艾汀(dorzagliatin)《药品生产许可证》。
多扎格列艾汀是一款在研的全球首创双作用的葡萄糖激酶激活剂,旨在通过恢复2型糖尿病患者的血糖稳态来控制糖尿病渐进性退变性疾病发展。通过修复葡萄糖激酶的葡萄糖传感器功能的缺陷,dorzagliatin 具有恢复2型糖尿病患者受损的血糖稳态的潜力,可作为该疾病的一线治疗标准,或作为与目前批准的抗糖尿病药物联合使用的基础治疗。
据悉,今年以来,华领医药成功完成两项III期新药上市注册临床试验的关键里程碑,其中包括在未用药2型糖尿病患者中开展的多扎格列艾汀单药治疗III期临床试验SEED(HMM0301),和在二甲双胍足量治疗失效的2型糖尿病患者中开展的二甲双胍联合用药临床试验DAWN(HMM0302)。临床研究数据表明,在相应治疗周期内,多扎格列艾汀展现出了显著稳定疗效和安全性,并具有改善胰岛β细胞功能、促进胰岛素早相分泌和降低胰岛素抵抗的效果,有望从根本上治疗糖尿病。
据药智数据,多扎格列艾汀在国内共登记了11项临床试验,其中2项目前已完成三期临床试验,另据其企业公告显示其在美国在同步进行多项早期临床试验,用以治疗成人2型糖尿病。
华领医药多扎格列艾汀国内临床试验项目详情表
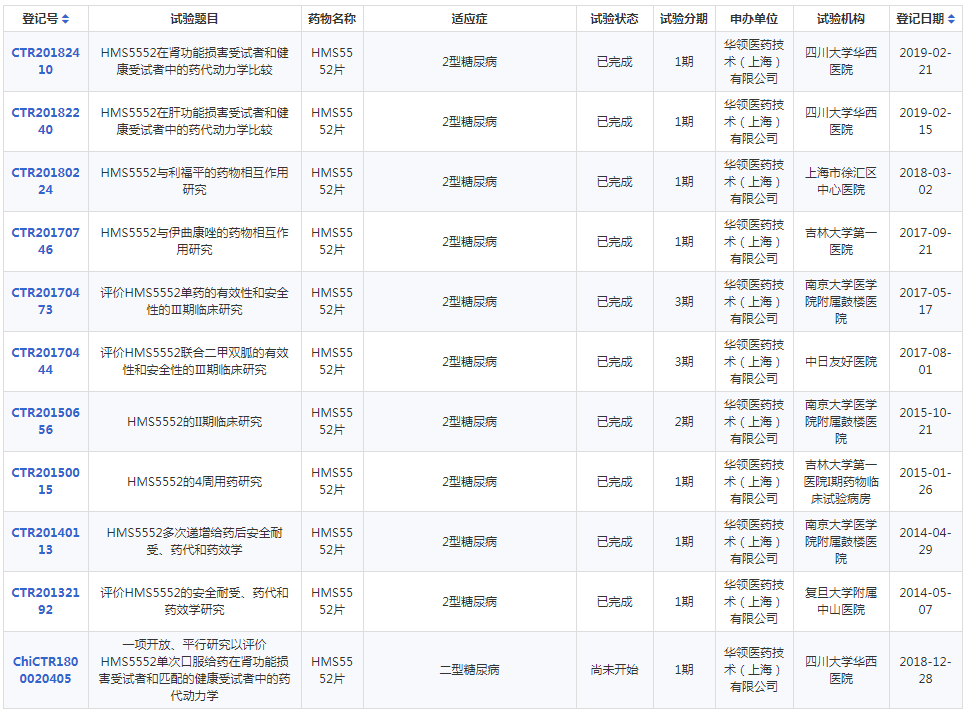
数据来源:药智中国临床试验数据库
此外,已有多扎格列艾汀药品注册受理号8条,先后多个受理号被纳入特殊审评,以及被列入重大专项品种之列。
多扎格列艾汀申报注册详情表
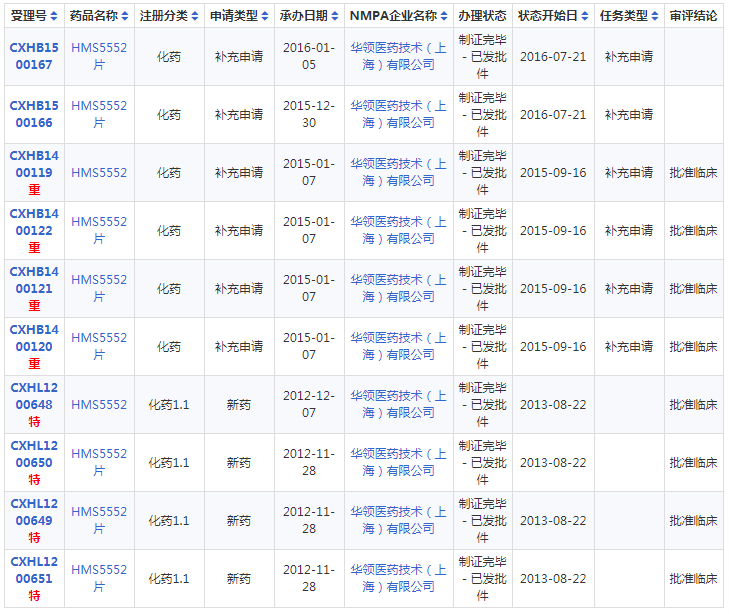
数据来源:药智药品注册与受理数据库
此外,8月17日,华领医药与拜耳宣布建立战略合作,就多扎格列艾汀在中国达成商业合作协议。华领将负责产品的临床开发、生产供应、一级商分销、注册和药物警戒等工作;拜耳作为多扎格列艾汀中国独家推销商,负责其在中国的市场营销、推广和医学教育等活动,华领医药因此获得3亿元人民币首付款,还将获得最高41.8亿元的里程碑付款。获批《药品生产许可证》将进一步加速华领医药的新药上市申请(NDA)进程,为上市后药品的商业化生产供应做好了准备,并为未来产能的逐步提升打下了坚实的基础。
公开数据显示,全球20-79岁成年人当中,已有2型糖尿病(T2DM)患者4亿6300万人,中国糖尿病患者已经增长到1.4亿,以目前的发病趋势,2045年全球T2DM成年患者将突破7亿,增长率51%。目前,中国糖尿病发病率12.8%,每8个中国人里就有1名患者;糖尿病前期人群则占35.2%,大约每3人当中就有1人处于糖尿病前期。近年来虽然上市了多个不同作用机制的降糖药,但是患者总体血糖达标率仍然不到50%,现华领医药的多扎格列艾汀获批生产,多扎格列艾汀通过修复患者体内受损的葡萄糖激酶(GK)使患者恢复自身的生理调糖功能。葡萄糖激酶(GK)是人体内的血糖传感器,在维持人体血糖稳态方面起着核心的作用。或将具有从根本上解决糖尿病患者血糖失稳态的潜力。

责任编辑:三七
声明:本文系药智网整理内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!

研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






