看这里!海外糖尿病药物销售Number 1利拉鲁肽药物研究报告
导读:盘踞海外糖尿病药物销售Number1(2018年全球销售额44.68亿美元)的利拉鲁肽专利期早已过期,国产仿制药迟迟没有迎来上市喜讯,那么该药品目前的整体研究情况究竟怎样?且随小编一起看本期的利拉鲁肽的药物研究报告。
目录
摘要信息
药物概述
API信息
药理作用
美国上市情况(2条)
欧盟上市情况(2条)
日本上市情况(3条)
中国上市情况(3条)
中国注册申报情况(43条)
药品说明书(25条)
全球临床试验情况(358条)
美国专利状态(60条)
国内专利状态(14)
世界专利状态(2118)
更多详细信息
利拉鲁肽由诺和诺德(NovoNordisk)研发,于2009年6月30日获得欧洲药物管理局(EMA)批准,2010年1月20日获得日本医药品医疗器械综合机构(PMDA)批准,2010年1月25日获得美国食品药品管理局(FDA)批准,2011年3月4日获得中国食品药品监督管理局(CFDA)批准上市,并由诺和诺德在美国、欧洲、日本和中国市场销售,商品名为Victoza和Saxenda。
摘要信息

药物概述
利拉鲁肽是一种胰高血糖素样肽-1(GLP-1)受体激动剂,能激活细胞表面GLP-1受体,通过活化G蛋白发挥腺苷环化酶活性。
该药用于治疗2型糖尿病和肥胖症。Victoza是一种皮下注射液,每只注射笔含0.6mg、1.2mg或1.8mg利拉鲁肽。推荐剂量为每日0.6mg,用药一个周后将剂量变更为每日1.2mg。Saxenda是一种皮下注射液,每只注射笔含0.6mg、1.2mg、1.8mg、2.4mg或3mg利拉鲁肽。推荐的初始剂量为每日0.6mg,用药一周后,可每周增加0.6mg,直至增加到每日3mg。
API信息
结构式:
化学名称:N26-(hexadecanoyl-γ-glutamyle)-[34-arginine]GLP-1-(7-37)-peptide
CAS登记号:204656-20-2
分子式:C172H265N43O51
分子量:3751.23
药理作用
ATC分类:A10BX07消化道及代谢>糖尿病用药>非胰岛素类降血糖药>其它非胰岛素类降血糖药
作用靶点:GLP-1receptor
美国上市情况
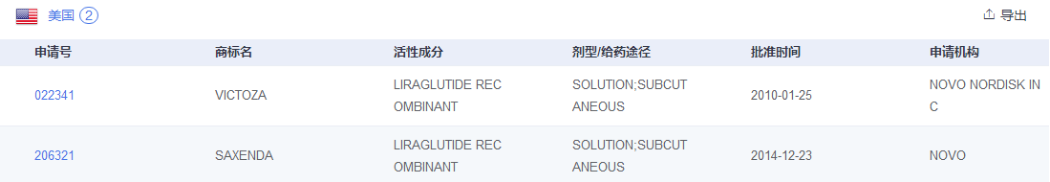
欧盟上市情况

日本上市情况

中国上市情况

中国注册申报情况
据药智药品注册与受理数据库显示,截止目前CDE共计受理43个利拉鲁肽注册受理号,其中注射剂34个,原料药9个。
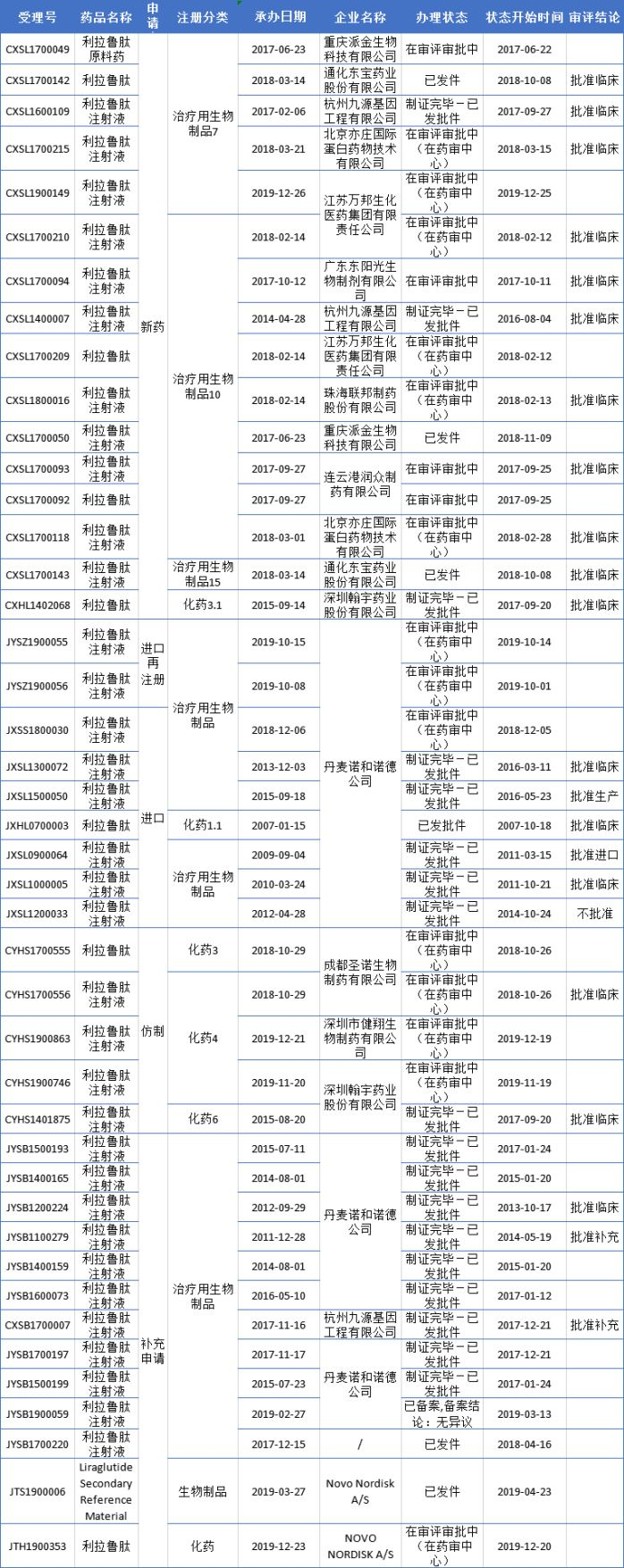
药品说明书
药智数据企业版药物数据库显示,目前全球利拉鲁肽共有25条说明书。

注:如需下载,点击文末链接,进入药智数据,在药物报告处进行说明书下载。
全球临床试验情况

注:因数据较多,此处只列举招募状态为Recruiting、研究阶段为Phase4的数据,详情点击文末链接,进入药智数据-药物报告进行查看。
美国专利状态

国内专利状态

世界专利状态

更多详细信息

数据来源:药智数据企业版药物数据库
因报告全文篇幅较大,文章只展示部分内容。如需获取详细资料,可进入药智数据企业版药物数据库https://vip.yaozh.com/report?ga_source=vip&ga_name=topnav直接查看。

责任编辑:萌萌
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。

研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






