NMIBC市场亟待破局
近日(5月3日),CGOncology宣布,其在研溶瘤病毒疗法cretostimogene(CG0070)单药在治疗对卡介苗治疗无应答、高危非肌层浸润性膀胱癌(NMIBC)患者的有效性和安全性III期研究数据显示,75.2%的患者实现了完全缓解(CR),29例患者维持完全缓解超过12个月。与NMIBC历史数据相比,该数据非常靓眼。
乐普生物拥有CG0070在中国区的开发、制造及商业化的权益。凭借优异的临床数据,自2024年3月底至今,公司股价已实现翻倍。
非肌层浸润性膀胱癌新发人数多,且缺少有效的治疗方案,晚期尿路上皮癌患者行根治性膀胱切除术后面临永久佩戴集尿袋的窘境,这一市场存在巨大未满足的临床需求。
存在巨大未满足的临床需求
膀胱癌新发人数多,临床治疗迫切性强。膀胱癌是一种发生在膀胱内的恶性肿瘤,是全球发病率排名第十三的常见癌症,高发年龄为50-70岁,男性尿路上皮癌的发病率为女性的3-4倍。2020年,我国膀胱尿路上皮癌新发病例约7.7万人,预计到2025年将达到9.1万人,到2030年将达到10.6万人。晚期膀胱癌患者生活质量较差,行根治性膀胱切除术后患者须在腹壁做造口,永久佩戴集尿袋,对正常的生活造成巨大的影响。鉴于膀胱癌发病人数多,且仍存在巨大未满足的临床需求,新药的研发可谓迫在眉睫。
膀胱癌分为非肌层浸润性膀胱癌(NMIBC)和肌层浸润性膀胱癌(MIBC)两大类。非肌层浸润性膀胱癌包括膀胱的原位癌(Tis)、非浸润性乳头状癌(Ta),以及侵犯上皮下结缔组织的膀胱癌(T1),其中Ta占70%,T1占20%,Tis占10%。肌层浸润性膀胱癌是指侵犯浅肌层以上的膀胱癌。
NMIBC的常规治疗是经尿道膀胱肿瘤切除术(TURBT),TURBT通过一个带有电切环和摄像头的器械,将膀胱内的肿瘤切除并送检。但由于NMIBC容易复发和进展,因此需要在术后使用辅助药物治疗。
目前,最有效的辅助药物治疗为化疗及卡介苗(BCG)膀胱灌注。化疗包括术后即刻膀胱灌注化疗和术后维持膀胱化疗,尤其是对于中危及高危NMIBC患者,术后即刻灌注化疗后需要维持灌注化疗或BCG灌注治疗以降低肿瘤复发率。卡介苗灌注为将一种弱化的结核杆菌制剂注入膀胱内,刺激免疫系统对抗肿瘤细胞。但无论是化疗及卡介苗膀胱灌注,50%的患者均会在5年内发生肿瘤复发,肿瘤复发后患者的标准疗法是根治性膀胱切除术,根治性膀胱切除术使患者失去正常的储尿和排尿功能,严重影响患者的生活质量和心理健康。因此,对于化疗和BCG无应答NMIBC患者而言,新药的研发十分关键。
二线疗法覆盖人群有限
目前,全球仅批准三款可用于非肌层浸润性膀胱癌的二线疗法,分别是默沙东的K药、FerringPharmaceuticals的Adstiladrin和ImmunityBio的N-803。其中,K药和Adstiladrin获批的适应症仅限于原位癌(CIS),但原位癌在NMIBC中占比仅10%,N-803于2024年4月上市,上市可谓一波三折。
表1:NMIBC竞争格局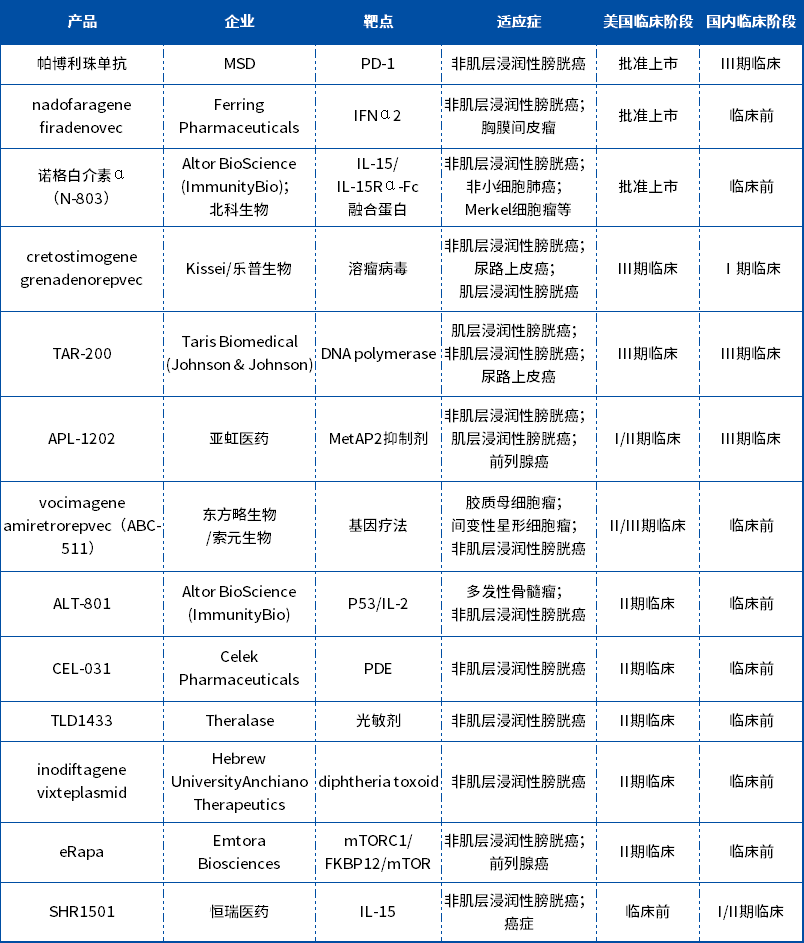
数据来源:药智数据、药智头条整理
(1)帕博利珠单抗:2020年1月8日,美国FDA批准Keytruda用于治疗卡介苗(BCG)治疗无反应、伴有或不伴有乳头状肿瘤,不适合或不接受膀胱切除术的高风险非肌层浸润性膀胱癌(NMIBC)患者。
该适应症的获批基于KEYNOTE-057研究,这是一项多中心、开放标签、单臂试验,入组对象为卡介苗(BCG)无应答、伴有或不伴有乳头状肿瘤,不适合或不接受膀胱切除术的高风险非肌层浸润性膀胱癌(NMIBC)患者。入组患者的人群特征为:中位年龄73岁,44%的患者≥75岁;男性占84%;67%的白人;ECOG评分为0(73%)或1(27%);基线高风险NMIBC疾病状态为持续性(27%)或复发性(73%)。试验结果表明,所有患者的CR为41%,中位DOR为16.2个月,DOR≥12个月的患者比例为46%。所有患者最常见的3~4级不良反应有:腹泻(2%)、尿路感染(2%)、关节痛(1.4%)、血尿(1.4%)、疲劳(0.7%)、皮疹(0.7%)、瘙痒(0.7%)。
(2)Adstiladrin是一种基于腺病毒载体的新型基因疗法,每三个月给药一次,通过导尿管注入患者膀胱,载体进入膀胱壁细胞,导致细胞分泌大量可对抗癌症的干扰素-2b蛋白。这种新型基因疗法将患者自身的膀胱壁细胞转变为干扰素微工厂,从而增强人体对癌症的天然防御能力。
2022年12月16日,FerringPharmaceuticals宣布,FDA已批准基因疗法Adstiladrin上市,用于治疗卡介苗(BCG)无响应的高风险非肌层浸润性膀胱癌(NMIBC)患者,这些患者伴有原位癌(CIS),可能携带或不携带状肿瘤。
FDA的批准是基于III期临床试验积极结果。该研究共纳入157例患者,其中98例原位癌患者伴有/不伴有高级别Ta或T1(CISTa/T1)。经过3个月1次Adstiladrin治疗后,有51%(50/98)患者实现了完全缓解(CR);在达到初始CR的患者中,有46%(23/50)在12个月时继续保持无高级别复发状态。研究中观察到的最常见的不良事件(AE)为:滴注部位分泌物(33%)、疲劳(24%)、膀胱痉挛(20%)、尿急(19%)和血尿(17%)等。因AE导致的停药率为1.9%。
(3)N-803是一种新型的IL-15超激动剂复合物,由ImmunityBio研发。N-803通过与β链-γT细胞受体结合直接刺激CD8+T细胞和NK细胞,同时避免刺激T调节细胞(T调节细胞)。2024年4月22日,ImmunityBio公司宣布,FDA已批准Anktiva(N-803)联合卡介苗(BCG),用于治疗卡介苗不响应的非肌层浸润性膀胱癌(NMIBC)伴原位癌(CIS),伴或不伴乳头状瘤患者。
N-803的BLA基于一项名为QUILT3032的II/III期试验,该临床试验在BCG无反应的高级别NMIBC患者中使用膀胱内BCG+N-803。在2022年泌尿生殖系统癌症研讨会上公布的该试验数据表明,在先前治疗失败的患者中,71%的患者达到了完全缓解(CR),中位缓解持续时间为26.6个月。此外,治疗使膀胱切除术避免率为91%,24个月膀胱癌总生存率为100%。也没有报告严重的不良反应。
但N-803的上市可谓一波三折。2023年5月11日,ImmunityBio表示,该公司IL-15超级激动剂Anktiva(N-803)与卡介苗联合治疗膀胱癌的上市申请被美国FDA拒绝批准。此次拒批主要是由于FDA在对其第三方合同制造商进行许可前检查时发现了缺陷。最终,于2024年4月,N-803解决了工艺问题后,终获FDA的批准。
非肌层浸润性膀胱癌潜力药物
多款非肌层浸润性膀胱癌药物处于临床三期,包括乐普生物引进的CG0070,亚虹医药的APL-1202等,均具有BIC药物的潜力。
(1)CG0070是由CGOncolog开发出的溶瘤病毒治疗癌症药物,是一种经过基因修饰的5型腺病毒(Ad5),联合免疫疗法具有BIC的潜力。修饰后,它包括癌症选择性启动子E2F-1和免疫细胞刺激因子GM-CSF基因,能够选择性地在Rb调控有缺陷的肿瘤细胞中复制并破裂肿瘤细胞。癌细胞破裂后,会释放出肿瘤原抗原和随病毒一起表达的GM-CSF,从而激发全身性抗肿瘤免疫应答。GM-CSF可以活化树突状细胞(DC),DC细胞能识别肿瘤抗原,并将其转递给细胞毒性和辅助性T细胞,从而促进它们的成熟。然后,这些T细胞会在全身内环流,去识别并攻击残存的肿瘤细胞。
CG0070正在对无法接受卡介苗(BCG)治疗的非肌层浸润性膀胱癌(NMIBC)患者进行第三期临床试验BOND-003。5月3日,CGOncology宣布,其在研溶瘤病毒疗法cretostimogene(CG0070)单药在治疗对卡介苗治疗无应答、高危非肌层浸润性膀胱癌(NMIBC)患者的有效性和安全性III期研究数据显示,75.2%的患者实现了完全缓解(CR),29例患者维持完全缓解超过12个月。
乐普生物拥有CG0070在中国区的开发、制造及商业化的权益。2021年3月,CG0070注射液IND申请获得CDE受理,适应症为卡介苗(BCG)无应答的非肌层浸润性膀胱癌。
(2)APL-1202是国际上首个进入关键性/Ⅲ期临床试验的非肌层浸润性膀胱癌(NMIBC)口服靶向治疗药物,具有抗血管生成、抗肿瘤活性及调节肿瘤免疫微环境的作用。
APL-1202治疗化疗灌注复发的高危NMIBC的2期临床试验展现出良好的效果。结果表明,经APL-1202治疗后患者的12个月无复发率为51.3%,显著高于化疗灌注药物的35%无复发率的历史研究数据。另外,经APL-1202治疗后患者的中位无复发生存期(mRFS)大于15个月,在12个月内无受试者进展为肌层浸润性膀胱癌。
然而,APL-1202最终折戟于三期临床研究。2024年2月4日,亚虹医药宣布,旗下核心在研产品APL-1202与化疗灌注联用二线治疗中高危“非肌层浸润性膀胱癌”(NMIBC)的临床研究未达到主要研究终点,决定终止APL-1202与化疗灌注联用在NMIBC治疗上的进一步开发。
尽管二线NMIBC研发失败,公司持续探索APL-1202联合PD-1新辅助治疗肌层浸润性膀胱癌。2023年,公司宣布APL-1202联合替雷利珠单抗新辅助治疗肌层浸润性膀胱癌Ⅱ期临床试验期中分析结果积极,pCR率相较于替雷利珠单抗单药治疗组大幅提升。APL-1202联合替雷利珠单抗预计将于2024年第三季度读出Ⅱ期试验的顶线数据。
小结
NMIBC在膀胱癌中占比达70%,具有易侵袭、易复发、易耐药、多中心等特性。目前对于NMIBC的治疗手段非常有限且复发率高,在BCG无效/复发情况下,推荐的治疗方案为根治性膀胱切除术,随后患者将终生携带尿袋。因此,对于化疗/卡介苗(BCG)无效/复发的NMIBC患者而言,亟待新的治疗方案。
目前,全球批准了三款用于卡介苗(BCG)无效/复发的NMIBC的药物,分别为帕博利珠单抗、Adstiladrin及N-803。聚焦国内,乐普生物引进了CG0070,联合帕博利珠单抗CR率达85%,具有潜在BIC的潜力。亚虹医药的APL-1202二线NMIBC适应症折戟,目前公司将研发聚焦于一线NMIBC适应症及联合PD-1新辅助治疗肌层浸润性膀胱癌,期待后续优异的临床数据。
参考资料:企业公告、药智数据等公开资料整理

责任编辑:白芨
声明:本文观点仅代表作者本人,不代表药智网立场,欢迎在留言区交流补充;如需转载,请务必注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。

研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938






