2016年6月CDE药品审评情况分析报告 ——药智注册与受理数据库
看点:
1.本月药品申报总量继续减少。
2.本月新增3个化药1.1类新药(按品种计)。
3.哈尔滨誉衡药业股份有限公司与无锡药明康德共同研发的抗PD-1单抗产品GLS-010注射液临床试验申请获得承办。
据药智数据库最新统计,2016年6月份CDE共承办新的药品注册申请以受理号计有255个(复审除外,下同)。
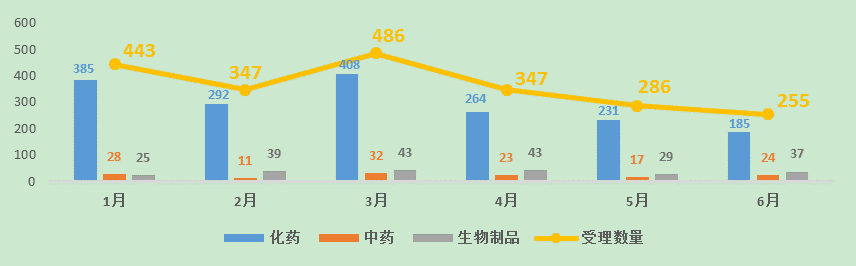
图一 2016年1-6月CDE药品受理情况
2016年6月,受理总量持续下降。从CDE收审情况来看,其中化药185个,中药24个,生物制品37个,药用辅料8个,体外诊断试剂1个。以下让我们分析一下化药、中药、生物制品的注册受理及审评情况。
一 化药
6月份CDE共承办新的化药注册申请以受理号计有185个。
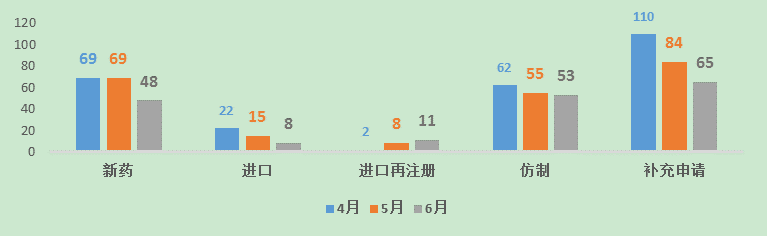
图二 2016年4-6月CDE化药各申请类型受理情况
从化药领域来看,2016年第二季度,与去年同期相比,化药受理数量下降达67.6%,重灾区即3.1类新药。新药、仿制药的注册申报继续下滑。
表一 2015年与2016年第二季度申报情况对比
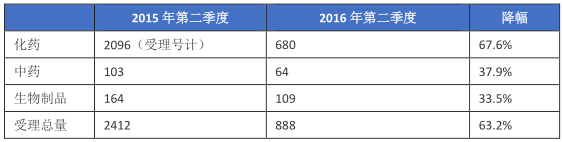
受化药申报的影响,药品受理总量也大幅下滑。
1.1类新药申报情况
本月CDE受理化药1.1类共计9个受理号,涉及3个品种3家企业。下图为6月新承办的1.1类新药。
表二 2016年6月新承办的化药1.1类新药
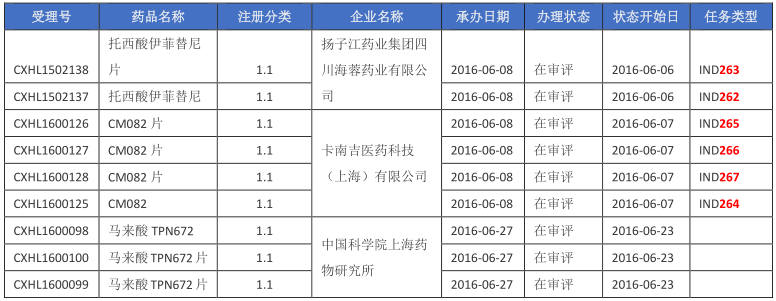
注:排队序号截止至2016年7月4日。
扬子江药业集团四川海蓉药业有限公司申报的托西酸伊菲替尼原料药及片剂于2016年6月8日获得药审中心受理,目前已进入IND序列排队待审。
卡南吉医药科技(上海)有限公司核心项目——抗肿瘤新药CM082及其片剂,于6月24日进入IND序列。早在2012年4月卡南吉获得了CM082胶囊的临床试验批件。据了解,面对艾科睿(卡南吉公司与美国艾科睿公司合作,在中美两国同步进行新药项目CM082的研发)在美国的实验结果,发现 CM082的片剂剂型比已有的胶囊剂型药效提高好几倍,同时,改用片剂意味着临床剂量要小好几倍,今后中国的癌症患者需要支付的用药费用会大幅降低。权衡之下,该公司于2012年12月,申报片剂临床试验(按补充申请申报),仅3个多月就拿到临床批件。
CM082的最大特点在于它不但具有针对VEGFR和PDGFR靶点的显著疗效,同时克服了这一类靶向药常见的高毒副作用。因此,它不但可以应用于抗肿瘤领域,同时有希望应用于很多种非肿瘤适应症,特别是眼底病适应症的治疗。
表三 CM082国内相关临床试验
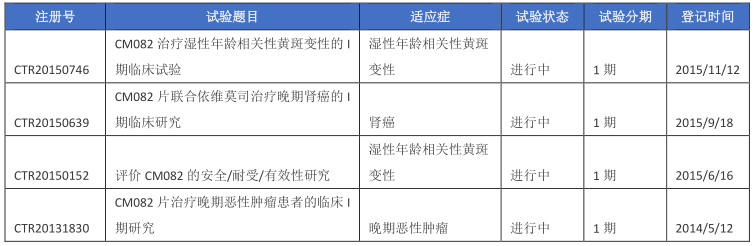
数据来源:药智网中国临床试验数据库
马来酸TPN672为中国科学院上海药物研究所2016年申报的第二项1.1类新药,目前暂未查到相关适应症信息。3月研究所申报了另一项1.1类新药谷美替尼,已进入IND序列。
二 中药
6月份CDE承办新的中药注册申请受理号共计24个,其中新药2个,补充申请21个,进口再注册1个。

图三 2016年4-6月CDE中药受理情况
三 生物制品
6月份CDE承办新的生物制品注册申请受理号共计37个,新药6个,补充申请24个,进口7个。
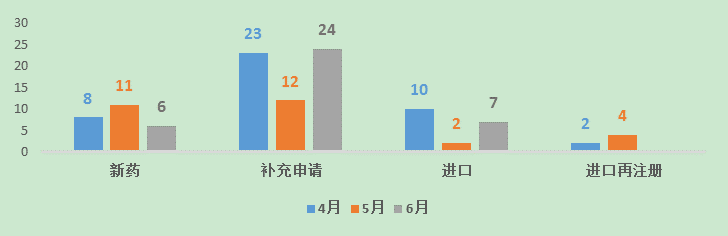
图四 2016年4-6月CDE生物制品受理情况
本月有1个1类生物制品受理号获得承办,目前已经进入临床试验申请序列排队待审。
表四 2016年6月新承办的生物制品1类新药

注:排队序号截止至2016年7月4日。
哈尔滨誉衡药业股份有限公司与与药明康德共同研发的抗PD-1单抗产品GLS-010注射液(规格:120mg/4.0ml/瓶),根据其公司公告知,与传统的放化疗等治疗手段相比,以PD-1单克隆抗体为代表的免疫检查点抗体药物在近期引发了抗肿瘤药物的一场革命,它具有疗效显著、副作用小等突出优点,尤其在与其它抗肿瘤药物的联合用药方面具有广泛前景。在国内PD-1抗体药物研发领域,GLS-010注射液是由国内研发机构完成临床申报的首个全人源抗 PD-1 单克隆抗体,具有完善的自主知识产权。
注:本文以上文章刊载内容知识产权归药智网所有,如需转载,请注明出处和作者。


研发/政策栏目
小张 2512509353 15213063982药圈/会展栏目
小徐 838568582 18202350072商业/器械栏目
小洋 2108599521 18502370446前沿/报告栏目
小娟 368946684 17783467842合作
合作咨询
 扫码关注-药智头条
扫码关注-药智头条药智网旗下药智新闻订阅号
Copyright © 2009-2024 药智网YAOZH.COM All Rights Reserved. 工信部备案号:渝ICP备10200070号-3
 渝公网安备 50010802001068号
渝公网安备 50010802001068号投诉热线: (023) 6262 8397
邮箱: tousu@yaozh.com
QQ: 236960938





